铁酸锌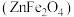 是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
Ⅰ.制备前驱物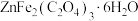
①分别配制 溶液和
溶液和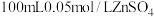 溶液,并将二者混合备用。
溶液,并将二者混合备用。
②另外称取 溶于
溶于 蒸馏水中。
蒸馏水中。
③将①和②所得溶液混合加热到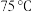 ,并在
,并在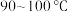 加热搅拌
加热搅拌 ;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
Ⅱ.制备铁酸锌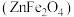
将步骤Ⅰ所得前驱物在 灼烧
灼烧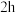 ,冷却后称量质量为
,冷却后称量质量为 ,计算产率。
,计算产率。
回答下列问题:
(1)步骤Ⅰ中配制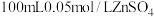 溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、
溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、 容量瓶和
容量瓶和___________ 。下列关于容量瓶的操作,正确的是___________ (填标号)。 晶体,加水溶解,滴加
晶体,加水溶解,滴加___________ (填写试剂名称),无明显现象,由此可知样品___________ (填“已”或“未”)变质。
(3)步骤Ⅰ中检验沉淀是否洗涤干净的操作是___________ 。
(4)步骤Ⅱ中“灼烧”发生的反应属于分解反应,其化学方程式为___________ 。
(5)该实验的总产率为___________ 。
(6) 晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示
晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示 。则“●”表示的微粒是
。则“●”表示的微粒是___________ (填符号), 晶体的密度为
晶体的密度为___________  (已知晶胞参数为
(已知晶胞参数为 ,列出计算式)。
,列出计算式)。
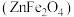 是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:Ⅰ.制备前驱物
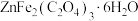
①分别配制
 溶液和
溶液和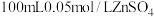 溶液,并将二者混合备用。
溶液,并将二者混合备用。②另外称取
 溶于
溶于 蒸馏水中。
蒸馏水中。③将①和②所得溶液混合加热到
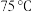 ,并在
,并在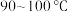 加热搅拌
加热搅拌 ;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。Ⅱ.制备铁酸锌
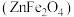
将步骤Ⅰ所得前驱物在
 灼烧
灼烧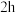 ,冷却后称量质量为
,冷却后称量质量为 ,计算产率。
,计算产率。回答下列问题:
(1)步骤Ⅰ中配制
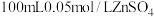 溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、
溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、 容量瓶和
容量瓶和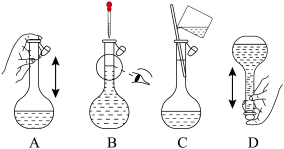
 晶体,加水溶解,滴加
晶体,加水溶解,滴加(3)步骤Ⅰ中检验沉淀是否洗涤干净的操作是
(4)步骤Ⅱ中“灼烧”发生的反应属于分解反应,其化学方程式为
(5)该实验的总产率为
(6)
 晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示
晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示 。则“●”表示的微粒是
。则“●”表示的微粒是 晶体的密度为
晶体的密度为 (已知晶胞参数为
(已知晶胞参数为 ,列出计算式)。
,列出计算式)。
更新时间:2024-05-20 16:38:07
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】碱式氧化镍(NiOOH)可作镍电池的正极材料,现用某废镍原料(主要含Ni、Al、SiO2,少量Cr、FeS等)来制备,其工艺流程如下:
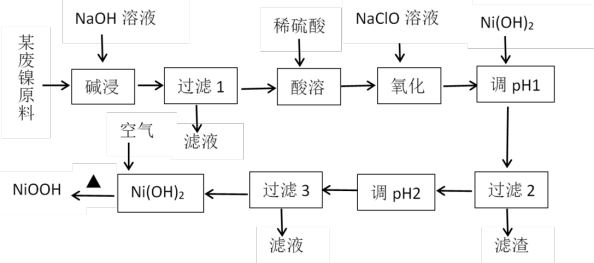
回答下列问题:
(1)“碱浸”时,发生反应的离子反应方程式①____________ ,②____________ 。
(2)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
“调pH 1”时,主要除去的离子是____ ,溶液pH范围____ 。
(3)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式______ 。
(4)在酸性溶液中CrO 可以转化成Cr2O
可以转化成Cr2O ,用离子方程式表示该转化反应
,用离子方程式表示该转化反应____ ,已知BaCrO4的Ksp=1.2×10-10,要使溶液中CrO 沉淀完全(c(CrO
沉淀完全(c(CrO )≤1×10-5mol·L-1),溶液中钡离子浓度至少为
)≤1×10-5mol·L-1),溶液中钡离子浓度至少为___ mol·L-1。

回答下列问题:
(1)“碱浸”时,发生反应的离子反应方程式①
(2)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,主要除去的离子是
(3)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式
(4)在酸性溶液中CrO
 可以转化成Cr2O
可以转化成Cr2O ,用离子方程式表示该转化反应
,用离子方程式表示该转化反应 沉淀完全(c(CrO
沉淀完全(c(CrO )≤1×10-5mol·L-1),溶液中钡离子浓度至少为
)≤1×10-5mol·L-1),溶液中钡离子浓度至少为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】活性炭载钯(Pd/C)催化剂被广泛应用于医药和化工行业,某废钯催化剂(钯碳)的杂质主要含炭、有机物及少量Fe等。如图是利用钯碳制备氯化钯(PdCl2)和Pd的流程。

回答下列问题:
(1)“钯灰”中的主要成分有PdO,加入甲酸(HCOOH),可以将PdO还原成金属单质,请写出HCOOH还原PdO的化学方程式___________ 。
(2)“焚烧”的目的是____ ;实验室中可在___________ (填仪器名称)中模拟该过程。
(3)王水是将浓盐酸和浓硝酸混合而得到的强氧化性溶液,加热条件下钯在王水中发生反应生成H2[PdCl4]和一种有毒的无色气体A,该气体遇空气变红棕色,该反应中消耗的HCl与HNO3的物质的量之比为___________ 。
(4)加入浓氨水,调节溶液pH至9.0,并控制温度在70 ~75℃,Pd元素以 的形式存在:
的形式存在:
①若温度大于75℃,则不利于除铁,原因是___________
②已知:黄色晶体的成分为 ,在合并液中加盐酸时,发生反应的离子方程式为
,在合并液中加盐酸时,发生反应的离子方程式为___________ 。
(5)洗涤滤渣并将洗涤液与滤液合并,其意义是___________ 。
(6)Pd是优良的储氢金属,假设海绵状金属钯密度为,ρg·cm-3标准状况下其吸附的氢气是其体积的n倍,则此条件下海绵钯的储氢容量R=___________ mL·g-1(储氢容量R即1g钯吸附氢气的体积)。

回答下列问题:
(1)“钯灰”中的主要成分有PdO,加入甲酸(HCOOH),可以将PdO还原成金属单质,请写出HCOOH还原PdO的化学方程式
(2)“焚烧”的目的是
(3)王水是将浓盐酸和浓硝酸混合而得到的强氧化性溶液,加热条件下钯在王水中发生反应生成H2[PdCl4]和一种有毒的无色气体A,该气体遇空气变红棕色,该反应中消耗的HCl与HNO3的物质的量之比为
(4)加入浓氨水,调节溶液pH至9.0,并控制温度在70 ~75℃,Pd元素以
 的形式存在:
的形式存在:①若温度大于75℃,则不利于除铁,原因是
②已知:黄色晶体的成分为
 ,在合并液中加盐酸时,发生反应的离子方程式为
,在合并液中加盐酸时,发生反应的离子方程式为(5)洗涤滤渣并将洗涤液与滤液合并,其意义是
(6)Pd是优良的储氢金属,假设海绵状金属钯密度为,ρg·cm-3标准状况下其吸附的氢气是其体积的n倍,则此条件下海绵钯的储氢容量R=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如图:
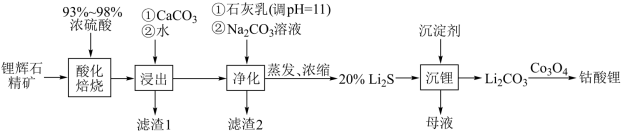
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为___ 。
②为提高“酸化焙烧”效率,常采取的措施是___ 。
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为___ 。(已知:,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,完全沉淀后离子浓度低于1×l0-5)mol/L)。
④“滤渣2”的主要化学成分为___ 。
⑤“沉锂”过程中加入的沉淀剂为饱和的___ (化学式)溶液。
(2)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6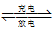 LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是
LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是___ (填字母)。
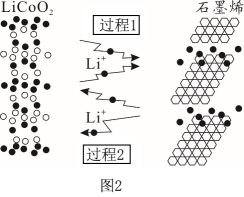
A.过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(3)LiFePO4也是一种电动汽车电池的电极材料,实验室先将绿矾溶解在磷酸中,再加入氢氧化钠和次氯酸钠溶液反应获得FePO4固体。再将FePO4固体与H2C2O4和LiOH反应即可获得LiFePO4同时获得两种气体。
①写出FePO4固体与H2C2O4和LiOH反应溶液获得LiFePO4的化学方程式___ 。
②LiFePO4需要在高温下成型才能作为电极,高温成型时要加入少量活性炭黑,其作用是___ 。
(1)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如图:

回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为
②为提高“酸化焙烧”效率,常采取的措施是
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为
④“滤渣2”的主要化学成分为
⑤“沉锂”过程中加入的沉淀剂为饱和的
(2)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6
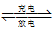 LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是
LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是
A.过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(3)LiFePO4也是一种电动汽车电池的电极材料,实验室先将绿矾溶解在磷酸中,再加入氢氧化钠和次氯酸钠溶液反应获得FePO4固体。再将FePO4固体与H2C2O4和LiOH反应即可获得LiFePO4同时获得两种气体。
①写出FePO4固体与H2C2O4和LiOH反应溶液获得LiFePO4的化学方程式
②LiFePO4需要在高温下成型才能作为电极,高温成型时要加入少量活性炭黑,其作用是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知A、B、C、D、E是周期表中前四周期原子序数依次增大的五种元素。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同。D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。含E元素的硫酸盐溶液是制备波尔多液的原料之一。按要求回答下列问题:
(1)五种元素中第一电离能最大的是__________ ,电负性最大的是__________ 。(以上两空均填元素名称)
(2)基态E原子的价电子排布式为__________ ;E元素所在周期中基态原子的成单电子数最多的元素是__________ (填元素符号)
(3)M分子中B原子的轨道杂化类型为__________ ,M分子中两种键角的大小关系是__________ 。(用∠XYZ表示,X、Y、Z代表元素符号)
(4)C3-的空间构型为__________ ;化合物CA3的沸点比BA4的高,其主要原因是__________ 。
(5)向E元素的硫酸盐溶液中通入过量的CA3,得到深蓝色的透明溶液,在此溶液中加入乙醇,析出深蓝色的晶体,此晶体中存在的化学键类型有__________ 。(填代号)
A.离子键 B.σ键 C.非极性共价键 D.配位键 E.金属键 F.氢键
(6)如图是D、E两种元素形成的化合物的晶胞结构示意图,D的配位数为__________ 。已知晶胞中最近两个D原子间距离为anm,,阿伏伽德罗常数用NA表示,则该晶体的密度为__________ g/cm3(用含a、NA的表达式表示)
(1)五种元素中第一电离能最大的是
(2)基态E原子的价电子排布式为
(3)M分子中B原子的轨道杂化类型为
(4)C3-的空间构型为
(5)向E元素的硫酸盐溶液中通入过量的CA3,得到深蓝色的透明溶液,在此溶液中加入乙醇,析出深蓝色的晶体,此晶体中存在的化学键类型有
A.离子键 B.σ键 C.非极性共价键 D.配位键 E.金属键 F.氢键
(6)如图是D、E两种元素形成的化合物的晶胞结构示意图,D的配位数为

您最近一年使用:0次
【推荐2】甲醇是重要的化工基础原料和清洁液体燃料,在 加氢合成
加氢合成 的体系中,同时发生下列竞争反应:
的体系中,同时发生下列竞争反应:
(ⅰ)
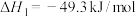
(ⅱ)
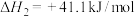
由CO也能直接加氢合成甲醇:(ⅲ)

(1)
_____ kJ/mol。
(2)反应(ⅱ) 的正、逆反应平衡常数随温度变化曲线如图所示。
的正、逆反应平衡常数随温度变化曲线如图所示。
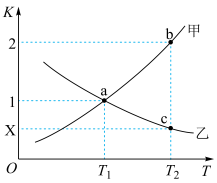
下列分析正确的是______ 。
A.曲线甲为K(逆),曲线乙为K(正) B.a点时,一定有 C.c点时,x=0.5
C.c点时,x=0.5
(3)催化剂M、N对 反应进程的能量影响如下图(a)所示,两种催化剂对应的
反应进程的能量影响如下图(a)所示,两种催化剂对应的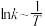 关系如下图(b)所示(已知;
关系如下图(b)所示(已知; ,其中
,其中 为活化能,k为速率常数,R和C为常数)。
为活化能,k为速率常数,R和C为常数)。
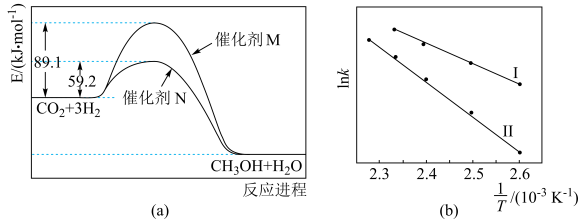
①使用催化剂M时,逆反应的活化能为______ kJ/mol。
②催化剂N对应曲线是图(b)中的______ (填“Ⅰ”或“Ⅱ”)
(4)为进一步研究 与
与 反应制
反应制 的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内。测得生成甲醇的速率与温度的关系如图所示。
的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内。测得生成甲醇的速率与温度的关系如图所示。
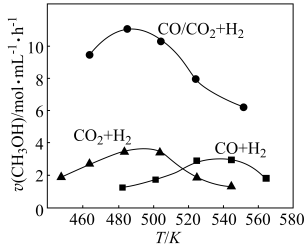
①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是_______ 。
②结合研究目的,参照图中三条曲线,你可得出的结论是____ (写一条)。
(5)恒温下,在压强恒定为P的装置中,按 加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若
加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若 转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)
转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)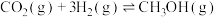
 的平衡常数计算式:
的平衡常数计算式:
______ (不必化简)。(已知: 的选择性
的选择性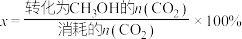 ;
; 为用分压代替浓度的平衡常数。)
为用分压代替浓度的平衡常数。)
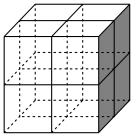
(6) 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体。边长为a nm,Ni原子占据顶点和面心,
晶胞形状为如图立方体。边长为a nm,Ni原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
①Ni原子的价电子排布式为______ 。
② 位于Ni原子形成的
位于Ni原子形成的______ (填“八面体空隙”或“四面体空隙”)。
③该晶体的密度为_____  (用含a、
(用含a、 代数式表示)。
代数式表示)。
 加氢合成
加氢合成 的体系中,同时发生下列竞争反应:
的体系中,同时发生下列竞争反应:(ⅰ)

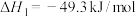
(ⅱ)

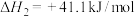
由CO也能直接加氢合成甲醇:(ⅲ)


(1)

(2)反应(ⅱ)
 的正、逆反应平衡常数随温度变化曲线如图所示。
的正、逆反应平衡常数随温度变化曲线如图所示。
下列分析正确的是
A.曲线甲为K(逆),曲线乙为K(正) B.a点时,一定有
 C.c点时,x=0.5
C.c点时,x=0.5(3)催化剂M、N对
 反应进程的能量影响如下图(a)所示,两种催化剂对应的
反应进程的能量影响如下图(a)所示,两种催化剂对应的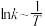 关系如下图(b)所示(已知;
关系如下图(b)所示(已知; ,其中
,其中 为活化能,k为速率常数,R和C为常数)。
为活化能,k为速率常数,R和C为常数)。
①使用催化剂M时,逆反应的活化能为
②催化剂N对应曲线是图(b)中的
(4)为进一步研究
 与
与 反应制
反应制 的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内。测得生成甲醇的速率与温度的关系如图所示。
的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内。测得生成甲醇的速率与温度的关系如图所示。
①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是
②结合研究目的,参照图中三条曲线,你可得出的结论是
(5)恒温下,在压强恒定为P的装置中,按
 加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若
加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若 转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)
转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)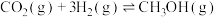
 的平衡常数计算式:
的平衡常数计算式:
 的选择性
的选择性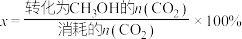 ;
; 为用分压代替浓度的平衡常数。)
为用分压代替浓度的平衡常数。)(6)
 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体。边长为a nm,Ni原子占据顶点和面心,
晶胞形状为如图立方体。边长为a nm,Ni原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
①Ni原子的价电子排布式为
②
 位于Ni原子形成的
位于Ni原子形成的③该晶体的密度为
 (用含a、
(用含a、 代数式表示)。
代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期。
(1)F原子基态的外围核外电子排布式为___________ ;
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为___________ ;
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为___________ ;
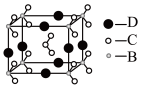
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________ ;
(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物。下列说法正确的是___________;
(6)NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4该配合物中心离子的配体为___________ ,其中提供空轨道的是___________ (填微粒符号)。
(1)F原子基态的外围核外电子排布式为
(2)由A、B、C形成的离子CAB﹣与AC2互为等电子体,则CAB﹣的结构式为
(3)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为
(4)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为

(5)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOx、CH2═CHCHO、HCOOH、CH3COONO2(PAN)等二次污染物。下列说法正确的是___________;
| A.N2O为直线型分子 |
| B.C、N、O的第一电离能依次增大 |
| C.CH2═CH一CHO分子中碳原子均采用sp2杂化 |
| D.相同压强下,HCOOH沸点比CH3OCH3高,说明前者是极性分子,后者是非极性分子 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】现需要0.1 mol·L−1CuSO4溶液240 mL,实验室提供以下试剂用于溶液的配制:蒸馏水、胆矾晶体(CuSO4·5H2O)、4 mol·L−1CuSO4溶液
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是_________ ,在使用该仪器前必须进行的操作是___________ 。
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4·5H2O的质量为_______ g;如果用 4 mol/L的CuSO4溶液稀释配制,需用量筒量取________ mL 4 mol/L CuSO4溶液。
(3)用4 mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:
a.用量筒量取一定体积4 mol/L的硫酸铜溶液于一烧杯中
b.洗涤烧杯和玻璃棒2~3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
c.计算所需4 mol/L硫酸铜溶液的体积
d.盖好瓶塞,反复上下颠倒摇匀后,将溶液转存于试剂瓶中
e.加水至液面离容量瓶刻度线1~2 cm处改用胶头滴管进行定容
f.往烧杯中加入约100 mL水进行初步稀释,冷却至室温
g.将溶液转移入容量瓶
其中正确的操作顺序为______________________ 。
(4)下列操作对所配制溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①称取的胆矾晶体失去了部分结晶水___________ 。
②定容时,仰视刻度线:___________ 。
③容量瓶未干燥,有少量蒸馏水:___________ 。
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4·5H2O的质量为
(3)用4 mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:
a.用量筒量取一定体积4 mol/L的硫酸铜溶液于一烧杯中
b.洗涤烧杯和玻璃棒2~3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
c.计算所需4 mol/L硫酸铜溶液的体积
d.盖好瓶塞,反复上下颠倒摇匀后,将溶液转存于试剂瓶中
e.加水至液面离容量瓶刻度线1~2 cm处改用胶头滴管进行定容
f.往烧杯中加入约100 mL水进行初步稀释,冷却至室温
g.将溶液转移入容量瓶
其中正确的操作顺序为
(4)下列操作对所配制溶液浓度的影响(填“偏高”“偏低”或“无影响”)。
①称取的胆矾晶体失去了部分结晶水
②定容时,仰视刻度线:
③容量瓶未干燥,有少量蒸馏水:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】Ⅰ.配制480 mL 0.3 mol/L NaOH溶液。具体如下:
(1)需______ g NaOH。
(2)配制过程中,下列仪器不会用到的是___________ (填字母) ,尚缺少的玻璃仪器有_____________ 。
A.托盘天平 B.250 mL容量瓶 C.玻璃棒 D.胶头滴管
(3)实验过程中两次用到玻璃棒,其作用分别是:_______________________ 、_____________________ 。
(4)定容操作:将蒸馏水注入所选的容器中,直到其中液面接近其刻度线______ 处时,改用______ 滴加蒸馏水至溶液的______ 正好与刻度线______ 。将瓶塞子盖好,反复______ 摇匀。
(5)下列操作的正确顺序是:B→______ →______ →______ →______ →______ →G (用字母表示)。
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.转移 G.摇匀
Ⅱ.乙同学用18.4 mol/L浓硫酸配制100 mL 3.6 mol/L的稀硫酸。
用100 mL量筒量取20 mL浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处_____________________ 。
Ⅲ.在配制物质的量浓度溶液时,判断下列操作出现的后果。(填“溶液浓度不准确”、“偏低”、“偏高”或“无影响”)
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体:_____________ 。
(2)配制氢氧化钠溶液时,容量瓶中有少量水:______________ 。
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度:____________ 。
(4) 转移时不慎将溶液倒在瓶外:____________ ;
(5)定容时俯视容量瓶刻度线:____________ 。
(1)需
(2)配制过程中,下列仪器不会用到的是
A.托盘天平 B.250 mL容量瓶 C.玻璃棒 D.胶头滴管
(3)实验过程中两次用到玻璃棒,其作用分别是:
(4)定容操作:将蒸馏水注入所选的容器中,直到其中液面接近其刻度线
(5)下列操作的正确顺序是:B→
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.转移 G.摇匀
Ⅱ.乙同学用18.4 mol/L浓硫酸配制100 mL 3.6 mol/L的稀硫酸。
用100 mL量筒量取20 mL浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。
你认为此法是否正确?若不正确,指出其中错误之处
Ⅲ.在配制物质的量浓度溶液时,判断下列操作出现的后果。(填“溶液浓度不准确”、“偏低”、“偏高”或“无影响”)
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体:
(2)配制氢氧化钠溶液时,容量瓶中有少量水:
(3)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度:
(4) 转移时不慎将溶液倒在瓶外:
(5)定容时俯视容量瓶刻度线:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医疗上常用作补血剂。某课外活动小组为测定该补血剂中铁元素的含量,设计如下实验。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为______ mL(保留一位小数)。
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为__________________________ 。
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为_______________________ 。
(4)该补血剂中铁元素的质量分数为____________ ,若步骤③加入氨水的量不足,则实验结果_____ (填“偏大”、“偏小”、“无影响”)
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是_________________ 。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为
(4)该补血剂中铁元素的质量分数为
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】水钴矿的主要成分为Co2O3,还含SiO2及少量Al2O3、Fe2O3、 CuO、MnO2等。一种利用水钴矿制取CoCl2·6H2O 的工艺流程如下:
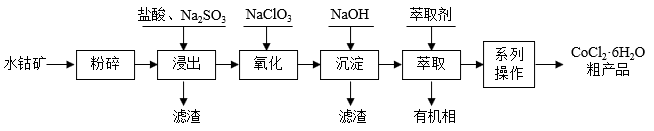
已知: ①CoCl2·6H2O受热易失去结晶水。
②25 ℃时,设定溶液中某金属离子初始浓度为0.1 mol•L-1,部分沉淀的参考数据如下表(“沉淀完全”指溶液中该离子浓度≤1.0×10-5mol•L-1):
回答下列问题
(1)计算25℃时Co(OH)2的Ksp =_______________ 。
(2)浸出工序中加入一定量的Na2SO3还原Co2O3、MnO2等,Co2O3发生反应的离子方程式为_______________________________ 。
(3)氧化工序要控制NaClO3用量,若不慎加入过量NaClO3,可能生成的有毒气体是______________ ;氧化工序主要反应的离子方程式为_______________________________ 。
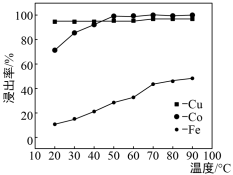
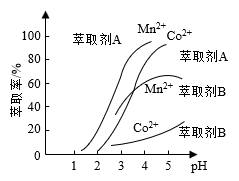
(4)已知温度对铜、钴、铁的浸出率的影响如左下图,萃取剂A、B中pH对钴、锰离子萃取率的影响如右下图:
①浸出温度控制在50-60℃的原因是_________________________ 。
②应选择萃取剂_________________________ (填“A”或“B”)。
(5)“系列操作”依次是____________ 、______________ 和过滤等;制得的CoCl2·6H2O需减压烘干的原因是_________________________ 。

已知: ①CoCl2·6H2O受热易失去结晶水。
②25 ℃时,设定溶液中某金属离子初始浓度为0.1 mol•L-1,部分沉淀的参考数据如下表(“沉淀完全”指溶液中该离子浓度≤1.0×10-5mol•L-1):
| 沉淀 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.4 | 1.5 | 6.3 | 7.0 | 4.7 | 8.1 |
| 沉淀完全时pH | 4.7 | 2.8 | 8.3 | 9.0 | 6.7 | 10.1 |
回答下列问题
(1)计算25℃时Co(OH)2的Ksp =
(2)浸出工序中加入一定量的Na2SO3还原Co2O3、MnO2等,Co2O3发生反应的离子方程式为
(3)氧化工序要控制NaClO3用量,若不慎加入过量NaClO3,可能生成的有毒气体是
(4)已知温度对铜、钴、铁的浸出率的影响如左下图,萃取剂A、B中pH对钴、锰离子萃取率的影响如右下图:


①浸出温度控制在50-60℃的原因是
②应选择萃取剂
(5)“系列操作”依次是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】二氯异氰尿酸钠(NaC3N3O3Cl2)是一种高效广谱杀菌消毒剂,常温下为白色固体,难溶于冷水。其制备原理为2NaClO+C3H3N3O2 NaC3N3O3Cl2+NaOH+H2O。请选择如图所示部分装置制备二氯异氰尿酸钠并测定其纯度。
NaC3N3O3Cl2+NaOH+H2O。请选择如图所示部分装置制备二氯异氰尿酸钠并测定其纯度。
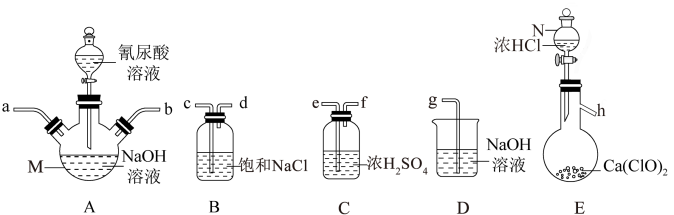
请回答下列问题:
(1)仪器M的名称是_______ 。若发现实际操作过程当中N中的浓HCl不易滴下,可将装置N改为_______ 。
(2)装置B的作用是_______ 。
(3)E中发生反应的化学方程式为_______ 。
(4)选择合适装置,按气流从左至右,导管连接顺序为_______ (填序号)。
(5)实验时,先向A中通入氯气,生成高浓度的NaClO溶液后,才加入氰尿酸溶液,而且整个过程中不断通入一定量的氯气,其原因是_______ 。
(6)反应结束后,A中浊液经过滤、_______ 、_______ 得到粗产品mg。
(7)粗产品中NaC3N3O3Cl2含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用cmol/LNa2S2O3的标准溶液进行滴定,加入指示剂,滴定至终点,消耗VmLNa2S2O3溶液。(假设杂质不与KI反应)已知: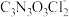 +3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2
+3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2 =2I-+
=2I-+ 。
。
①滴定过程中加入的指示剂是_______ 。
②根据上述数据计算NaC3N3O3Cl2的百分含量为_______ %。[用含m,c,V的代数式表示,已知M(NaC3N3O3Cl2)=220g/mol]
 NaC3N3O3Cl2+NaOH+H2O。请选择如图所示部分装置制备二氯异氰尿酸钠并测定其纯度。
NaC3N3O3Cl2+NaOH+H2O。请选择如图所示部分装置制备二氯异氰尿酸钠并测定其纯度。
请回答下列问题:
(1)仪器M的名称是
(2)装置B的作用是
(3)E中发生反应的化学方程式为
(4)选择合适装置,按气流从左至右,导管连接顺序为
(5)实验时,先向A中通入氯气,生成高浓度的NaClO溶液后,才加入氰尿酸溶液,而且整个过程中不断通入一定量的氯气,其原因是
(6)反应结束后,A中浊液经过滤、
(7)粗产品中NaC3N3O3Cl2含量测定。将mg粗产品溶于无氧蒸馏水中配制成100mL溶液,取20.00mL所配制溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min。用cmol/LNa2S2O3的标准溶液进行滴定,加入指示剂,滴定至终点,消耗VmLNa2S2O3溶液。(假设杂质不与KI反应)已知:
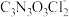 +3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2
+3H++4I-=C3H3N3O3+2I2+2Cl-,I2+2 =2I-+
=2I-+ 。
。①滴定过程中加入的指示剂是
②根据上述数据计算NaC3N3O3Cl2的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】硫氰化钾(KSCN)是中学实验室的常见药品,某校化学兴趣小组在实验室制备少量样品,并进行探究实验。他们查阅有关资料:CS2+2NH3 NH4SCN+H2S,该反应比较缓慢。
NH4SCN+H2S,该反应比较缓慢。
Ⅰ.制备KSCN样品。
(1)制备NH4SCN溶液,装置如图:
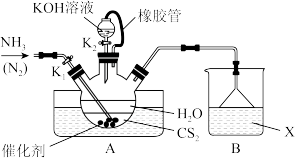
①实验开始时打开K1,关闭K2,加热水浴装置,缓缓地向三颈烧瓶中持续通入NH3和N2,导气管末端伸入CS2层的目的是___________ 。
②一段时间后,当CS2反应完毕,停止实验,此时可以观察到三颈烧瓶内的现象是___________ 。
③为了防止反应产物泄漏污染环境,烧杯内的X可为CuCl2溶液,则B中的离子反应方程式为___________ 。
(2)再制备KSCN溶液:关闭K1,打开K2,利用耐碱分液漏斗缓慢加入适量KOH溶液,继续加热,此时三颈烧瓶中发生反应的化学方程式是___________ 。
Ⅱ.KSCN的探究实验,同学们用实验室配制的KSCN溶液做下列实验。
(3)同学甲想利用反应Fe3++3SCN− Fe(SCN)3来检验溶液中的Fe3+。KSCN中,碳的化合价为
Fe(SCN)3来检验溶液中的Fe3+。KSCN中,碳的化合价为___________ 。
(4)同学乙往FeCl2和KSCN的混合溶液中滴加氯水,溶液变成红色,不过他注意到,当氯水过量时,红色会褪去,为此,他设计如图装置进行探究。
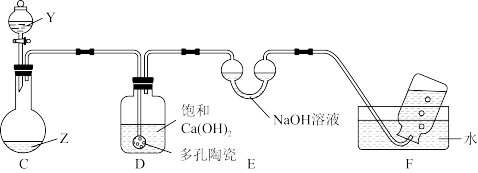
Y为NaClO溶液,Z为FeCl3和KSCN的混合溶液。打开分液漏斗,持续缓慢滴入NaClO溶液至过量,他观察到:C中红色变浅,有大量气泡产生,D中的澄清石灰水变浑浊,F中有气泡。以此为依据分析,C中还有的现象为___________ ;试写出向C中滴加适量NaClO溶液后,溶液中KSCN发生反应的离子方程式___________ (经检测产物中有SO 生成)
生成)
 NH4SCN+H2S,该反应比较缓慢。
NH4SCN+H2S,该反应比较缓慢。Ⅰ.制备KSCN样品。
(1)制备NH4SCN溶液,装置如图:

①实验开始时打开K1,关闭K2,加热水浴装置,缓缓地向三颈烧瓶中持续通入NH3和N2,导气管末端伸入CS2层的目的是
②一段时间后,当CS2反应完毕,停止实验,此时可以观察到三颈烧瓶内的现象是
③为了防止反应产物泄漏污染环境,烧杯内的X可为CuCl2溶液,则B中的离子反应方程式为
(2)再制备KSCN溶液:关闭K1,打开K2,利用耐碱分液漏斗缓慢加入适量KOH溶液,继续加热,此时三颈烧瓶中发生反应的化学方程式是
Ⅱ.KSCN的探究实验,同学们用实验室配制的KSCN溶液做下列实验。
(3)同学甲想利用反应Fe3++3SCN−
 Fe(SCN)3来检验溶液中的Fe3+。KSCN中,碳的化合价为
Fe(SCN)3来检验溶液中的Fe3+。KSCN中,碳的化合价为(4)同学乙往FeCl2和KSCN的混合溶液中滴加氯水,溶液变成红色,不过他注意到,当氯水过量时,红色会褪去,为此,他设计如图装置进行探究。

Y为NaClO溶液,Z为FeCl3和KSCN的混合溶液。打开分液漏斗,持续缓慢滴入NaClO溶液至过量,他观察到:C中红色变浅,有大量气泡产生,D中的澄清石灰水变浑浊,F中有气泡。以此为依据分析,C中还有的现象为
 生成)
生成)
您最近一年使用:0次



