X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(水及部分产物已略去)。
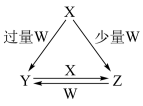
(1)若X为金属单质,W是某强酸的稀溶液。X与过量W反应生成Y的离子方程式为_________ 。向Z溶液中加入某种试剂_______ (填试剂名称或化学式),若出现蓝色沉淀,即可判断Z溶液中阳离子的存在。
(2)若X为非金属单质,W是空气的主要成分之一。它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为_______ 。
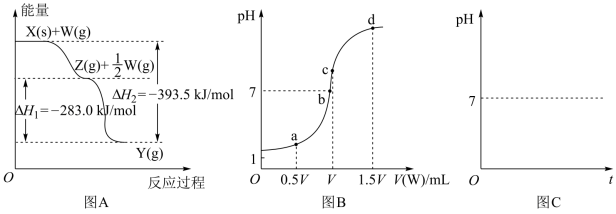
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为_______ 。室温下,若用0.1 mol/L的W溶液滴定V mL 0.1 mol/L HA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是______ 点;a点溶液中离子浓度的大小顺序为______________ ;取少量c点溶液于试管中,再滴加0.1 mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为______________ 。
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图(不考虑水的挥发)。______________

(1)若X为金属单质,W是某强酸的稀溶液。X与过量W反应生成Y的离子方程式为
(2)若X为非金属单质,W是空气的主要成分之一。它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为

(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图(不考虑水的挥发)。
更新时间:2016-12-09 07:18:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】固体化合物X由3种元素组成。某学习小组进行了如下实验:
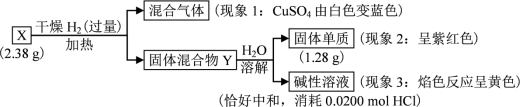
回答:
(1)由现象1得出化合物X含有_______ 元素(填元素符号)。
(2)固体混合物Y的成分_______ (填化学式)。
(3)X的化学式_______ 。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,且黄绿色气体与蓝色溶质物质的量之比为1:2,写出该反应的化学 方程式:_______ 。
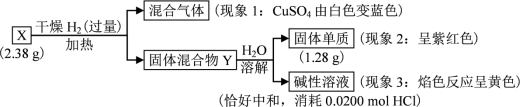
回答:
(1)由现象1得出化合物X含有
(2)固体混合物Y的成分
(3)X的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】各物质间的转化关系如下图所示,请完成下列空白
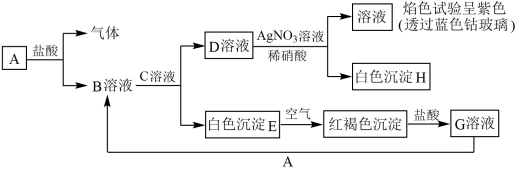
(1)写出D和B的化学式:D___________ ,B___________
(2)写出E转化为红褐色沉淀的化学方程式:___________
(3)写出向G溶液中加入A后的离子方程式:___________
(4)向G溶液中加入Cu也能生成B,写出加入Cu的离子方程式___________

(1)写出D和B的化学式:D
(2)写出E转化为红褐色沉淀的化学方程式:
(3)写出向G溶液中加入A后的离子方程式:
(4)向G溶液中加入Cu也能生成B,写出加入Cu的离子方程式
您最近一年使用:0次
【推荐3】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:

请回答下列问题。
(1)滤渣Ⅰ的主要成分是___ (填化学式)。
(2)从分离出滤渣Ⅱ后的滤液中得到产品,应进行的操作是___ 、___ 、过滤、洗涤、干燥。
(3)还原时,试剂X若选用SO2,则该反应的离子方程式为___ 。
(4)绿矾(FeSO4·7H2O)若保存不当或长期放置,易与空气中的氧气反应,检验绿矾是否被氧化的方法是___ 。

请回答下列问题。
(1)滤渣Ⅰ的主要成分是
(2)从分离出滤渣Ⅱ后的滤液中得到产品,应进行的操作是
(3)还原时,试剂X若选用SO2,则该反应的离子方程式为
(4)绿矾(FeSO4·7H2O)若保存不当或长期放置,易与空气中的氧气反应,检验绿矾是否被氧化的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】化学实验小组从印刷电路板废液(含FeCl3、FeCl2、CuCl2)中回收铜并重新获得FeCl3∙6H2O晶体的流程如图:
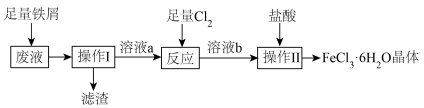
回答下列问题:
(1)检验腐蚀废液中含有Fe2+一种试剂是___________ 。
(2)有同学建议,使用H2O2和盐酸代替Cl2以减少污染,则反应离子方程式___________ 。
(3)甲同学用酸性KMnO4溶液检测溶液b中是否含有Fe2+。乙同学认为甲的方案不正确,理由是___________ (用离子方程式表示)。
(4)操作II有五步:___________ 、___________ 、___________ 、洗涤、干燥。加盐酸的目的是防止加热时溶液b与沸水的反应,写出要防止发生的反应的化学方程式___________ 。

回答下列问题:
(1)检验腐蚀废液中含有Fe2+一种试剂是
(2)有同学建议,使用H2O2和盐酸代替Cl2以减少污染,则反应离子方程式
(3)甲同学用酸性KMnO4溶液检测溶液b中是否含有Fe2+。乙同学认为甲的方案不正确,理由是
(4)操作II有五步:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某兴趣小组对化合物M(由2种元素组成)开展探究实验如图:
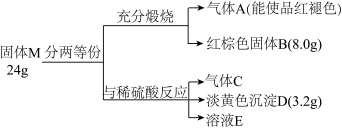
其中气体C在标况下的密度为1.518g/L,溶液E中滴加KSCN未出现明显现象。
请回答:
(1)固体M的组成元素是_____ (填元素符号);气体C的结构式是_____ 。
(2)固体M与稀硫酸反应的化学方程式为______ 。
(3)检验溶液E中的金属阳离子的方法是______ 。

其中气体C在标况下的密度为1.518g/L,溶液E中滴加KSCN未出现明显现象。
请回答:
(1)固体M的组成元素是
(2)固体M与稀硫酸反应的化学方程式为
(3)检验溶液E中的金属阳离子的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(一)某实验小组设计如下实验探究二价铁的还原性。
(1)实验I中白色沉淀变为红褐色,发生反应的化学方程式为_________ 。
(2)探究实验II中白色沉淀的组成。
①预测沉淀的组成。已知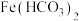 在水中不存在。
在水中不存在。
假设a:依据 溶液显
溶液显_________ 性,推测白色沉淀可能为
假设b:白色沉淀还可能为_________ (填化学式)。
②实验探究沉淀的组成。
I.取少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
II.向I所得溶液中滴入KSCN溶液,溶液几乎不变红。
III.向II溶液中再滴入少量 ,溶液立即变为红色。
,溶液立即变为红色。
由此可知,白色沉淀中一定含有的离子为_________ (填离子符号)。
(3)探究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比实验I中所得的
_________ (填“难”或“易”)于被空气氧化。
(4)若某溶液中只含有 而不含
而不含 ,可证明该事实的实验方法是_________(填序号)。
,可证明该事实的实验方法是_________(填序号)。
①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加 溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
④只滴加KSCN溶液不显红色
(二) 和
和 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
(5)与酸反应的差异。甲组进行了如下4组实验。

其中实验_________ 和_________ (填实验序号)可以鉴别 和
和 。
。
(6)稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。
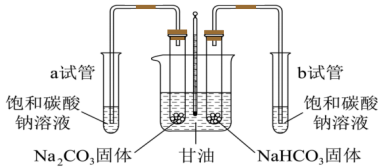
①将分别装有 和
和 的试管同时放入甘油浴加热(甘油沸点为290°C)。
的试管同时放入甘油浴加热(甘油沸点为290°C)。
②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为:_________ 、_________ 。
③试管b中发生反应的化学方程式为_________ 。
| 序号 | 实验方案 | 现象 |
| Ⅰ |  | 现象a:生成白色沉淀,3min后沉淀基本变为红色 |
| Ⅱ |  | 现象b:生成白色沉淀,3min后沉淀颜色几乎不变 |
(2)探究实验II中白色沉淀的组成。
①预测沉淀的组成。已知
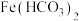 在水中不存在。
在水中不存在。假设a:依据
 溶液显
溶液显
假设b:白色沉淀还可能为
②实验探究沉淀的组成。
I.取少量白色沉淀,充分洗涤,向其中加入稀硫酸,沉淀完全溶解,产生无色气泡。
II.向I所得溶液中滴入KSCN溶液,溶液几乎不变红。
III.向II溶液中再滴入少量
 ,溶液立即变为红色。
,溶液立即变为红色。由此可知,白色沉淀中一定含有的离子为
(3)探究过程中发现白色沉淀在空气中久置,最终变为红褐色。则该沉淀比实验I中所得的

(4)若某溶液中只含有
 而不含
而不含 ,可证明该事实的实验方法是_________(填序号)。
,可证明该事实的实验方法是_________(填序号)。①先加氯水,后加KSCN溶液后显红色
②先加KSCN溶液,不显红色,再加氯水后显红色
③滴加
 溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色
溶液,只产生白色沉淀,迅速变为灰绿色,最后呈红褐色④只滴加KSCN溶液不显红色
| A.①② | B.②③ | C.③④ | D.①④ |
(二)
 和
和 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:(5)与酸反应的差异。甲组进行了如下4组实验。

其中实验
 和
和 。
。(6)稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。

①将分别装有
 和
和 的试管同时放入甘油浴加热(甘油沸点为290°C)。
的试管同时放入甘油浴加热(甘油沸点为290°C)。②该实验用饱和碳酸钠溶液检验反应的产物,a、b试管中的实验现象分别为:
③试管b中发生反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现有实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时反应:CO(g)+2H2(g) CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:

(1)上图中表示CH3OH的变化的曲线是___________________ 。
(2)用H2表示从0~2s内该反应的平均速率v(H2) =__________________ 。
(3)能说明该反应已达到平衡状态的是_________________ 。
a.v(CH3OH) =2v(H2) b.容器内压强保持不变
c.2v逆(CO) = v正(H2) d.容器内密度保持不变
(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:__________________ 。CH3OH与O2的反应可将化学能转化为电能,其工作原理如图所示,图中CH3OH从_______________ (填A或B)通入,b极的电极反应式是___________________ 。

 CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:
CH3OH(g) △H<0,体系中n(CO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(1)上图中表示CH3OH的变化的曲线是
(2)用H2表示从0~2s内该反应的平均速率v(H2) =
(3)能说明该反应已达到平衡状态的是
a.v(CH3OH) =2v(H2) b.容器内压强保持不变
c.2v逆(CO) = v正(H2) d.容器内密度保持不变
(4)已知常温常压下1g液态甲醇燃烧生成CO2气体和液态水放出22.68kJ的热量,则该反应的热化学方程式为:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】为减小和消除CO2对环境的影响,有科学家提出“绿色自由”构想。即先把空气吹人碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:

(1)写出分解池中反应的化学方程式 。
(2)在合成塔中,当有4.4kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(3)写出以氢氧化钾为电解质的甲醇燃料电池的负极反应式 。
当电子转移为 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)在体积为l L的密闭容器中,充人1mol CO2和3molH2在500°C下发生反应。有关物质的浓度随时间变化如下图所示。
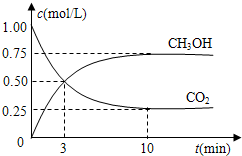
①从反应开始到平衡,H2的平均反应速率v(H2)= 。
②若其他条件不变,只将温度提高到800°C,再次达平衡时,n(CH3OH)/n(CO2)比值 (填“增大”、“减小”或“不变”)。

(1)写出分解池中反应的化学方程式 。
(2)在合成塔中,当有4.4kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(3)写出以氢氧化钾为电解质的甲醇燃料电池的负极反应式 。
当电子转移为 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)在体积为l L的密闭容器中,充人1mol CO2和3molH2在500°C下发生反应。有关物质的浓度随时间变化如下图所示。

①从反应开始到平衡,H2的平均反应速率v(H2)= 。
②若其他条件不变,只将温度提高到800°C,再次达平衡时,n(CH3OH)/n(CO2)比值 (填“增大”、“减小”或“不变”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】了解化石燃料燃烧过程中二氧化硫( )和氮氧化物(
)和氮氧化物( )的处理对改善环境推动可持续发展具有重要意义。结合所学知识,回答下列问题:
)的处理对改善环境推动可持续发展具有重要意义。结合所学知识,回答下列问题:
I.用活性炭吸附 。
。
(1)活性炭可以和 反应。一定条件下,当1mol NO与活性炭完全反应生成两种无毒的气体时,放出17kJ的热量,写出其反应的热化学方程式:
反应。一定条件下,当1mol NO与活性炭完全反应生成两种无毒的气体时,放出17kJ的热量,写出其反应的热化学方程式:______ 。
(2)活性炭吸附 反应如下:
反应如下:
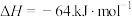 。
。
在 ℃时,该反应在2L容器中测得反应不同时间各物质的物质的量如下:
℃时,该反应在2L容器中测得反应不同时间各物质的物质的量如下:
0~10min内, 的平均反应速率
的平均反应速率
______ ,30min时,该反应的平衡常数
______ 。
(3)30min后,只改变某一条件,反应重新达到平衡;根据表中的数据判断改变的条件可能是______ (填字母)。
a.加入活性炭 b.通入
c.缩小容器的体积 d.加入合适的催化剂
II. 烟气脱除。
烟气脱除。
工业上可用纳米MgO分散到一定浓度的 溶液中,配制成
溶液中,配制成 烟气脱硫试剂。
烟气脱硫试剂。
将含有 的烟气以一定流速持续通入到该脱硫试剂中,实时监测出口处气体中
的烟气以一定流速持续通入到该脱硫试剂中,实时监测出口处气体中 脱除效率及脱硫试剂溶液的pH值,如图1所示。
脱除效率及脱硫试剂溶液的pH值,如图1所示。
已知:ⅰ.纳米MgO活性较高,常温下可以与水反应;
ⅱ. 在水中难溶,
在水中难溶, 可溶。
可溶。
(4)烟气脱硫开始阶段溶液呈碱性,很快pH值降到4左右,烟气脱硫效率始终很高。结合化学用语解释其原因______ 。
(5)脱硫试剂中Mg2+维持较高的初始浓度,对脱硫效率有显著影响。实验发现,在600s以后,随着 的脱除,溶液pH值几乎不变,但
的脱除,溶液pH值几乎不变,但 浓度逐渐升高,结合图2中含硫微粒的分布情况,用离子方程式解释其可能原因
浓度逐渐升高,结合图2中含硫微粒的分布情况,用离子方程式解释其可能原因______ 。 的浓度、
的浓度、______ (写出两条)。
 )和氮氧化物(
)和氮氧化物( )的处理对改善环境推动可持续发展具有重要意义。结合所学知识,回答下列问题:
)的处理对改善环境推动可持续发展具有重要意义。结合所学知识,回答下列问题:I.用活性炭吸附
 。
。(1)活性炭可以和
 反应。一定条件下,当1mol NO与活性炭完全反应生成两种无毒的气体时,放出17kJ的热量,写出其反应的热化学方程式:
反应。一定条件下,当1mol NO与活性炭完全反应生成两种无毒的气体时,放出17kJ的热量,写出其反应的热化学方程式:(2)活性炭吸附
 反应如下:
反应如下:
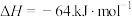 。
。在
 ℃时,该反应在2L容器中测得反应不同时间各物质的物质的量如下:
℃时,该反应在2L容器中测得反应不同时间各物质的物质的量如下:时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| 2 | 1.16 | 0.80 | 0.80 | 1.23 | 1.23 |
| 0 | 0.42 | 0.60 | 0.60 | 0.80 | 0.80 |
 的平均反应速率
的平均反应速率

(3)30min后,只改变某一条件,反应重新达到平衡;根据表中的数据判断改变的条件可能是
a.加入活性炭 b.通入

c.缩小容器的体积 d.加入合适的催化剂
II.
 烟气脱除。
烟气脱除。工业上可用纳米MgO分散到一定浓度的
 溶液中,配制成
溶液中,配制成 烟气脱硫试剂。
烟气脱硫试剂。将含有
 的烟气以一定流速持续通入到该脱硫试剂中,实时监测出口处气体中
的烟气以一定流速持续通入到该脱硫试剂中,实时监测出口处气体中 脱除效率及脱硫试剂溶液的pH值,如图1所示。
脱除效率及脱硫试剂溶液的pH值,如图1所示。
已知:ⅰ.纳米MgO活性较高,常温下可以与水反应;
ⅱ.
 在水中难溶,
在水中难溶, 可溶。
可溶。(4)烟气脱硫开始阶段溶液呈碱性,很快pH值降到4左右,烟气脱硫效率始终很高。结合化学用语解释其原因
(5)脱硫试剂中Mg2+维持较高的初始浓度,对脱硫效率有显著影响。实验发现,在600s以后,随着
 的脱除,溶液pH值几乎不变,但
的脱除,溶液pH值几乎不变,但 浓度逐渐升高,结合图2中含硫微粒的分布情况,用离子方程式解释其可能原因
浓度逐渐升高,结合图2中含硫微粒的分布情况,用离子方程式解释其可能原因
 的浓度、
的浓度、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】“消洗灵”是具有消毒、杀菌、漂白和洗涤等综合功效的固体粉末,消毒原理与“84消毒液”相似,化学组成可以表示为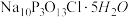 (磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
(磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
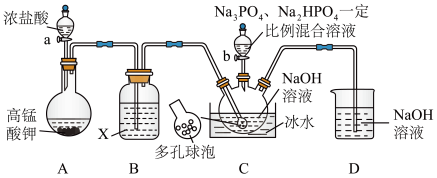
回答下列问题:
(1)仪器a的名称为___________ ,C中采用多孔球泡的目的是___________ 。
(2)磷酸是三元弱酸,常温下三级电离常数分别是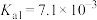 ,
, ,
,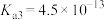 ,常温下同浓度
,常温下同浓度 、
、 的混合溶液pH
的混合溶液pH_______ (填“>”“<”或“=”)7。
(3)“消洗灵”消毒时对金属腐蚀性小,原因是在金属表面形成一种不溶性磷酸盐膜,对金属有良好的保护作用,在空气中对镁合金消毒,磷酸钠溶液使镁合金表面形成含有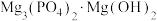 的保护层,写出反应的化学方程式:
的保护层,写出反应的化学方程式:___________ 。
(4)产品纯度测定(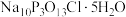 的摩尔质量为656.5
的摩尔质量为656.5  )。
)。
①取a g待测试样溶于蒸馏水配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2 稀硫酸、25 mL 0.1
稀硫酸、25 mL 0.1  碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;
③滴入3滴5%淀粉溶液,用0.05 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
已知: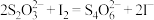 ,达到滴定终点的现象为
,达到滴定终点的现象为___________ ,产品的纯度为___________ (用含a的代数式表示)。若滴定前滴定管中含有气泡,滴定结束无气泡会造成纯度测定值___________ (填“偏大”“偏小”或“不变”)。
 (磷酸三钠次氯酸钠)。实验室制备装置和过程如图:
(磷酸三钠次氯酸钠)。实验室制备装置和过程如图: 
回答下列问题:
(1)仪器a的名称为
(2)磷酸是三元弱酸,常温下三级电离常数分别是
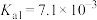 ,
, ,
,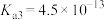 ,常温下同浓度
,常温下同浓度 、
、 的混合溶液pH
的混合溶液pH(3)“消洗灵”消毒时对金属腐蚀性小,原因是在金属表面形成一种不溶性磷酸盐膜,对金属有良好的保护作用,在空气中对镁合金消毒,磷酸钠溶液使镁合金表面形成含有
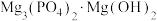 的保护层,写出反应的化学方程式:
的保护层,写出反应的化学方程式:(4)产品纯度测定(
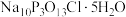 的摩尔质量为656.5
的摩尔质量为656.5  )。
)。①取a g待测试样溶于蒸馏水配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2
 稀硫酸、25 mL 0.1
稀硫酸、25 mL 0.1  碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;③滴入3滴5%淀粉溶液,用0.05
 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗20.00 mL。已知:
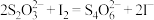 ,达到滴定终点的现象为
,达到滴定终点的现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01mol·L-1的X、Y、Z、W溶液的pH。
(1)X、W的化学式分别为_______ 、_______ 。
(2)W在溶液中的电离方程式为_______ 。
(3)25℃时,Z溶液的pH>7的原因是_______ (用离子方程式表示)。
(4)将X、Y、Z各1mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为_______ 。
(5)Z溶液与W溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为____ 。
| 0.01mol·L-1的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
(2)W在溶液中的电离方程式为
(3)25℃时,Z溶液的pH>7的原因是
(4)将X、Y、Z各1mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为
(5)Z溶液与W溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】甲烷是天然气的主要成分,是一种重要的清洁能源和化工原料。
(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知:C(s)+2H2(g) CH4 △H=-73kJ/mol
CH4 △H=-73kJ/mol
2CO(g) C(s)+CO2(g) △H=-171kJ/mol
C(s)+CO2(g) △H=-171kJ/mol
CO(g)+3H(g) CH4(g)+H2O(g) △H=-203kJ/mol。
CH4(g)+H2O(g) △H=-203kJ/mol。
写出CO与H2O(g)反应生成H2和CO2的热化学方程式_________________ 。
(2)天然气中含有H2S杂质,某科研小组用氨水吸收得到NH4HS溶液,已知T℃k(NH3·H2O)=1.74×10-5;k1(H2S)=1.07×10-7,k2(H2S)=1.74×10-13,NH4HS溶液中所含粒子浓度大小关系正确的是_______ 。
A. c(NH4+)>c(HS-)>c(OH-)>c(H+) B. c(HS-)>c(NH4+)>(S2-)>c(H+)
C. c(NH4+)>c(HS-)>c(H2S)>c(H+) D. c(HS-)>c(S2-)>c(H+)>c(OH-)
(3)工业上常用CH4与水蒸气在一定条件下来制取H2,其原理为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
①一定温度时,在一个体积为2L的恒容密闭容器中,加入lnmolCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为_________ 。此反应的平衡常数为_____ (结果保留到小数点后三位)。
②下列说法中能说明此反应达到平衡状态的是_________ 。
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.各组分的物质的量浓度不再改变
D.体系的密度不再发生变化
E.反应速率V(CH4):V(H2O)v(CO):v(H2)=1:1:1:3
(4)甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)==CO2(g)+3H2(g) △H=+49kJ/mol。某温度下,将[n(H2O):n(CH3OH)]=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为______ 。
(5)如图所示,直接甲醇燃料电池是质子交换膜燃料电池的一种变种,它直接使用甲醇而勿需预先重整。请写出电池工作时的负极反应式:__________________ 。

(1)用煤制天然气时会发生多个反应,通过多种途径生成CH4。
已知:C(s)+2H2(g)
 CH4 △H=-73kJ/mol
CH4 △H=-73kJ/mol2CO(g)
 C(s)+CO2(g) △H=-171kJ/mol
C(s)+CO2(g) △H=-171kJ/molCO(g)+3H(g)
 CH4(g)+H2O(g) △H=-203kJ/mol。
CH4(g)+H2O(g) △H=-203kJ/mol。写出CO与H2O(g)反应生成H2和CO2的热化学方程式
(2)天然气中含有H2S杂质,某科研小组用氨水吸收得到NH4HS溶液,已知T℃k(NH3·H2O)=1.74×10-5;k1(H2S)=1.07×10-7,k2(H2S)=1.74×10-13,NH4HS溶液中所含粒子浓度大小关系正确的是
A. c(NH4+)>c(HS-)>c(OH-)>c(H+) B. c(HS-)>c(NH4+)>(S2-)>c(H+)
C. c(NH4+)>c(HS-)>c(H2S)>c(H+) D. c(HS-)>c(S2-)>c(H+)>c(OH-)
(3)工业上常用CH4与水蒸气在一定条件下来制取H2,其原理为:CH4(g)+H2O(g)
 CO(g)+3H2(g)
CO(g)+3H2(g)①一定温度时,在一个体积为2L的恒容密闭容器中,加入lnmolCH4和1.4mol水蒸气发生上述反应,5min后达平衡,生成0.2molCO,用H2表示该反应的速率为
②下列说法中能说明此反应达到平衡状态的是
A.体系的压强不再发生变化
B.生成1molCH4的同时消耗3molH2
C.各组分的物质的量浓度不再改变
D.体系的密度不再发生变化
E.反应速率V(CH4):V(H2O)v(CO):v(H2)=1:1:1:3
(4)甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)==CO2(g)+3H2(g) △H=+49kJ/mol。某温度下,将[n(H2O):n(CH3OH)]=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为
(5)如图所示,直接甲醇燃料电池是质子交换膜燃料电池的一种变种,它直接使用甲醇而勿需预先重整。请写出电池工作时的负极反应式:

您最近一年使用:0次

 (mol)
(mol)

