下列有关说法正确的是
| A.1 mol FeBr2与足量氯气反应时,理论上转移的电子数约为3×6.02×1023 |
| B.常温下,pH均为3的三种溶液:①HCl溶液 ②H2SO4溶液③CH3COOH溶液,各自溶质的物质的量浓度大小顺序为①=②<③ |
| C.电解熔融NaCl或AlCl3制取Na或Al |
D.一定条件下反应 (aq)+H2O(l) (aq)+H2O(l) 2 2 (aq)+2H+(aq)达到平衡后,滴加少量浓硫酸,重新达平衡前,2v正( (aq)+2H+(aq)达到平衡后,滴加少量浓硫酸,重新达平衡前,2v正( )<v逆( )<v逆( ) ) |
更新时间:2016-04-29 12:25:46
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】下列有关实验现象的解释或所得结论正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某补血口服液中滴加几滴酸性 溶液 溶液 | 酸性 溶液紫色褪去 溶液紫色褪去 | 该补血口服液中一定含有 |
| B | 用蒸馏水溶解 固体,并继续加水稀释 固体,并继续加水稀释 | 溶液由绿色逐渐变为蓝色 | 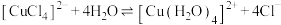 正向移动 正向移动 |
| C | 将25℃0.1mol/L的 溶液加热到40℃,用传感器监测溶液pH变化 溶液加热到40℃,用传感器监测溶液pH变化 | 溶液的pH逐渐减小 | 温度升高, 的水解增大程度小于水的电离增大程度,导致最终氢离子浓度升高 的水解增大程度小于水的电离增大程度,导致最终氢离子浓度升高 |
| D | 向 溶液中滴加几滴KSCN溶液,观察现象,再滴加氯水直至过量 溶液中滴加几滴KSCN溶液,观察现象,再滴加氯水直至过量 | 滴加KSCN溶液无色,加入氯水后溶液先变红,一段时间后红色消失 | 氯水具有氧化性和漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】工业制硫酸的一步重要反应为2SO2(g)+O2(g)⇌2SO3(g) ∆H<0。下列说法正确的是
| A.其他条件不变时,升高温度,平衡向逆反应方向移动 |
| B.其他条件不变时,增大c(O2),SO2的平衡转化率增大 |
| C.其他条件不变时,增大压强,该反应的平衡常数增大 |
| D.将2mol SO2和1mol O2混合,充分反应后得到2mol SO3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
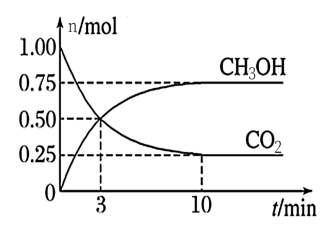
【推荐3】工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
 CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
| A.达到平衡时,H2的转化率为75% |
| B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态 |
| C.反应进行到10 min后,向容器中再充入CO2,则CO2的转化率会增大 |
| D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】由下列实验操作及现象推出的相应结论不正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将绿矾样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | 绿矾晶体已经变质 |
| B | 常温下,用pH试纸测定同浓度的NaCl和NaF溶液的pH,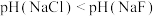 | 结合 能力: 能力: |
| C | 向 溶液中通入少量 溶液中通入少量 ,出现黑色沉淀 ,出现黑色沉淀 |  是强酸 是强酸 |
| D | 向 溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管中出现凝胶 溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管中出现凝胶 | 酸性:硅酸>盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 在0.1 mol•L-1Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深 | CO32-水解是吸热反应 |
| B | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性A比B强 |
| C | 常温下,用饱和Na2CO3溶液可将BaSO4部分转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| D | 室温下,用pH试纸测得:0.1 mol•L-1 Na2SO3溶液的pH约为10;0.1 mol•L-1 NaHSO3溶液的pH约为5 | HSO 结合H+的能力比SO32-的弱 结合H+的能力比SO32-的弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
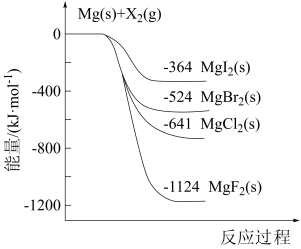
【推荐1】如图是金属镁和卤素单质( )反应的能量变化示意图。下列说法错误的是
)反应的能量变化示意图。下列说法错误的是
 )反应的能量变化示意图。下列说法错误的是
)反应的能量变化示意图。下列说法错误的是
A.工业上可通过电解熔融状态下的 制取金属Mg,Mg是阴极产物 制取金属Mg,Mg是阴极产物 |
B.标准状况条件下,11.2L (g)与足量的Mg充分反应,吸热562kJ (g)与足量的Mg充分反应,吸热562kJ |
C.热稳定性: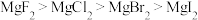 |
D.由图可知: 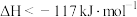 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
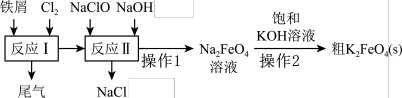
下列叙述不正确的是

下列叙述不正确的是
| A.反应I产生的尾气可通入澄清石灰水中吸收 |
| B.反应I生成的FeCl3,在碱性条件下会被NaClO氧化成Na2FeO4 |
| C.反应II中每消耗3个ClO-转移6个电子 |
| D.Na2FeO4转化成K2FeO4的反应是氧化还原反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用一种超薄LDH(层状双金属氢氧化物)纳米片光催化剂,实现了在常温常压和可见光或直接太阳辐射下, 和
和 合成氨的过程,其原理示意图如下图所示。下列说法中正确的是
合成氨的过程,其原理示意图如下图所示。下列说法中正确的是

 和
和 合成氨的过程,其原理示意图如下图所示。下列说法中正确的是
合成氨的过程,其原理示意图如下图所示。下列说法中正确的是
| A.在该合成氨反应条件下,每转移6个电子需要3个水分子参与反应 |
B.2分子 参加反应,反应后分子总数目减少1个 参加反应,反应后分子总数目减少1个 |
| C.LDH是反应的催化剂,并不参与反应 |
D.反应中氧化产物与还原产物的分子数目之比为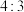 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】利用空气催化氧化法除掉电石渣浆(含CaO)上清液中的S2-,制取石膏(CaSO4·2H2O)的过程如图所示,下列说法错误的是
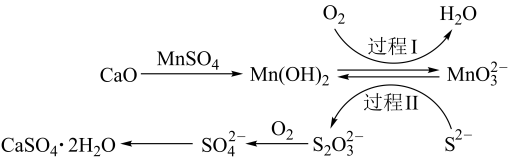

| A.CaSO4·2H2O属于盐类和混合物 |
B.过程Ⅱ中,反应的离子方程式为:4MnO +2S2-+9H2O=S2O +2S2-+9H2O=S2O +4Mn(OH)2↓+10OH- +4Mn(OH)2↓+10OH- |
| C.过程Ⅰ后溶液pH增大 |
D.将10 L上清液中的S2-(S2-浓度为480 mg·L-1)转化为SO ,理论上共需要0.3 mol O2 ,理论上共需要0.3 mol O2 |
您最近一年使用:0次



