对于平衡体系mA(g)+nB(g)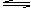 pC(g)+qD(g);ΔH<0。下列结论中正确的是( )
pC(g)+qD(g);ΔH<0。下列结论中正确的是( )
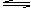 pC(g)+qD(g);ΔH<0。下列结论中正确的是( )
pC(g)+qD(g);ΔH<0。下列结论中正确的是( )| A.若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48 倍,则m+n>p+q |
| B.若平衡时,A、B的转化率相等,说明反应开始A、B的物质的量之比为m∶n |
| C.若温度.体积不变,当m+n<p+q时,向平衡体系中再加入少量气体E(E与所有组分均不反应),A的转化率减小 |
| D.若升高温度,则反应中逆反应速率减小,正反应速率增大 |
10-11高三上·河北唐山·期中 查看更多[1]
(已下线)2010年河北省唐山一中高三上学期期中考试化学卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】对某一可逆反应来说,其他条件不变时,使用催化剂( )
①可以提高反应物的平衡转化率
②可以同等程度改变正逆反应的速率
③增大正反应速率,减小逆反应速率
④不能改变平衡混合物的组成
⑤不能使化学平衡发生移动
⑥改变反应的ΔH
①可以提高反应物的平衡转化率
②可以同等程度改变正逆反应的速率
③增大正反应速率,减小逆反应速率
④不能改变平衡混合物的组成
⑤不能使化学平衡发生移动
⑥改变反应的ΔH
| A.①②⑤ | B.①③⑤⑥ | C.②④⑥ | D.②④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列事实中,能用勒夏特列原理解释的是
| A.用牺牲阳极的阴极保护法保护船舶的外壳 |
| B.压缩氢气与碘蒸气的平衡混合体系,气体颜色变深 |
| C.夏天打开冰镇啤酒,把啤酒倒入玻璃杯中,杯中立即泛起大量泡沫 |
D.500℃左右比常温下更有利于 和 和 反应生成 反应生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】对已达化学平衡的下列反应 2X(g)+Y(s) 2Z(g)增大压强时,对反应产生的影响是
2Z(g)增大压强时,对反应产生的影响是
 2Z(g)增大压强时,对反应产生的影响是
2Z(g)增大压强时,对反应产生的影响是| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都增大,平衡不发生移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在密闭容器,一定条件下进行反应:mA(g)+nB(g)⇌pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,变化过程均如图所示,则对该反应叙述正确的是
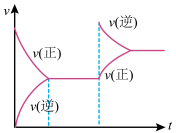

| A.m+n<p+q | B.逆反应是放热反应 |
| C.m+n>p+q | D.正反应是吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
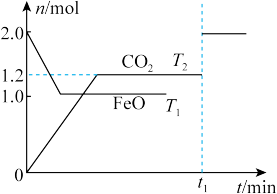
【推荐1】羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害。在一定条件下,将CO与H2S以体积比1:2置于某刚性密闭容器中发生下列反应:CO(g)+H2S(g)⇌COS(g)+H2(g)。下列说法正确的是
| A.升高温度,H2S的浓度增大,表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大,逆反应速率不变 |
| C.COS与H2的体积比保持不变时,说明反应达到平衡状态 |
| D.向反应器中再通入CO,能使H2S的转化率增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列有关说法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.化学反应过程中吸热或放热越多,则温度变化对速率的影响越明显 |
| C.使用高效催化剂,可大大提高原料平衡转化率的有效方法 |
| D.升高温度能增大单位体积内的活化分子百分数,加快反应速率 |
您最近一年使用:0次

 PCl3
PCl3

