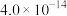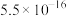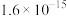化学在解决雾霾污染中有着重要的作用,雾霾由多种污染物形成,其中包含颗粒物PM2.5)、
氮氧化物(NOx)、CO、SO2等.
(1)已知:NO(g)+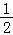 O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)△H=_________ kJ•mol﹣1.
一定条件下,将NO2与SO2以物质的量比1:2置于恒温恒容的密闭容器中发生上述反应,
下列能说明反应达到平衡状态的有____________
a.混合气体的平均相对分子质量
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2物质的量比为1:3,则平衡常数K=________ (用分数表示)
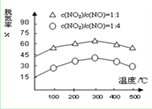
NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请解释300℃之后脱氮率逐渐减小的原因:__________________________
(2)CO综合利用.
①CO用于合成甲醇反应方程式为:CO(g)+2H2(g)═CH3OH(g)
若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如图所示.得知该反应的△H_________ 0,该反应的实际生产条件控制在 250 ℃、1.3×104kPa左右最为适宜.反应达平衡后,下列操作既能加快反应速率,又能使平衡混合物中CH3OH物质的量分数增大的是____________
a. 升温 b.恒容条件下充入H2
c.加入合适的正催化剂 d.恒容条件下再充入1molCO,2mol H2
e.压缩体积 f.移走一部分CH3OH
②电解CO制备CH4,电解质为碳酸钠溶液,工作原理如图2所示,写出阴极区电极
反应式_______________
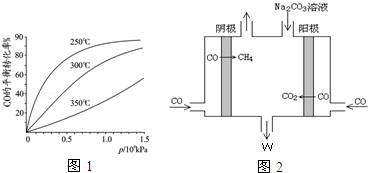
(3)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,具体步骤如下:
SO2(g)+H2O(l) H2SO3(l)
H2SO3(l)  H+(aq)+HSO
H+(aq)+HSO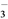 (aq) Ⅰ
(aq) Ⅰ
HSO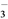 (aq)
(aq)  H+(aq)+SO
H+(aq)+SO (aq) Ⅱ
(aq) Ⅱ
Ca(OH)2(s) Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+SO (aq)
(aq)  CaSO3(s) Ⅳ
CaSO3(s) Ⅳ
该温度下,测定吸收后液体中c(Ca2+)一直保持为0.70 mol/L,已知Ksp(CaSO3)=1.4×10-7,则吸收后溶液中的SO 的浓度为
的浓度为_________________
氮氧化物(NOx)、CO、SO2等.
(1)已知:NO(g)+
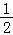 O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣12SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)△H=
一定条件下,将NO2与SO2以物质的量比1:2置于恒温恒容的密闭容器中发生上述反应,
下列能说明反应达到平衡状态的有
a.混合气体的平均相对分子质量
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2物质的量比为1:3,则平衡常数K=
NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请解释300℃之后脱氮率逐渐减小的原因:

(2)CO综合利用.
①CO用于合成甲醇反应方程式为:CO(g)+2H2(g)═CH3OH(g)
若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如图所示.得知该反应的△H
a. 升温 b.恒容条件下充入H2
c.加入合适的正催化剂 d.恒容条件下再充入1molCO,2mol H2
e.压缩体积 f.移走一部分CH3OH
②电解CO制备CH4,电解质为碳酸钠溶液,工作原理如图2所示,写出阴极区电极
反应式

(3)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,具体步骤如下:
SO2(g)+H2O(l)
 H2SO3(l)
H2SO3(l)  H+(aq)+HSO
H+(aq)+HSO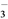 (aq) Ⅰ
(aq) ⅠHSO
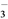 (aq)
(aq)  H+(aq)+SO
H+(aq)+SO (aq) Ⅱ
(aq) ⅡCa(OH)2(s)
 Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+2OH-(aq) ⅢCa2+(aq)+SO
 (aq)
(aq)  CaSO3(s) Ⅳ
CaSO3(s) Ⅳ该温度下,测定吸收后液体中c(Ca2+)一直保持为0.70 mol/L,已知Ksp(CaSO3)=1.4×10-7,则吸收后溶液中的SO
 的浓度为
的浓度为
更新时间:2017-03-04 06:10:56
|
相似题推荐
【推荐1】氢能是一种极具发展潜力的清洁能源。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为___________________________________ ;该反应自发进行的条件是___________ 。
(2)Bodensteins研究了如下反应:2HI(g) H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:___________ 。
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=__________ min-1(保留三位有效数字)
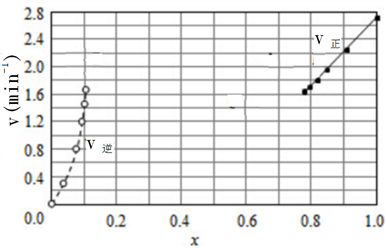
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。______________
(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________ 。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为
(2)Bodensteins研究了如下反应:2HI(g)
 H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| X(HI) | 1.00 | 0.910 | 0.850 | 0.815 | 0.795 | 0.784 |
| X(HI) | 0.00 | 0.600 | 0.730 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。

(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】合成氨工业对国民经济和社会发展具有重要意义
(1)工业合成氨工业常用的催化剂是____________ ,氨分子的电子式是__________
(2)图是一定的温度和压强下是N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式_______ 。(热量Q的数值用含字母a、b的代数式表示)

(3)下列有关该反应的说法正确的是_____ (填序号)
A.保持容器的体积不变,当混合气体的密度不变时,说明反应已经达到平衡状态。
B.达到平衡时若升高温度,混合气体中氮元素的质量分数将变大。
C.达到平衡时若减少容器的体积,正反应速率将大于逆反应速率。
D.达到平衡后,N2的转化率和H2的转化率一定相等。
(4)在催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出反应的化学方程式:_____________________ ;该反应中氧化产物与还原产物的物质的量之比是___________
(5)把NH3通入盐酸溶液中,所得溶液的pH=7, 此时溶液中离子浓度关系是__________ ; ______
(1)工业合成氨工业常用的催化剂是
(2)图是一定的温度和压强下是N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式

(3)下列有关该反应的说法正确的是
A.保持容器的体积不变,当混合气体的密度不变时,说明反应已经达到平衡状态。
B.达到平衡时若升高温度,混合气体中氮元素的质量分数将变大。
C.达到平衡时若减少容器的体积,正反应速率将大于逆反应速率。
D.达到平衡后,N2的转化率和H2的转化率一定相等。
(4)在催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出反应的化学方程式:
(5)把NH3通入盐酸溶液中,所得溶液的pH=7, 此时溶液中离子浓度关系是
您最近一年使用:0次
【推荐3】硫酸在生活和生产中应用广泛。
Ⅰ 某工厂以黄铁矿(主要成分为FeS2)为原料,采用“接触法”制备硫酸。
已知298 K和101 kPa条件下:
2FeS2(s)=2FeS(s)+S(s) ΔH1
S(s)+2O2(g)=2SO2(g) ΔH2
4FeS(s)+7O2(g)=2Fe2O3(s)+4SO2(g) ΔH3
则在该条件下FeS2与O2生成Fe2O3和SO2的总热化学方程式是________ 。
Ⅱ 催化氧化反应:2SO2(g)+O2(g)2SO3(g) ΔH<0
(1) 在体积可变的密闭容器,维持压强为1×105 Pa和初始n(SO2)=2 mol,充入一定量的O2,SO2平衡转化率α(SO2)随O2物质的量n(O2)的变化关系如图所示:
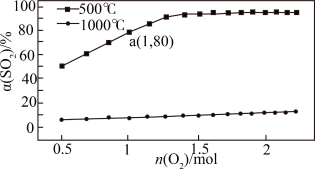
①在1000℃时,SO2平衡转化率随着O2物质的量的增大缓慢升高,解释其原因________ 。
②a点时SO3的平衡分压p(SO3)=________ Pa(保留2位有效数字,某组分的平衡分压=总压×某组分的物质的量分数)。
(2)保持温度不变,向固定体积的密闭容器中充入一定量的SO2、O2。请画出平衡体系中SO3的体积分数φ(SO3)随初始SO2、O2的物质的量之比[n(SO2)/n(O2)]的变化趋势图。

(3)已知活化氧可以把SO2快速氧化为SO3。根据计算机模拟结果,在炭黑表面上O2转化为活化氧的反应历程与能量变化如图所示。下列说法正确的是________ 。

A O2转化为活化氧是氧氧键的断裂与碳氧键的生成过程
B 该过程中最大能垒(活化能)E正=0.73 eV
C 每活化一个O2吸收0.29 eV的能量
D 炭黑可作为SO2转化为SO3的催化剂
E 其它条件相同时,炭黑颗粒越小,反应速率越快
Ⅲ 硫酸工厂尾气中的SO2可被NaOH溶液吸收,用惰性电极将所得的Na2SO3溶液进行电解,可循环再生NaOH的同时得到H2SO4,写出阳极的电极方程式________ 。
Ⅰ 某工厂以黄铁矿(主要成分为FeS2)为原料,采用“接触法”制备硫酸。
已知298 K和101 kPa条件下:
2FeS2(s)=2FeS(s)+S(s) ΔH1
S(s)+2O2(g)=2SO2(g) ΔH2
4FeS(s)+7O2(g)=2Fe2O3(s)+4SO2(g) ΔH3
则在该条件下FeS2与O2生成Fe2O3和SO2的总热化学方程式是
Ⅱ 催化氧化反应:2SO2(g)+O2(g)2SO3(g) ΔH<0
(1) 在体积可变的密闭容器,维持压强为1×105 Pa和初始n(SO2)=2 mol,充入一定量的O2,SO2平衡转化率α(SO2)随O2物质的量n(O2)的变化关系如图所示:

①在1000℃时,SO2平衡转化率随着O2物质的量的增大缓慢升高,解释其原因
②a点时SO3的平衡分压p(SO3)=
(2)保持温度不变,向固定体积的密闭容器中充入一定量的SO2、O2。请画出平衡体系中SO3的体积分数φ(SO3)随初始SO2、O2的物质的量之比[n(SO2)/n(O2)]的变化趋势图。

(3)已知活化氧可以把SO2快速氧化为SO3。根据计算机模拟结果,在炭黑表面上O2转化为活化氧的反应历程与能量变化如图所示。下列说法正确的是

A O2转化为活化氧是氧氧键的断裂与碳氧键的生成过程
B 该过程中最大能垒(活化能)E正=0.73 eV
C 每活化一个O2吸收0.29 eV的能量
D 炭黑可作为SO2转化为SO3的催化剂
E 其它条件相同时,炭黑颗粒越小,反应速率越快
Ⅲ 硫酸工厂尾气中的SO2可被NaOH溶液吸收,用惰性电极将所得的Na2SO3溶液进行电解,可循环再生NaOH的同时得到H2SO4,写出阳极的电极方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】我国力争在2030年前实现“碳达峰”,2060年前实现“碳中和”。目前,化石燃料仍是我国生产生活中重要的能量来源。因此, 的循环再利用是减少碳排放的重要研究课题。
的循环再利用是减少碳排放的重要研究课题。
(1)化工生产中常将 转化为有机物以实现碳循环。利用催化剂对
转化为有机物以实现碳循环。利用催化剂对 催化加氢转化成甲醇的化学方程式如下:
催化加氢转化成甲醇的化学方程式如下: 。一定温度下,向
。一定温度下,向 恒容密闭容器中按
恒容密闭容器中按 的物质的量之比充入
的物质的量之比充入 和
和 ,测得
,测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
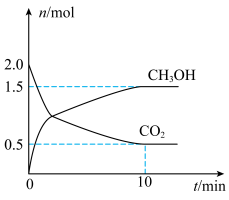
① 内,用
内,用 表示的化学反应速率
表示的化学反应速率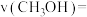
_______ 。
②下列现象能说明上述反应达到化学平衡状态的是_______ 。
a.反应体系中 b.混合气体的压强不再改变
b.混合气体的压强不再改变
c. d.混合气体的密度不再改变
d.混合气体的密度不再改变
e.单位时间内消耗 的同时消耗
的同时消耗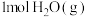
(2)有科学家提出用电化学方法将 转化为CO,从而实现
转化为CO,从而实现 再利用,其转化的基本原理如图所示。
再利用,其转化的基本原理如图所示。
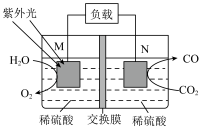
(已知:在同一电池中,正极的电极电势高于负极)
①电极电势较高的一极是_______ (填“M”或“N”)。
②写出M极的电极反应式:_______ 。
(3)二氧化碳甲烷化是 循环再利用最有效的技术之一,其反应为:
循环再利用最有效的技术之一,其反应为: 。
。
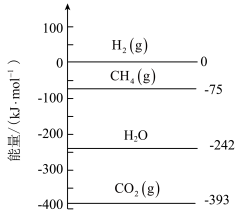
① 时,已知相关物质的相对能量如图所示,则
时,已知相关物质的相对能量如图所示,则 和
和 完全反应生成
完全反应生成 和
和
_______ (填“吸收”或“释放”)的能量为_______ kJ。
② 甲烷化过程中会发生副反应
甲烷化过程中会发生副反应 ,由于该反应的存在导致
,由于该反应的存在导致 不能100%转化为
不能100%转化为 ,生成的
,生成的 须依据
须依据 的选择性公式进行计算。某温度下,在体积为
的选择性公式进行计算。某温度下,在体积为 的恒容密闭容器中加入
的恒容密闭容器中加入 和
和 ,
, 后达到平衡,测得CO的平均化学反应速率为
后达到平衡,测得CO的平均化学反应速率为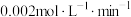 。已知上述反应条件下
。已知上述反应条件下 的选择性为95%,则
的选择性为95%,则 的平衡转化率为
的平衡转化率为_______ 。
(注: 的选择性=
的选择性=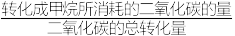 ×100%)
×100%)
 的循环再利用是减少碳排放的重要研究课题。
的循环再利用是减少碳排放的重要研究课题。(1)化工生产中常将
 转化为有机物以实现碳循环。利用催化剂对
转化为有机物以实现碳循环。利用催化剂对 催化加氢转化成甲醇的化学方程式如下:
催化加氢转化成甲醇的化学方程式如下: 。一定温度下,向
。一定温度下,向 恒容密闭容器中按
恒容密闭容器中按 的物质的量之比充入
的物质的量之比充入 和
和 ,测得
,测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
①
 内,用
内,用 表示的化学反应速率
表示的化学反应速率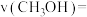
②下列现象能说明上述反应达到化学平衡状态的是
a.反应体系中
 b.混合气体的压强不再改变
b.混合气体的压强不再改变c.
 d.混合气体的密度不再改变
d.混合气体的密度不再改变e.单位时间内消耗
 的同时消耗
的同时消耗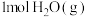
(2)有科学家提出用电化学方法将
 转化为CO,从而实现
转化为CO,从而实现 再利用,其转化的基本原理如图所示。
再利用,其转化的基本原理如图所示。
(已知:在同一电池中,正极的电极电势高于负极)
①电极电势较高的一极是
②写出M极的电极反应式:
(3)二氧化碳甲烷化是
 循环再利用最有效的技术之一,其反应为:
循环再利用最有效的技术之一,其反应为: 。
。①
 时,已知相关物质的相对能量如图所示,则
时,已知相关物质的相对能量如图所示,则 和
和 完全反应生成
完全反应生成 和
和

②
 甲烷化过程中会发生副反应
甲烷化过程中会发生副反应 ,由于该反应的存在导致
,由于该反应的存在导致 不能100%转化为
不能100%转化为 ,生成的
,生成的 须依据
须依据 的选择性公式进行计算。某温度下,在体积为
的选择性公式进行计算。某温度下,在体积为 的恒容密闭容器中加入
的恒容密闭容器中加入 和
和 ,
, 后达到平衡,测得CO的平均化学反应速率为
后达到平衡,测得CO的平均化学反应速率为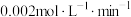 。已知上述反应条件下
。已知上述反应条件下 的选择性为95%,则
的选择性为95%,则 的平衡转化率为
的平衡转化率为(注:
 的选择性=
的选择性=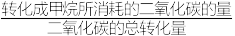 ×100%)
×100%)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】Ⅰ.为了实现“碳达峰和碳中和”目标,科学家利用C3N4/Cu催化剂(CuNPs)加氢还原CO2制备烃类和烃类含氧衍生物,实现太阳能综合利用。如图所示:
(1)上述装置中能量转化形式主要是________
太阳能→___________能→___________能。
(2)图中采用___________ (填“质子”或“阴离子”)交换膜。
(3)下列措施不利于绿色低碳发展的是___________。
Ⅱ.CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
(4)写出该反应的平衡常数表达式K=___________ 。
(5)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。 =
=___________ kJ/mol。第①步反应的热化学方程式为___________ 。
(6)一定温度下,在一体积固定的密闭容器中投入一定量的CO2和H2进行上述总反应,达到平衡后,改变下列1个条件,反应速率和CO2平衡转化率都增大的是___________。
(7)下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO2,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
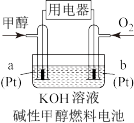
Ⅲ.该反应的产物甲醇燃烧电池具有很多优点。
(8)在碱性甲醇燃料电池中,Pt(a)发生___________ (填“氧化”或“还原”)反应:在酸性甲醇燃料电池中,电极b上发生的电极反应式为___________ 。

(1)上述装置中能量转化形式主要是
太阳能→___________能→___________能。
(2)图中采用
(3)下列措施不利于绿色低碳发展的是___________。
| A.使用氢能源车 | B.杭州西站光伏发电 |
| C.使用脱硫煤发电 | D.使用可循环快递箱 |
Ⅱ.CO2催化加氢制甲醇(CH3OH)是实现碳达峰、碳中和的途径之一,其反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 
(4)写出该反应的平衡常数表达式K=
(5)该反应分两步进行,反应过程能量变化如图所示,所有物质均为气态。
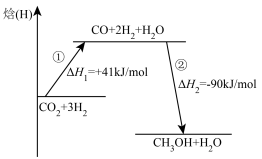
 =
=(6)一定温度下,在一体积固定的密闭容器中投入一定量的CO2和H2进行上述总反应,达到平衡后,改变下列1个条件,反应速率和CO2平衡转化率都增大的是___________。
| A.加入高效催化剂 | B.增大CO2浓度 | C.缩小容器容积 | D.升高温度 |
(7)下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO2,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
Ⅲ.该反应的产物甲醇燃烧电池具有很多优点。
(8)在碱性甲醇燃料电池中,Pt(a)发生

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】合成氨是人工固氮的一种主要途径。
(1)采用高质子导电性SCY陶瓷(能传递 )实现氮的固定即电解法合成氨,大大提高了氮气和氢气的转化率。总反应式为
)实现氮的固定即电解法合成氨,大大提高了氮气和氢气的转化率。总反应式为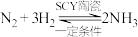 。在电解法合成氨的过程中,应将
。在电解法合成氨的过程中,应将 不断地通入
不断地通入___________ 极(填“阴”或“阳”),该电极的反应式为___________ 。
(2)通常条件下 与水蒸气几乎不发生反应,但在掺有少量氧化铁的二氧化钛催化剂表面,
与水蒸气几乎不发生反应,但在掺有少量氧化铁的二氧化钛催化剂表面, 能与水发生反应生成
能与水发生反应生成 ,反应方程式为
,反应方程式为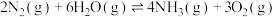 ,这里加快反应速率的因素是
,这里加快反应速率的因素是___________ 。等体积的 和
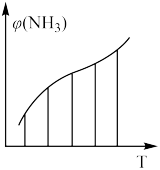
和 的混合气体(物质的量之比均为1∶3),分别加入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,经过相同时间后,测得氨气平衡时的体积分数
的混合气体(物质的量之比均为1∶3),分别加入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,经过相同时间后,测得氨气平衡时的体积分数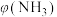 与反应温度T的关系曲线如图所示,则上述反应的
与反应温度T的关系曲线如图所示,则上述反应的
___________ 0(填“>”、“<”或“=”)。
(3)哈伯和博施用锇催化剂在 Pa、550°C的条件下工业化合成氨。在2L恒容密闭容器中充入0.1 mol
Pa、550°C的条件下工业化合成氨。在2L恒容密闭容器中充入0.1 mol  和0.3 mol
和0.3 mol  发生反应:
发生反应: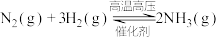
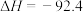 kJ⋅mol
kJ⋅mol 。
。
①下图所示的a、b、c、d四条曲线中,能表示该反应体系能量变化的是___________ (填字母代号)。
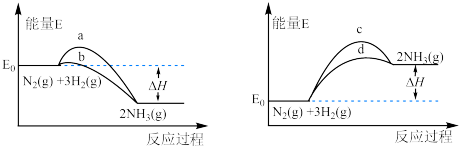
②经过10 min后达到平衡状态,测得体系内 mol,则10 min内的化学反应速率
mol,则10 min内的化学反应速率
___________ ,能证明反应已经达到平衡状态的是___________ 。
A.容器内气体压强保持不变。
B.单位时间减少0.1 mol 的同时增加了0.2 mol
的同时增加了0.2 mol  。
。
C.混合气体的平均相对分子质量保持不变
D.
③若此时再向容器中加入 和
和 各0.075 mol,平衡向
各0.075 mol,平衡向___________ 移动(填“正反应方向”或“逆反应方向”或“不”)。
(1)采用高质子导电性SCY陶瓷(能传递
 )实现氮的固定即电解法合成氨,大大提高了氮气和氢气的转化率。总反应式为
)实现氮的固定即电解法合成氨,大大提高了氮气和氢气的转化率。总反应式为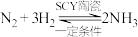 。在电解法合成氨的过程中,应将
。在电解法合成氨的过程中,应将 不断地通入
不断地通入(2)通常条件下
 与水蒸气几乎不发生反应,但在掺有少量氧化铁的二氧化钛催化剂表面,
与水蒸气几乎不发生反应,但在掺有少量氧化铁的二氧化钛催化剂表面, 能与水发生反应生成
能与水发生反应生成 ,反应方程式为
,反应方程式为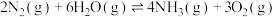 ,这里加快反应速率的因素是
,这里加快反应速率的因素是 和
和 的混合气体(物质的量之比均为1∶3),分别加入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,经过相同时间后,测得氨气平衡时的体积分数
的混合气体(物质的量之比均为1∶3),分别加入体积相同的恒容密闭容器中,在温度不相同的情况下发生反应,经过相同时间后,测得氨气平衡时的体积分数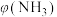 与反应温度T的关系曲线如图所示,则上述反应的
与反应温度T的关系曲线如图所示,则上述反应的

(3)哈伯和博施用锇催化剂在
 Pa、550°C的条件下工业化合成氨。在2L恒容密闭容器中充入0.1 mol
Pa、550°C的条件下工业化合成氨。在2L恒容密闭容器中充入0.1 mol  和0.3 mol
和0.3 mol  发生反应:
发生反应: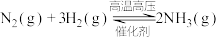
 kJ⋅mol
kJ⋅mol 。
。①下图所示的a、b、c、d四条曲线中,能表示该反应体系能量变化的是

②经过10 min后达到平衡状态,测得体系内
 mol,则10 min内的化学反应速率
mol,则10 min内的化学反应速率
A.容器内气体压强保持不变。
B.单位时间减少0.1 mol
 的同时增加了0.2 mol
的同时增加了0.2 mol  。
。C.混合气体的平均相对分子质量保持不变
D.

③若此时再向容器中加入
 和
和 各0.075 mol,平衡向
各0.075 mol,平衡向
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】钼酸铵[ (NH4)2MoO4]为白色晶体,具有很高的水溶性,不溶于乙醇,在地质勘探、石油冶炼等工业生产方面有着广泛的应用。以辉钼矿(主要成分为MoS2,还含有少量CuFeS2等杂质)为原料制备钼酸铵的工艺如下。回答下列问题:
I.火法工艺:
在空气中煅烧辉钼矿可得到MoO3,然后经过一系列处理制得钼酸铵。
(1)写出MoS2在空气中煅烧的化学方程式_______ 。
(2)该工艺最大的缺陷是_______ 。
II.湿法工艺:

已知:①滤液中的主要成分是 、
、  ;②
;② 易溶于有机溶剂。
易溶于有机溶剂。
③25 °C时相关物质的Ksp如下表所示:
(3)滤渣的主要成分是Cu(OH)2和Fe(OH)3,则加入NaClO碱性溶液反应后得到的浸取液的pH最小值为_______ 。( 当溶液中某离子浓度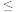 1×10-5mol·L-1时,可认为该离子沉淀完全。)
1×10-5mol·L-1时,可认为该离子沉淀完全。)
(4)写出MoS2和NaClO反应的离子方程式_______ 。
(5)萃取和反萃取的目的是_______ 。
(6)写出加入氨水反萃取过程中的离子方程式_______ 。
(7)(NH4)2MoO4溶液经过降温结晶、过滤、洗涤等操作得到(NH4)2MoO4晶体,洗涤时所选用的洗涤试剂为_______ 。
(8)钼酸铅(PbMoO4)难溶于水,常用作钼的质量鉴定。称取钼酸铵产品10.0 g,配成100mL溶液,量取10.00mL所配溶液于锥形瓶中,滴加1.000mol·L-1的Pb(NO3)2溶液,恰好完全反应时消耗Pb(NO3)2溶液4.50mL,计算钼酸铵产品中含有Mo元素的质量分数为_______ 。
I.火法工艺:
在空气中煅烧辉钼矿可得到MoO3,然后经过一系列处理制得钼酸铵。
(1)写出MoS2在空气中煅烧的化学方程式
(2)该工艺最大的缺陷是
II.湿法工艺:

已知:①滤液中的主要成分是
 、
、  ;②
;② 易溶于有机溶剂。
易溶于有机溶剂。③25 °C时相关物质的Ksp如下表所示:
| 物质 | Cu(OH)2 | Fe(OH)3 |
| Ksp | 1×10-19.6 | 1×10-38.6 |
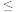 1×10-5mol·L-1时,可认为该离子沉淀完全。)
1×10-5mol·L-1时,可认为该离子沉淀完全。)(4)写出MoS2和NaClO反应的离子方程式
(5)萃取和反萃取的目的是
(6)写出加入氨水反萃取过程中的离子方程式
(7)(NH4)2MoO4溶液经过降温结晶、过滤、洗涤等操作得到(NH4)2MoO4晶体,洗涤时所选用的洗涤试剂为
(8)钼酸铅(PbMoO4)难溶于水,常用作钼的质量鉴定。称取钼酸铵产品10.0 g,配成100mL溶液,量取10.00mL所配溶液于锥形瓶中,滴加1.000mol·L-1的Pb(NO3)2溶液,恰好完全反应时消耗Pb(NO3)2溶液4.50mL,计算钼酸铵产品中含有Mo元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某三元锂电池放电时,正极材料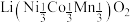 部分变为
部分变为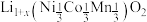 。从废旧三元锂电池正极材料(还含少量Al、Fe等杂质)中回收锂、钴、镍的工艺流程如下:
。从废旧三元锂电池正极材料(还含少量Al、Fe等杂质)中回收锂、钴、镍的工艺流程如下:

回答下列问题:
(1)“酸浸”时,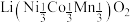 氧化
氧化 的离子方程式为
的离子方程式为__________________ 。
(2)25℃时,几种难溶电解质的溶度积如下:
该“浸出液”中金属离子的起始浓度范围均在0.001~0.01mol/L之间,“除杂”时所得“滤渣”中可能含有的物质有____________ (填化学式)。
(3)“萃取1”是将____________ (填离子符号)萃取入“有机相1”中而除去。“萃取2”时, 、
、 的萃取率与水相pH的关系如图所示。“萃取2”时水相pH控制的最佳范围为
的萃取率与水相pH的关系如图所示。“萃取2”时水相pH控制的最佳范围为____________ (填标号)。

A.4.0~4.5 B.4.5~5.0 C.5.0~5.5 D.5.5~6.0
(4)“沉锂”时,锂的沉淀率越大,最终溶液的pH越小,其原因是________________________ (请结合离子方程式解释原因)。
(5)镍与铁性质相似,均易与一氧化碳作用形成羰基配合物,中心原子价电子数与配位体提供的成键电子数遵循 规则。如:
规则。如: ,则镍与CO形成的配合物化学式为
,则镍与CO形成的配合物化学式为______ ,该镍与CO形成的配合物中 键和
键和 键数目之比为
键数目之比为______ 。
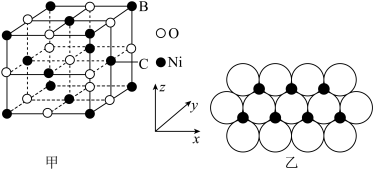
(6)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为______ 。一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为a pm,设阿伏加德罗常数值为
的半径为a pm,设阿伏加德罗常数值为 ,每平方米面积上具有该晶体的质量为
,每平方米面积上具有该晶体的质量为______ g(用含a、 的代数式表示)。
的代数式表示)。
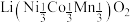 部分变为
部分变为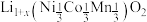 。从废旧三元锂电池正极材料(还含少量Al、Fe等杂质)中回收锂、钴、镍的工艺流程如下:
。从废旧三元锂电池正极材料(还含少量Al、Fe等杂质)中回收锂、钴、镍的工艺流程如下:
回答下列问题:
(1)“酸浸”时,
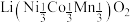 氧化
氧化 的离子方程式为
的离子方程式为(2)25℃时,几种难溶电解质的溶度积如下:
化学式 |
|
|
|
|
|
溶度积 |
|
|
|
|
|
该“浸出液”中金属离子的起始浓度范围均在0.001~0.01mol/L之间,“除杂”时所得“滤渣”中可能含有的物质有
(3)“萃取1”是将
 、
、 的萃取率与水相pH的关系如图所示。“萃取2”时水相pH控制的最佳范围为
的萃取率与水相pH的关系如图所示。“萃取2”时水相pH控制的最佳范围为
A.4.0~4.5 B.4.5~5.0 C.5.0~5.5 D.5.5~6.0
(4)“沉锂”时,锂的沉淀率越大,最终溶液的pH越小,其原因是
(5)镍与铁性质相似,均易与一氧化碳作用形成羰基配合物,中心原子价电子数与配位体提供的成键电子数遵循
 规则。如:
规则。如: ,则镍与CO形成的配合物化学式为
,则镍与CO形成的配合物化学式为 键和
键和 键数目之比为
键数目之比为(6)NiO的晶胞结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为
 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为a pm,设阿伏加德罗常数值为
的半径为a pm,设阿伏加德罗常数值为 ,每平方米面积上具有该晶体的质量为
,每平方米面积上具有该晶体的质量为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】锑属于氮族元素,广泛用于制造合金、瓷器、颜料、印刷油墨、防爆材料等。现用锑精矿(主要含有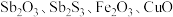 等杂质)来制备锑和焦锑酸钠
等杂质)来制备锑和焦锑酸钠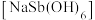 。其工艺流程如图所示:
。其工艺流程如图所示: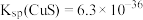 ,
,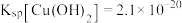 。
。
回答下列问题:
(1) 位于元素周期表的
位于元素周期表的___________ 区,其基态原子的价电子排布式为___________ 。
(2)滤渣Ⅰ的主要成分有___________ 。
(3)“碱浸”时, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(4)“电解”过程中,阳极上发生的两个电极反应式为___________ 、___________ 。
(5)滤渣Ⅱ的主要成分有___________ 。
(6)产品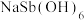 需洗涤、干燥,检验固体是否洗涤干净的试剂为
需洗涤、干燥,检验固体是否洗涤干净的试剂为___________ (填化学式)。
(7)常温条件下,向碱浸液中加入 溶液,生成
溶液,生成 和
和 沉淀时,溶液的
沉淀时,溶液的 为10,则溶液中剩余
为10,则溶液中剩余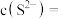
___________  。
。
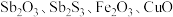 等杂质)来制备锑和焦锑酸钠
等杂质)来制备锑和焦锑酸钠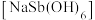 。其工艺流程如图所示:
。其工艺流程如图所示: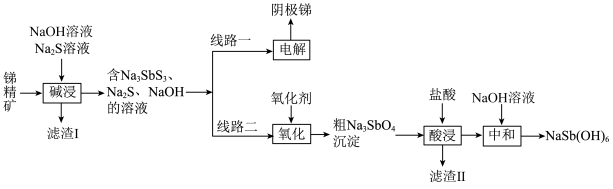
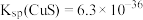 ,
,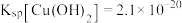 。
。回答下列问题:
(1)
 位于元素周期表的
位于元素周期表的(2)滤渣Ⅰ的主要成分有
(3)“碱浸”时,
 发生反应的化学方程式为
发生反应的化学方程式为(4)“电解”过程中,阳极上发生的两个电极反应式为
(5)滤渣Ⅱ的主要成分有
(6)产品
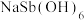 需洗涤、干燥,检验固体是否洗涤干净的试剂为
需洗涤、干燥,检验固体是否洗涤干净的试剂为(7)常温条件下,向碱浸液中加入
 溶液,生成
溶液,生成 和
和 沉淀时,溶液的
沉淀时,溶液的 为10,则溶液中剩余
为10,则溶液中剩余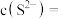
 。
。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】请完成下列小题:
(1)工业上可利用CO2和H2生成甲醇,热化学方程式如下:
CO2(g)+3H2(g) CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
又查资料得知:①CH3OH(l)+ O2(g)
O2(g)  CO2(g)+H2(g) △H=Q2 kJ·mol-1
CO2(g)+H2(g) △H=Q2 kJ·mol-1
②H2O(g)= H2O(l) △H=Q3 kJ·mol-1
则表示甲醇的燃烧热的热化学方程式为________________ 。
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:
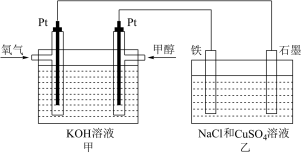
(2)写出甲中通入甲醇这一极的电极反应式_______________________ 。
(3)理论上乙中两极所得气体的体积随时间变化的关系如图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式___________ ,原混合溶液中NaCl的物质的量浓度为_______ mol/L。(设溶液体积不变)

(4)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为_________ g。
(5)已知草酸H2C2O4为弱酸。
①常温下,下列事实能说明草酸是弱电解质的是____________ 。
A.向草酸钠溶液加酚酞,溶液变红
B.取一定量草酸溶液加水稀释至10倍,pH变化小于1
C.草酸能使酸性KMnO4溶液褪色
D.取相同pH的草酸溶液和盐酸,分别加入足量的大小、形状相同的镁条,草酸溶液反应速度快
②常温下,0.1mol·L-1的草酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC2O4-)+2c(C2O42-)=________________ 。(用准确的数学表达式表示)
(1)工业上可利用CO2和H2生成甲醇,热化学方程式如下:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1
CH3OH(l)+H2O(g) △H=Q1 kJ·mol-1又查资料得知:①CH3OH(l)+
 O2(g)
O2(g)  CO2(g)+H2(g) △H=Q2 kJ·mol-1
CO2(g)+H2(g) △H=Q2 kJ·mol-1②H2O(g)= H2O(l) △H=Q3 kJ·mol-1
则表示甲醇的燃烧热的热化学方程式为
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:

(2)写出甲中通入甲醇这一极的电极反应式
(3)理论上乙中两极所得气体的体积随时间变化的关系如图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式

(4)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为
(5)已知草酸H2C2O4为弱酸。
①常温下,下列事实能说明草酸是弱电解质的是
A.向草酸钠溶液加酚酞,溶液变红
B.取一定量草酸溶液加水稀释至10倍,pH变化小于1
C.草酸能使酸性KMnO4溶液褪色
D.取相同pH的草酸溶液和盐酸,分别加入足量的大小、形状相同的镁条,草酸溶液反应速度快
②常温下,0.1mol·L-1的草酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC2O4-)+2c(C2O42-)=
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。请回答下列问题:
(1)戊离子的结构示意图为________ 。
(2)写出乙的单质的电子式:________ 。
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原的物质的物质的量之比为________ 。
(4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:____________ 。
(5)按图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:____________ 。

(1)戊离子的结构示意图为
(2)写出乙的单质的电子式:
(3)戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原的物质的物质的量之比为
(4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:
(5)按图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】钴钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有MoS2、CoS和Al2O3)中回收钴和钼的工艺流程如图:

已知:浸取液中的金属离子主要为MoO 、Co2+、Al3+。
、Co2+、Al3+。
(1)钼酸铵[(NH4)2MoO4]中Mo的化合价为________ ,MoS2在空气中高温焙烧产生两种氧化物:SO2和____________ (填化学式)。
(2)为了加快酸浸速率,可采取的措施为_______________________ (任写一条)。
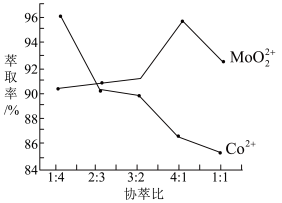
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取MoO 和Co2+,萃取情况如图所示,当协萃比
和Co2+,萃取情况如图所示,当协萃比
_________________ ,更有利于MoO 的萃取。
的萃取。
(4)操作Ⅰ的名称为_______________________ 。
(5)向有机相1中滴加氨水,发生反应的离子方程式为_____________________________ 。
(6)Co2+萃取的反应原理为Co2+ +2HR CoR2 +2H+,向有机相2中加入H2SO4能进行反萃取的原因是
CoR2 +2H+,向有机相2中加入H2SO4能进行反萃取的原因是_______________________ (结合平衡移动原理解释)。
(7)Co3O4可用作电极,若选用KOH电解质溶液,通电时可转化为CoOOH,其电极反应式为___________________________ 。

已知:浸取液中的金属离子主要为MoO
 、Co2+、Al3+。
、Co2+、Al3+。(1)钼酸铵[(NH4)2MoO4]中Mo的化合价为
(2)为了加快酸浸速率,可采取的措施为
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取MoO
 和Co2+,萃取情况如图所示,当协萃比
和Co2+,萃取情况如图所示,当协萃比
 的萃取。
的萃取。
(4)操作Ⅰ的名称为
(5)向有机相1中滴加氨水,发生反应的离子方程式为
(6)Co2+萃取的反应原理为Co2+ +2HR
 CoR2 +2H+,向有机相2中加入H2SO4能进行反萃取的原因是
CoR2 +2H+,向有机相2中加入H2SO4能进行反萃取的原因是(7)Co3O4可用作电极,若选用KOH电解质溶液,通电时可转化为CoOOH,其电极反应式为
您最近一年使用:0次