(1)铁与同周期的钙性质有很大的差异,铁的熔点更高,而钙的金属活动性更强,这都说明铁的金属键比钙更_____ (选填“强”、“弱”)。与钢铁比,纯净的铁有很强的抗腐蚀性,原因是_______________________ 。氯化铁受热会发生升华现象,这说明氯化铁是______ (选填“离子”、“共价”)化合物。
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g)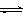 FeO(s)+CO(g),该反应的平衡常数表达式K=
FeO(s)+CO(g),该反应的平衡常数表达式K=_____________ 。下列措施中能使平衡时c(CO)/c(CO2)增大的是______ (选填编号)。
a.升高温度 b.增大压强
c.充入一定量CO d.再加入一些铁粉
(3)FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。__________
____□FeS2+ □Fe2(SO4)3 +□____→ □FeSO4 +□____
(4)溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成; 将FeCl3溶液滴加到Na2S溶液中,生成的是Fe2S3而不是S或Fe(OH)3。从以上反应可得出的结论是______________________ 。
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g)
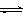 FeO(s)+CO(g),该反应的平衡常数表达式K=
FeO(s)+CO(g),该反应的平衡常数表达式K=a.升高温度 b.增大压强
c.充入一定量CO d.再加入一些铁粉
(3)FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。
____□FeS2+ □Fe2(SO4)3 +□____→ □FeSO4 +□____
(4)溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成; 将FeCl3溶液滴加到Na2S溶液中,生成的是Fe2S3而不是S或Fe(OH)3。从以上反应可得出的结论是
2015·上海静安·二模 查看更多[3]
更新时间:2017-04-06 10:16:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】聚合硫酸铁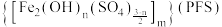 是一种应用广泛的水处理剂。制备方法如下:
是一种应用广泛的水处理剂。制备方法如下:
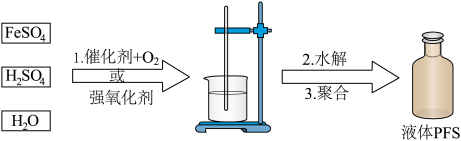
(1)氧化可采用催化氧化或直接氧化。
①以 为氧化剂,
为氧化剂, 作催化剂,需控温55℃,反应4h。氧化的化学方程式为
作催化剂,需控温55℃,反应4h。氧化的化学方程式为_______ 。
②以 为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是
为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是_______ 。
③以NaClO作为氧化剂,比方法② 用量大,反应中生成少量污染性气体。原因是
用量大,反应中生成少量污染性气体。原因是_______ 。
(2)水解-聚合过程中部分反应过程如下:

①水解-聚合过程中pH变化趋势是_______ 。
②聚合的原理是_______ 。
③聚合硫酸铁净水效果好的原因是_______ 。
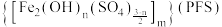 是一种应用广泛的水处理剂。制备方法如下:
是一种应用广泛的水处理剂。制备方法如下:
(1)氧化可采用催化氧化或直接氧化。
①以
 为氧化剂,
为氧化剂, 作催化剂,需控温55℃,反应4h。氧化的化学方程式为
作催化剂,需控温55℃,反应4h。氧化的化学方程式为②以
 为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是
为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是③以NaClO作为氧化剂,比方法②
 用量大,反应中生成少量污染性气体。原因是
用量大,反应中生成少量污染性气体。原因是(2)水解-聚合过程中部分反应过程如下:

①水解-聚合过程中pH变化趋势是
②聚合的原理是
③聚合硫酸铁净水效果好的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】“价—类”二维图基于核心元素的化合价和物质类别研究物质,为我们认识物质性质和实现物质转化提供了新思路。如图是硫及其化合物的“价—类”二维图,其中的箭头表示部分物质间的转化关系,请根据要求回答相关问题。
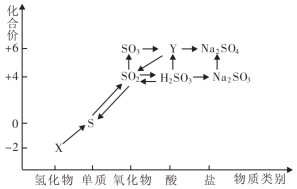
(1)X的化学式为___ 。
(2)请写出SO2转化为H2SO3的化学方程式___ ,将Na2SO3转化为Na2SO4,需加入__ (填“氧化剂”或“还原剂”)。
(3)Y的浓溶液与铜单质在一定条件下可以发生化学反应生成SO2,该反应的化学方程式为__ 。
(4)24mL0.05mol•L-1的Na2SO3溶液与20mL0.02mol•L-1的K2Cr2O7溶液恰好反应,已知Na2SO3转化为Na2SO4,则Cr元素在还原产物中的化合价为___ 。
(5)硫代硫酸钠(Na2S2O3)是一种重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方法理论上可行的是___ (填字母)。
A.SO2+Na2SO3 B.SO2+Na2SO4 C.Na2SO3+Na2SO4 D.S+Na2SO3

(1)X的化学式为
(2)请写出SO2转化为H2SO3的化学方程式
(3)Y的浓溶液与铜单质在一定条件下可以发生化学反应生成SO2,该反应的化学方程式为
(4)24mL0.05mol•L-1的Na2SO3溶液与20mL0.02mol•L-1的K2Cr2O7溶液恰好反应,已知Na2SO3转化为Na2SO4,则Cr元素在还原产物中的化合价为
(5)硫代硫酸钠(Na2S2O3)是一种重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方法理论上可行的是
A.SO2+Na2SO3 B.SO2+Na2SO4 C.Na2SO3+Na2SO4 D.S+Na2SO3
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】高温下炼铁的主要反应为:Fe2O3(s) + 3CO(g) 2Fe(s) + 3CO2(g) - Q
(1)写出该反应的平衡常数的表达式_____________________ 。当混合气体的________________ (填物理量名称)不变时,表明上述反应已达到平衡。
(2)写出一种能提高上述反应中氧化铁转化率的措施__________________ 。取一定量铝热剂,在高温下进行铝热反应:2Al + Fe2O3  2Fe + Al2O3。
2Fe + Al2O3。
(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁_______ g。
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
_____________________________________________
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
______________________________________________________________________
______________________________________________________________________
(1)写出该反应的平衡常数的表达式
(2)写出一种能提高上述反应中氧化铁转化率的措施
 2Fe + Al2O3。
2Fe + Al2O3。(3)请标出电子转移的方向和数目。若反应中有 1.5 mol 电子转移,可得到铁
(4)将铝热剂直接加到足量氢氧化钠溶液中,有气体生成。请写出该现象对应的离子方程式。
(5)若将铝热反应后所得固体用足量盐酸溶解,并加入硫氰化钾溶液,溶液不变血红色。据此能否确认固体中已不含氧化铁?说明理由。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】良好生态环境是最普惠的民生福祉。治理大气污染物CO、NOX、SO2具有十分重要的意义。
(1)氧化还原法消除NOX的转化如下所示: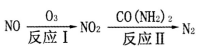 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是_________ 。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________ 。
(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式_______________ 。装置III中发生反应的离子方程式为_________________ 。
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气____ L(用含a代数式表示)。
(1)氧化还原法消除NOX的转化如下所示:
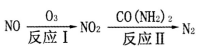 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】NaCN超标的电镀废水可用两段氧化法处理:
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为___________ (选填“酸性”、“碱性”或“中性”);原因是___________ 。
(2)写出第二次氧化时发生反应的离子方程式。___________
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成___________ 、___________ 和H2O。
a.NaCN与NaClO反应,生成NaOCN和NaCl
b.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(1)第一次氧化时,溶液的pH应调节为
(2)写出第二次氧化时发生反应的离子方程式。
(3)(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2020年世界环境日的宣传主题为“关爱自然。刻不容慢”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。
(1)氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。
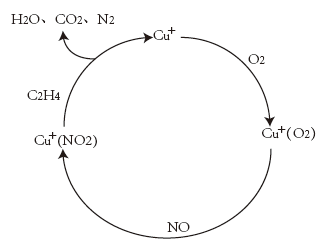
C2H4催化还原NO是重要的烟气脱硝技术,研究发现在Cu+上可能发生的反应过程如图。写出该脱硝过程的总反应的化学方程式:___________ 。
(2)烟气中的氮氧化物经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中氮氧化物的含量。
①室温下,固定进入反应器的NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前n(O3):n(NO)的变化见下图。
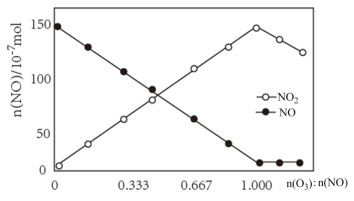
当n(O3):n(NO)≤1时,发生反应的化学方程式为___________ ;
当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是___________ ;
②当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(弱碱性)中SO 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为___________ 。
(3)可综合利用上述吸收烟气后的溶液处理含NH 废水,每产生1 mol无污染气体转移电子数为
废水,每产生1 mol无污染气体转移电子数为_______ 。
(1)氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。

C2H4催化还原NO是重要的烟气脱硝技术,研究发现在Cu+上可能发生的反应过程如图。写出该脱硝过程的总反应的化学方程式:
(2)烟气中的氮氧化物经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中氮氧化物的含量。
①室温下,固定进入反应器的NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前n(O3):n(NO)的变化见下图。

当n(O3):n(NO)≤1时,发生反应的化学方程式为
当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是
②当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(弱碱性)中SO
 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为(3)可综合利用上述吸收烟气后的溶液处理含NH
 废水,每产生1 mol无污染气体转移电子数为
废水,每产生1 mol无污染气体转移电子数为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】乙苯催化脱氢制取苯乙烯的反应为: (g)+CO2(g)⇌
(g)+CO2(g)⇌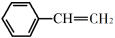 (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
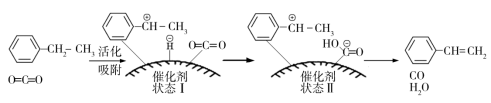
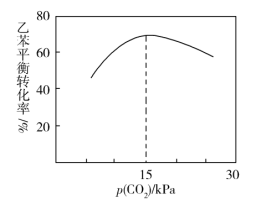
一定温度下,向恒容密闭容器中充入一定量的乙苯和CO2,起始压强为p0[气体分压(p分)=气体总压(p总)×气体体积分数]。乙苯平衡转化率与p(CO2)的关系如下图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因_______ 。
 (g)+CO2(g)⇌
(g)+CO2(g)⇌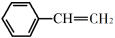 (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
一定温度下,向恒容密闭容器中充入一定量的乙苯和CO2,起始压强为p0[气体分压(p分)=气体总压(p总)×气体体积分数]。乙苯平衡转化率与p(CO2)的关系如下图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】合成氨的温度和压强通常控制在约500 ℃以上20~50MPa的范围。当进入合成塔的N2和H2体积之比为1∶3时,经科学实验测定,在相应条件下N2和H2反应所得氨的平衡浓度(体积分数)如表所示,而实际上从合成塔出来的混合气体中含有氨约为15%。请回答下列问题:

(1)298 K下合成氨时,每生成1 mol·L-1氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为_______ 。在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在的条件下进行反应,测得反应放出的热量总小于92.4 kJ,其原因是_______ 。
(2)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的根本原因是_______。
(3)若工业生产中N2和H2按投料比为1∶2.8的比例进入合成塔,那么转化率较大的应该是_______ ,采用此投料比的原因是_______ ,若从合成塔出来的混合气体中氨的体积分数仍为15%,则N2和H2的转化率之比是_______ 。

(1)298 K下合成氨时,每生成1 mol·L-1氨气,同时放出46.2 kJ的热量,则该反应的热化学方程式为
(2)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的根本原因是_______。
| A.表中所测数据有明显误差 |
| B.生产条件控制不当 |
| C.氨的分解速度大于预测值 |
| D.合成塔中的反应未达到平衡状态 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲醇是重要的化工原料。利用合成气(主要成分为CO、 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:
Ⅰ.

Ⅱ.

在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
(1)
_______ 0,其理由是_______ 。
(2)能判断该反应达到化学平衡状态的依据是_______。
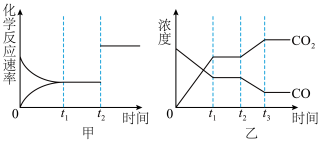
(3)图甲、图乙分别表示反应在 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况。图甲中
时刻因改变某个条件而发生变化的情况。图甲中 时刻发生改变的条件是
时刻发生改变的条件是_______ ,图乙中 时刻发生改变的条件是
时刻发生改变的条件是_______ 。
(4)若1200℃时,在某时刻平衡体系中 、
、 、
、 、
、 的浓度分别为
的浓度分别为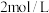 、
、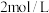 、
、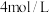 、
、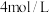 ,此时v(正)
,此时v(正)_______ v(逆)(填大于、小于或等于),其理由是_______ 。
 和
和 )在催化剂的作用下合成甲醇,发生的主要反应如下:
)在催化剂的作用下合成甲醇,发生的主要反应如下:Ⅰ.


Ⅱ.


在恒容密闭容器进行反应Ⅰ,测得其化学平衡常数K和温度t的关系如表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)

(2)能判断该反应达到化学平衡状态的依据是_______。
A. | B.容器内 的体积分数保持不变 的体积分数保持不变 |
| C.容器内气体密度保持不变 | D.容器中压强保持不变 |
(3)图甲、图乙分别表示反应在
 时刻达到平衡,在
时刻达到平衡,在 时刻因改变某个条件而发生变化的情况。图甲中
时刻因改变某个条件而发生变化的情况。图甲中 时刻发生改变的条件是
时刻发生改变的条件是 时刻发生改变的条件是
时刻发生改变的条件是
(4)若1200℃时,在某时刻平衡体系中
 、
、 、
、 、
、 的浓度分别为
的浓度分别为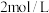 、
、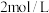 、
、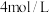 、
、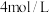 ,此时v(正)
,此时v(正)
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)前20号元素中气态氢化物最稳定的是:_____ (填化学式)。
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:_____ (填写名称)。
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:____ (填化学式)。
(4)短周期主族元素中原子半径最大的元素是:_____ (填写名称)。
(5)Fe在元素周期表中位置为:______ 。
(6)以下晶体,存在分子间作用力的共价化合物是_______ (填序号)。
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_______ (填序号)。
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
(1)前20号元素中气态氢化物最稳定的是:
(2)前20号元素中最高价氧化物对应水化物碱性最强的碱为:
(3)第Ⅵ A族元素所形成的氢化物中沸点最高的是:
(4)短周期主族元素中原子半径最大的元素是:
(5)Fe在元素周期表中位置为:
(6)以下晶体,存在分子间作用力的共价化合物是
①Ne晶体 ②NH4Cl晶体 ③CaCl2晶体 ④干冰 ⑤水晶
(7)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
① HCl的溶解度比H2S的大
② HCl的酸性比H2S的强
③ HCl的稳定性比H2S的强
④ Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑤ HClO4的酸性比H2SO4的强
⑥ Cl2能与H2S反应生成S
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z三种元素位于元素周期表的不同短周期内,X与Z属于同主族元素,Z元素的焰色反应为黄色。X单质与Y单质相互化合可以得到X2Y和X2Y2两种液体化合物,Z单质与Y单质相互化合可以得到Z2Y与Z2Y2两种固体化合物,其中Z、Z2Y、Z2Y2都能与X2Y反应生成一种能使无色酚酞变红的ZYX溶液。
(1)试推测X、Y所代表的元素分别为X______ 、Y______ (填元素符号), X2Y和Z2Y的化合物类型分别是__________ 、___________ ;
(2)写出Z单质与X2Y反应的离子方程式_________________________________________ ;
(3)写出Z2Y2与X2Y反应的化学方程式_________________________________________ 。
(1)试推测X、Y所代表的元素分别为X
(2)写出Z单质与X2Y反应的离子方程式
(3)写出Z2Y2与X2Y反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩中10种元素回答以下问题:
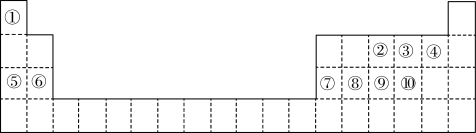
(1)写出⑧元素在周期表的位置______________________ ;
(2)实验室制取②氢化物的化学方程式_______________________________________ ;
②的氢化物与其最高价氧化物水化物反应生成的物质是________________ (填名称)
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是________ (填“共价化合物”或“离子化合物”),可以证明你判断正确的实验依据为:________________________ 。
(4)用电子式表示④、⑥两元素结合成化合物的形成过程____________________________ 。

(1)写出⑧元素在周期表的位置
(2)实验室制取②氢化物的化学方程式
②的氢化物与其最高价氧化物水化物反应生成的物质是
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是
(4)用电子式表示④、⑥两元素结合成化合物的形成过程
您最近半年使用:0次



