铁及其化合物在生产、生活中存在广泛用途。

(1)如图是铁元素在元素周期表中的有关信息。
补全铁原子的核外电子排布式_____________ 3p63d64s2。“55.85”是________________________ 。自然界中存在的54Fe和56Fe,它们互称为_____________ 。
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是_____________ 。通常证明某溶液中含Fe2+的化学方法是_____________________ 。
(3)SO2 有强还原性,写出其与 FeCl3 溶液反应的离子方程式______________________ 。
若有 0.4mol FeCl3 发生反应,则需要标准状况下的 SO2______________ 升。
(4)发黄的深井水通常含 Fe3+,若向水中加入 Na2CO3 溶液,则产生红褐色沉淀和无色无味的气体。请从平衡移动角度解释这一现象___________________ 。

(1)如图是铁元素在元素周期表中的有关信息。
补全铁原子的核外电子排布式
(2)将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是
(3)SO2 有强还原性,写出其与 FeCl3 溶液反应的离子方程式
若有 0.4mol FeCl3 发生反应,则需要标准状况下的 SO2
(4)发黄的深井水通常含 Fe3+,若向水中加入 Na2CO3 溶液,则产生红褐色沉淀和无色无味的气体。请从平衡移动角度解释这一现象
更新时间:2017-05-03 13:20:55
|
相似题推荐
【推荐1】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2 7N2+12H2O
7N2+12H2O
①该反应的氧化剂是____ 。
②用单线桥表示该反应中电子转移的方向和数目:____ 。
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是_______ (填序号)。
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+ +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)
①配平后的反应中H+前的化学计量数为_________ 。
②由反应可知酸性条件下粒子的氧化性大小:____ >____ 。
(1)在催化剂作用下,NH3可与NO2发生如下反应:8NH3+6NO2
 7N2+12H2O
7N2+12H2O①该反应的氧化剂是
②用单线桥表示该反应中电子转移的方向和数目:
③为研究哪些物质能将NOx转化为N2以消除污染,根据氧化还原反应的知识可知,下列物质中不适宜选用的是
A.CO B.H2 C.CO2
(2)水体中含有较多的硝酸盐会污染水质。一种用铁粉处理水体中的硝酸盐的反应如下:Fe+
 +H+-Fe2++
+H+-Fe2++ +H2O(未配平)
+H2O(未配平)①配平后的反应中H+前的化学计量数为
②由反应可知酸性条件下粒子的氧化性大小:
您最近一年使用:0次
【推荐2】氰化钠化学式为NaCN,白色结晶颗粒或粉末,易潮解,易溶于水,有微弱的苦杏仁气味,剧毒,皮肤伤口接触、吸入、吞食微量可中毒死亡,是一种重要的化工原料,用于电镀、冶金和有机合成医药、农药及金属处理方面。试回答下列问题:
(1)NaCN中C元素显________ 价,N元素显________ 价。
(2)在微生物的作用下,CN-能够被氧气氧化,生成碳酸氢钠和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性,写出上述反应的离子方程式____________ 。
(3)用硫代硫酸钠也可处理含CN-的废水,反应的离子方程式为CN-+S2O32-=A+SO32-,A为_____________ (填化学式)。
(4)白磷有毒,能和氯酸溶液发生氧化还原反应:3P4+10HClO3+18H2O=10HCl+12H3PO4,该反应的氧化剂是________ ,还原产物是________ ,若有1mol P4参加反应转移电子数为________ 。
(1)NaCN中C元素显
(2)在微生物的作用下,CN-能够被氧气氧化,生成碳酸氢钠和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性,写出上述反应的离子方程式
(3)用硫代硫酸钠也可处理含CN-的废水,反应的离子方程式为CN-+S2O32-=A+SO32-,A为
(4)白磷有毒,能和氯酸溶液发生氧化还原反应:3P4+10HClO3+18H2O=10HCl+12H3PO4,该反应的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】Ⅰ.请回答:
(1)H2O2的电子式___________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________ 。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式___________ 。
(4)完成以下氧化还原反应的离子方程式:___________
( ) +( )C2O
+( )C2O +___________=( )Mn2++( )CO2↑+___________
+___________=( )Mn2++( )CO2↑+___________
Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4.将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(5)甲的化学式___________ 。
(6)甲与AlCl3反应得到NaAlH4的化学方程式___________ 。
(7)NaAlH4与水发生氧化还原反应的化学方程式___________ 。
(8)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式___________ 。
(9)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由___________ 。
(1)H2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)完成以下氧化还原反应的离子方程式:
( )
 +( )C2O
+( )C2O +___________=( )Mn2++( )CO2↑+___________
+___________=( )Mn2++( )CO2↑+___________Ⅱ.化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4.将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(5)甲的化学式
(6)甲与AlCl3反应得到NaAlH4的化学方程式
(7)NaAlH4与水发生氧化还原反应的化学方程式
(8)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式
(9)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。判断该同学设想的制备和验纯方法的合理性并说明理由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是________ 。
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是______ 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____ (填离子符号);实验①和③说明:在I- 过量的情况下,溶液中仍含有______ (填离子符号),由此可以证明该氧化还原反应为______ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________ ;
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】亚铁盐由于具有较强的还原性,久置于空气中容易氧化变质,日常实验中常以复盐硫酸亚铁铵晶体 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过___________ (操作)处理后再使用。向 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是___________ (填字母)。
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,
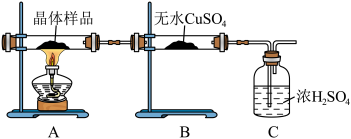
①若B装置中无水 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是___________ 。
②另取少量晶体于试管中,加水溶解,___________ (填操作与现象),证明晶体中有 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:___________ 。
 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:| 溶剂 | 蒸馏水 | ||||
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 9.8 | 22.0 | 28.2 | 35.7 | 45.2 |
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制
 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,

①若B装置中无水
 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是②另取少量晶体于试管中,加水溶解,
 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据要求填空:
(1)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下:
 .
.
①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)______________________________________________________ 。
②该反应中,______ 是氧化剂,______ 是氧化产物.
③转移3mol电子,则所产生的氮气在标准状况下的体积为______ .
(2)铁是人类较早使用的金属之一.
①鉴别 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是______ .
②某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是______ (填序号).
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有
(1)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下: .
.①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)
②该反应中,
③转移3mol电子,则所产生的氮气在标准状况下的体积为
(2)铁是人类较早使用的金属之一.
①鉴别
 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是②某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有

C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)①常温下,0.01mol/L的二元酸H2A溶液的pH=5,其电离方程式为________ 。
②用Al2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式________________________________________________________ 。
③比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa___________ NaClO;CuSO4_________ KHCO3。(填“>”、“<”或“=”)
(2)25℃时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
①混合溶液中由水电离出的c(H+)________ 0.1mol/LNaOH溶液中由水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合物中下列算式的计算结果(填具体数字):
c(A-)+c(HA)=__________ mol/L; c(OH-)-c(HA)=__________ mol/L。
②用Al2(SO4)3与NaHCO3溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式
③比较0.1mol/L的下列各种溶液的pH大小:
CH3COONa
(2)25℃时,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=10。试回答以下问题:
①混合溶液中由水电离出的c(H+)
②求出混合物中下列算式的计算结果(填具体数字):
c(A-)+c(HA)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)写出泡沫灭火器(硫酸铝和碳酸氢钠溶液)灭火时发生反应的离子方程式:_______ 。
(2)写出明矾(KAl(SO4)2·12H2O)净水原理的离子方程式_______ 。
(3)物质的量浓度相同的①NH4Cl;②NH4HCO3;③NH4HSO4;④(NH4)2SO4四种溶液中,c(NH )由大到小的顺序是
)由大到小的顺序是_______ 。
(4)等物质的量浓度的下列溶液:①NaCl②CH3COONa③NH4Cl④AlCl3⑤Ba(OH)2⑥Na2CO3⑦NaHCO3⑧NaHSO4⑨NaOH⑩H2SO4其pH值由大到小的顺序是(填序号)_______ 。
(5)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO﹣+H+△H>0,下列方法中,可以使0.10mol·L﹣1CH3COOH溶液中CH3COOH电离程度增大的是_______ 。
a.加入少量0.10mol·L﹣1的稀盐酸b.加热c.加水稀释至0.010mol·L﹣1d.加入少量冰醋酸e.加入少量氯化钠固体f.加入少量0.10mol·L﹣1的NaOH溶液
(6)将FeCl2溶液蒸干、灼烧后所得固体为:_______ ;Al2(SO4)3溶液蒸干所得固体为:_______ 。配制FeCl3溶液时,加入少量的_______ ,目的是_______ 。
(1)写出泡沫灭火器(硫酸铝和碳酸氢钠溶液)灭火时发生反应的离子方程式:
(2)写出明矾(KAl(SO4)2·12H2O)净水原理的离子方程式
(3)物质的量浓度相同的①NH4Cl;②NH4HCO3;③NH4HSO4;④(NH4)2SO4四种溶液中,c(NH
 )由大到小的顺序是
)由大到小的顺序是(4)等物质的量浓度的下列溶液:①NaCl②CH3COONa③NH4Cl④AlCl3⑤Ba(OH)2⑥Na2CO3⑦NaHCO3⑧NaHSO4⑨NaOH⑩H2SO4其pH值由大到小的顺序是(填序号)
(5)在一条件下,CH3COOH溶液中存在电离平衡:CH3COOH⇌CH3COO﹣+H+△H>0,下列方法中,可以使0.10mol·L﹣1CH3COOH溶液中CH3COOH电离程度增大的是
a.加入少量0.10mol·L﹣1的稀盐酸b.加热c.加水稀释至0.010mol·L﹣1d.加入少量冰醋酸e.加入少量氯化钠固体f.加入少量0.10mol·L﹣1的NaOH溶液
(6)将FeCl2溶液蒸干、灼烧后所得固体为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】基态24Cr的核外电子排布式为___________ ;基态35Br-的核外电子排布式为___________ ,原子结构示意图为___________ ;基态Fe原子结构示意图为___________ 。
您最近一年使用:0次
【推荐2】①、②、③、④是原子序数依次增大的四种短周期元素,①周期表中原子半径最小的元素,②的最外层电子数比次外层多1,③的第一电离能比左右相邻两元素的都要大,④是周期表中电负性最大的元素。元素①和③可形成一种三角锥形的分子A,元素②和④可形成一种平面三角形的分子B。
(1)元素②的基态原子的电子排布式为___________ 。
(2)元素③的价电子的轨道表示式为___________ 。
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:___________ (用元素符号表示)。
(4)分子A的电子式为___________ ,分子B的中心原子杂化方式为___________ ;A与B之间能否形成配位键?若能,用化学用语表示出两者之间的配位键;若不能,说明理由:___________ 。
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:___________ 。
(1)元素②的基态原子的电子排布式为
(2)元素③的价电子的轨道表示式为
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:
(4)分子A的电子式为
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分类思想是化学重要的学科思想。下表是对部分常见的 18 电子微粒的分类。
请结合表格中的微粒(或由微粒组成的物质)完成下列问题:
(1)根据分类时呈现的规律,可推知表格中:①_________ ②_______ (填分子式)
(2)热稳定性:H2S____ SiH4(填“>”、“<”或“=”)还原性:Cl- ___ S2-(填“>”、“<”或“=”)
(3)KHS的电子式为______ , CaO2和 N2H4均含有____ 键(填“离子”、“极性”“非极性'”)
(4)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2)当它们混合时 , 即产 生大量的N2和水蒸气,并放出大量热。已知 0.2mol 液态肼 和足量H2O2反应,生成氮气和水蒸气, 放出 Q kJ 的热量。写出该反应的热化学方程式____ 。
(5)已知拆开 lmolHCl 分子中的化学键需要消耗 431kJ 能量, 根据下面的能量图,回答下列问题:
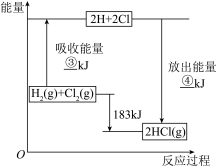
分别写出③、④ 的数值:③______ kJ;④______ kJ。
(6)已知在常温常压下:
2CH3OH(l)+ 3O2(g)=2CO2(g)+4H2O(g) ΔH= -1275.6kJ/mol
H2O(l)= H2O(g) ΔH = + .44.0kJ/mol
写出表示甲醇燃烧热的热化学方程式_______ 。
| 分子 | Ar |
| HCl H2S ① SiH4 | |
| F2 H2O2 N2H4 ② | |
| CH3F CH3OH | |
| 阳离子 | K+ Ca2+ |
| 阴离子 | Cl- S2- |
HS- O |
请结合表格中的微粒(或由微粒组成的物质)完成下列问题:
(1)根据分类时呈现的规律,可推知表格中:①
(2)热稳定性:H2S
(3)KHS的电子式为
(4)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2)当它们混合时 , 即产 生大量的N2和水蒸气,并放出大量热。已知 0.2mol 液态肼 和足量H2O2反应,生成氮气和水蒸气, 放出 Q kJ 的热量。写出该反应的热化学方程式
(5)已知拆开 lmolHCl 分子中的化学键需要消耗 431kJ 能量, 根据下面的能量图,回答下列问题:

分别写出③、④ 的数值:③
(6)已知在常温常压下:
2CH3OH(l)+ 3O2(g)=2CO2(g)+4H2O(g) ΔH= -1275.6kJ/mol
H2O(l)= H2O(g) ΔH = + .44.0kJ/mol
写出表示甲醇燃烧热的热化学方程式
您最近一年使用:0次



