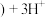下列化学用语表示正确的是
A.碳酸的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| B.碱性氢氧燃料电池负极的电极反应式:H2-2e-==2H+ |
C.HCO3-的水解方程式:HCO3-+H2O CO32-+H2O+ CO32-+H2O+ |
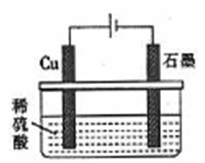
D.如图所示,反应开始时的离子方程式:Cu+2H+ Cu2++H2↑ Cu2++H2↑ |
更新时间:2017-05-03 09:03:15
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】关于电解质溶液下列说法中不正确的是
A.向浓度均为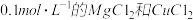 混合溶液中逐滴加入氨水,先生成蓝色 混合溶液中逐滴加入氨水,先生成蓝色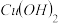 沉淀,则 沉淀,则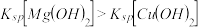 |
| B.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaOH溶液的体积前者是后者的10倍 |
C.由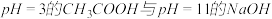 溶液等体积混合,其离子浓度的顺序为: 溶液等体积混合,其离子浓度的顺序为: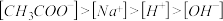 |
D.某温度下纯水中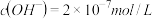 ,则该温度下0.1mol/L的盐酸的pH=1 ,则该温度下0.1mol/L的盐酸的pH=1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,已知:Ka(CH3COOH)=1.8×10-5,Kb(NH3·H2O)=1.8×10-5,下列说法正确的是
| A.向0.1mol·L-lCH3COOH溶液中滴入氨水,至中性:c(NH3·H2O)+c(NH4+)>c(CH3COO-)+c(CH3COOH) |
| B.向20 mL 1 mol·L-l CH3 COONa溶液中通入0.01 mol HCl:c(Na+)>c(Cl-)>c( CH3COO-)>c(H+) |
| C.向100mL0.1 mol·L-l NH4HSO4溶液中通入224mL(标况下)NH3:c(NH3·H2O)=c(H+)-c(OH-) |
| D.用0.1mol·L-l醋酸滴定10.00mL0.1mol·L-l的NaOH溶液至恰好中和:c(CH3COOH)+c(H+)=c(CH3COO-)+ c(OH-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,将醋酸和氢氧化钠溶液混合,所得溶液pH=7,下列叙述正确的是
| A.若浓度相同,混合时V(NaOH)>V(CH3COOH) |
| B.若体积相同,混合时c(CH3COOH)<c(NaOH) |
| C.混合后的溶液中溶质既有CH3COONa又有CH3COOH |
| D.无法确定混合后的溶液中c(CH3COO-)与c(Na+)的关系 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验的反应原理用离子方程式表示正确的是
A.室温下,测得氯化铵溶液pH<7: |
B.用金属铜作为电极电解硫酸铜溶液: |
C.在酸化的 溶液中滴加少量“84”消毒液: 溶液中滴加少量“84”消毒液: |
D.用高锰酸钾标准溶液滴定草酸: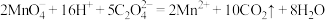 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某酸式盐NaHY的水溶液显碱性,下列叙述正确的是
| A.该酸式盐溶液中离子浓度关系:[Na+]>[HY-]>[OH-]>[H+] |
B.HY-的水解方程式:HY-+H2O H3O++Y2– H3O++Y2– |
| C.该酸式盐溶液中离子浓度关系:[Na+]>[Y2–] >[HY-]>[OH-]>[H+] |
D.H2Y的电离方程式:H2Y 2H++Y2– 2H++Y2– |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】电化学原理在化学工业中有广泛的应用。根据如下工作原理图,下列说法正确的是
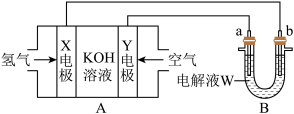

A.电极Y为正极,电极反应式为: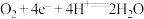 |
| B.若W为饱和食盐水(滴有几滴酚酞溶液),则工作一段时间后a电极附近溶液变红 |
C.若a为粗铜(含Zn、Ag等杂质),W为CuSO4溶液,工作一段时间后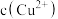 减小 减小 |
| D.若a为银棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.16g,则X电极消耗氢气0.224L |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】燃料电池的优点是化学能直接转化为电能,而不经过热能这一中间环节,能量利用率高。氢氧燃料电池可同时供应电和水蒸气,所需燃料为H2,电解质为熔融K2CO3。已知该电池的正极反应为O2+2CO2+4e- 2CO32-。下列叙述正确的是
2CO32-。下列叙述正确的是
 2CO32-。下列叙述正确的是
2CO32-。下列叙述正确的是| A.放电时CO32-向正极移动 |
| B.随着反应的进行,CO32-在不断消耗 |
C.负极反应为H2+CO32--2e- H2O+CO2 H2O+CO2 |
| D.当该电池产生的水蒸气折算成标准状况下的体积为22.4 L时,转移电子4 mol |
您最近半年使用:0次

 的电离:
的电离:
 和
和 的混合溶液中:
的混合溶液中: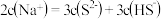
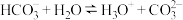
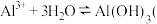 胶体
胶体