某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
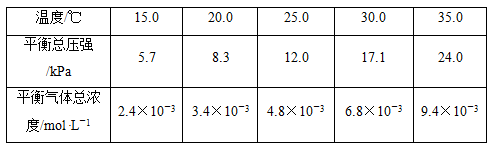
(1)可以判断该分解反应已经达到平衡的是________ (填字母序号)。
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)根据表中数据,列式计算25.0 ℃时的分解平衡常数:____________________________ 。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将________ (填“增加”“减少”或“不变”)。
(4)氨基甲酸铵分解反应的焓变ΔH____ 0(填“>”“=”或“<”,下同),熵变ΔS____ 0。
 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)实验测得不同温度下的平衡数据列于下表:

(1)可以判断该分解反应已经达到平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)根据表中数据,列式计算25.0 ℃时的分解平衡常数:
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将
(4)氨基甲酸铵分解反应的焓变ΔH
更新时间:2017-11-16 10:15:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在一固定容积的密闭容器中,进行如下反应:C(s)+H2O(g) CO(g)+H2(g)。
CO(g)+H2(g)。
(1)若容器体积为2 L,反应10秒后氢气的质量增加0.4 g,则该时间内一氧化碳的反应速率为___ mol/(L•s)。
(2)该反应达到平衡状态的标志是___ (选填编号)。
A.压强不变 B.v正(H2)=v正(H2O)
C.c(CO)不变 D.c(H2O)=c(CO)
(3)若增加炭的量,则正反应速率___ (选填“增大”、“减小”、不变);若增大压强,化学平衡向___ 移动(选填“正向”、“逆向”或“不”)。
(4)若升高温度,平衡向正向移动,则正反应方向为___ 反应。(填“吸热”或“放热”)
 CO(g)+H2(g)。
CO(g)+H2(g)。(1)若容器体积为2 L,反应10秒后氢气的质量增加0.4 g,则该时间内一氧化碳的反应速率为
(2)该反应达到平衡状态的标志是
A.压强不变 B.v正(H2)=v正(H2O)
C.c(CO)不变 D.c(H2O)=c(CO)
(3)若增加炭的量,则正反应速率
(4)若升高温度,平衡向正向移动,则正反应方向为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列属于可逆反应的是_______ 。
A.氯化钠溶解与结晶析出
B.氯气溶于水
C.电解水生成H2、O2与H2在O2中燃烧生成H2O
D.反应物和生成物相反的反应
E.SO2被氧气氧化成SO3
F.H2和I2在高温下边化合边分解
G.品红溶液通入SO2褪色,加热后又恢复红色
H.Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
I.SO2+Br2+2H2O=H2SO4+2HBr与2HBr+H2SO4(浓)= Br2+SO2↑+2H2O
A.氯化钠溶解与结晶析出
B.氯气溶于水
C.电解水生成H2、O2与H2在O2中燃烧生成H2O
D.反应物和生成物相反的反应
E.SO2被氧气氧化成SO3
F.H2和I2在高温下边化合边分解
G.品红溶液通入SO2褪色,加热后又恢复红色
H.Pb+PbO2+2H2SO4
 2PbSO4+2H2O
2PbSO4+2H2OI.SO2+Br2+2H2O=H2SO4+2HBr与2HBr+H2SO4(浓)= Br2+SO2↑+2H2O
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氨是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)下列关于氨气的叙述中,错误的是_____。
(2)工业上合成氨气的化学方程式是:_____ 。
(3)下列表示合成氨反应的速率中,反应最快的是_____。
(4)在一个恒温恒容的密闭容器中进行合成氨反应,下列证据能判断反应已达平衡状态的是_____。
(5)在一个密闭容器中进行的合成氨反应,达到平衡后改变一个条件,一段时间又达到平衡,此时测得氨气的浓度增大。下列可能的原因是_____。
(1)下列关于氨气的叙述中,错误的是_____。
| A.氨气遇浓盐酸冒白烟 | B.氨气在一定的条件下能被氧气氧化 |
| C.氨气能使干燥的蓝色石蕊试纸变红色 | D.氨气能使酚酞试液变红色 |
(3)下列表示合成氨反应的速率中,反应最快的是_____。
A.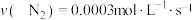 | B. |
C. | D. |
A.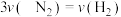 |
| B.气体密度不再变化 |
C.每消耗 就同时消耗 就同时消耗 |
| D.混合气体的平均摩尔质量不再变化 |
| A.升高温度 | B.降低温度 | C.增大容器体积 | D.缩小容器体积 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上采用乙苯脱氢制取苯乙烯,最新研究得出乙苯脱氢有两种路径(如图所示)。一种是先脱亚甲基上的H原子,再脱甲基上的H原子,中间产物为1-苯乙基,如图PATH(I)。另一种是先脱甲基上的H原子,再脱亚甲基上的H原子,中间产物为2-苯乙基,如图PATH(II)。工业上在恒容容器中进行反应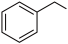 (g)
(g)
 (g)+H2(g) ∆H>0,加入高温水蒸气的目的是
(g)+H2(g) ∆H>0,加入高温水蒸气的目的是____ ,若在恒压容器中进行该反应,加入高温水蒸气还可以起到的作用是____ 。

 (g)
(g)
 (g)+H2(g) ∆H>0,加入高温水蒸气的目的是
(g)+H2(g) ∆H>0,加入高温水蒸气的目的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】改变温度对平衡常数的影响
(1)改变温度可以使化学平衡发生移动,化学平衡常数也会发生改变,通过分析以下两个反应,总结出温度对化学平衡常数的影响规律。
①N2(g)+3H2(g) 2NH3(g)
2NH3(g)
化学平衡常数K1=_______ ,升温化学平衡向逆向移动,K1______ (填“增大”或“减小”,下同),ΔH____ 0(填“>”或“<”,下同)。
②CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
化学平衡常数K2=________ ,升温化学平衡向正向移动,K2________ ,ΔH________ 0。
(2)判断反应的热效应
①升高温度:K值增大→正反应为________ 反应;K值减小→正反应为________ 反应。
②降低温度:K值增大→正反应为________ 反应;K值减小→正反应为________ 反应。
(1)改变温度可以使化学平衡发生移动,化学平衡常数也会发生改变,通过分析以下两个反应,总结出温度对化学平衡常数的影响规律。
①N2(g)+3H2(g)
 2NH3(g)
2NH3(g)化学平衡常数K1=
②CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)化学平衡常数K2=
(2)判断反应的热效应
①升高温度:K值增大→正反应为
②降低温度:K值增大→正反应为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】绿色能源是未来能源发展的方向,积极发共氢能,是实现“碳达峰、碳中和”的重要举措。回答下列问题:
(1)工业上常用甲俒水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ.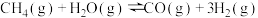
Ⅱ.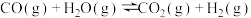
下列操作中,能提高 平衡转化率的是_______(填标号)。
平衡转化率的是_______(填标号)。
(2)在一定条件下,向密闭容器中充入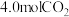 和
和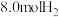 ,发生反应
,发生反应 。测得相同时间内,
。测得相同时间内, 的转化率随温度的变化如图1所示(虚线表示
的转化率随温度的变化如图1所示(虚线表示 的平衡转化率随温度的变化);速率常数的对数
的平衡转化率随温度的变化);速率常数的对数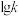 与温度的倒数
与温度的倒数 之间的关系如图2所示。
之间的关系如图2所示。
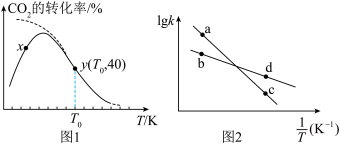
①由上图判断,该反应为_______ (填“吸热”或“放热”)反应。
② 时,该反应的平衡常数
时,该反应的平衡常数
_______ (对于反应 ,
,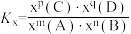 ,x为物质的量分数)。
,x为物质的量分数)。
③y点达到平衡后,保持恒温、恒压,再向该容器中充入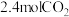 和
和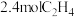 ,平衡将
,平衡将_______ (填“逆向移动”“正向移动”或“不移动”)。
(3)已知该反应的速率方程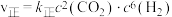 ,
, ,
, 、
、 是速率常数。升高温度时,
是速率常数。升高温度时,
_______ (填“增大”、“减小”或“不变”);图2中a、b、c、d分别代表x点、y点的速率常数,其中_______ 点表示x点的 。
。
(1)工业上常用甲俒水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ.
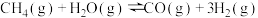
Ⅱ.
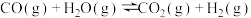
下列操作中,能提高
 平衡转化率的是_______(填标号)。
平衡转化率的是_______(填标号)。A.增加 用量 用量 | B.恒温恒压下通入惰性气体 |
C.移除 | D.加入催化剂 |
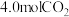 和
和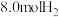 ,发生反应
,发生反应 。测得相同时间内,
。测得相同时间内, 的转化率随温度的变化如图1所示(虚线表示
的转化率随温度的变化如图1所示(虚线表示 的平衡转化率随温度的变化);速率常数的对数
的平衡转化率随温度的变化);速率常数的对数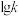 与温度的倒数
与温度的倒数 之间的关系如图2所示。
之间的关系如图2所示。
①由上图判断,该反应为
②
 时,该反应的平衡常数
时,该反应的平衡常数
 ,
,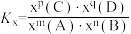 ,x为物质的量分数)。
,x为物质的量分数)。③y点达到平衡后,保持恒温、恒压,再向该容器中充入
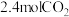 和
和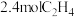 ,平衡将
,平衡将(3)已知该反应的速率方程
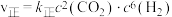 ,
, ,
, 、
、 是速率常数。升高温度时,
是速率常数。升高温度时,
 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(Ⅰ)已知在448℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为___ ;
(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___ 。
(2)该反应为___ 反应(填“吸热”或“放热”)。
(3)能判断该反应达到化学平衡状态的依据是___ 。
A.容器中压强不变 B.混合气体中C(CO)不变
C.V(H2)正=V(H2O)逆 D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)•C(H2)=c(CO)•c(H2O),判断此时温度为___ ℃。
 2HI(g)的平衡常数K1为49,则该温度下反应2HI(g)
2HI(g)的平衡常数K1为49,则该温度下反应2HI(g) H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中C(CO)不变
C.V(H2)正=V(H2O)逆 D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:C(CO2)•C(H2)=c(CO)•c(H2O),判断此时温度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______ (用K1、K2表示)。500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol·L-1)分别为0.8、0.1、0.3、0.15,则此时v正_______ v逆(填“>”、“=”或“<”)。
(2)在3L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

①当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______ 。
②当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_______ 。
Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)⇌CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。

(3)p1_______ p2(填“>”、“<”或“=”),理由是_______ 。
(4)该甲醇合成反应在A点的平衡常数K=_______ (用a和V表示)。
(5)该反应达到平衡时,反应物转化率的关系是CO_______ H2。(填“>”、“<”或“=”)
(6)下列措施中能够同时满足增大反应速率和提高CO转化率的是_______ (填字母)。
A.使用高效催化剂
B.降低反应温度
C.增大体系压强
D.不断将CH3OH从反应混合物中分离出来
E.增加等物质的量的CO和H2
| 化学反应 | 平衡常数 | 温度/℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)⇌CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)⇌H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) | K3 | ||
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(2)在3L容积可变的密闭容器中发生反应②,已知c(CO)—反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

①当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
②当曲线Ⅰ变为曲线Ⅲ时,改变的条件是
Ⅱ.利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)⇌CH3OH(g)。一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如下图所示。

(3)p1
(4)该甲醇合成反应在A点的平衡常数K=
(5)该反应达到平衡时,反应物转化率的关系是CO
(6)下列措施中能够同时满足增大反应速率和提高CO转化率的是
A.使用高效催化剂
B.降低反应温度
C.增大体系压强
D.不断将CH3OH从反应混合物中分离出来
E.增加等物质的量的CO和H2
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在某一容积为5 L的密闭容器内,加入0.2mol 的CO和0.2mol的H2O(g),在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。

(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速率为__ mol·(L·min)-1;反应平衡时c(H2)=__ mol·L-1。
(2)判断该反应达到平衡的依据是________(填序号)。
 CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
CO2(g)+H2(g),反应放出热量。反应中CO2的浓度随时间变化的情况如下图所示。
(1)根据图中数据,从反应开始至达到平衡时,CO的化学反应速率为
(2)判断该反应达到平衡的依据是________(填序号)。
| A.CO减少的化学反应速率和CO2减少的化学反应速率相等 | B.CO、H2O、CO2、H2的浓度都相等 |
| C.CO、H2O、CO2、H2的浓度都不再发生变化 | D.正、逆反应速率都为零 |
您最近半年使用:0次



