电导率是衡量电解质溶液导电能力大小的物理量。常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示。下列说法正确的( )
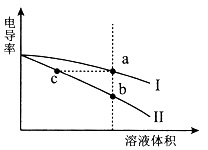

| A.I表示NaOH溶液加水稀释过程中溶液电导率的变化 |
| B.a、b、c三点溶液的pH:b>c>a |
| C.将a、b两点溶液混合,所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D.a点水电离出的n(H+)大于c点水电离出的n(H+) |
更新时间:2018-03-13 10:05:25
|
相似题推荐
单选题
|
适中
(0.65)
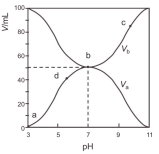
【推荐1】25℃时,将浓度均为0.1mol/L、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL (溶液体积有简单叠加),Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是

| A.Ka(HX)的值与Kb(NH3·H2O)的值相等 |
B.c、d两点,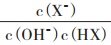 值相等 值相等 |
| C.a→d点过程中,存在c (X-) =c (NH4+) |
| D.b点,c(NH4+)+c (HX) = 0.05mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电导率是衡量电解质溶液导电能力大小的物理量。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·L-1的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是


| A.①表示的是 KOH溶液滴定盐酸溶液 |
| B.A点的溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L |
| C.水电离的c(OH-):C点小于A点 |
| D.B点的溶液中有:c(CH3COO-)>c(K+)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有1mL0.1mol·L-1AgNO3溶液的试管中滴加3滴0.1mol·L-1NaCl溶液,再向其中滴加一定量0.1mol·L-1KI溶液 | 先有白色沉淀生成,后又产生黄色沉淀 | 常温下,溶度积常数:Ksp(AgCl)>Ksp(AgI) |
| B | 其他条件不变,压缩2HI(g) I2(g)+H2(g) I2(g)+H2(g) | 混合气体颜色变深 | 平衡向生成I2(g)的方向移动 |
| C | 用等体积pH=3的HA和HB两种酸溶液分别与足量的Fe反应 | HA放出的氢气多且速率快 | HA酸性比HB弱 |
| D | 向5mLFeCl3溶液中加入5滴同浓度的KI溶液,再加入几滴KSCN溶液 | 溶液显红色 | FeCl3与KI的反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列有关电解质溶液的说法中不正确的是
A.向0.1mol⋅L-1CH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中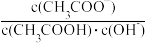 减小 减小 |
C.向盐酸中加入氨水至中性,溶液中 =1 =1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】MOH和ROH两种一元碱,常温下向其水溶液中加水稀释,pH变化如图。下列说法正确的是


| A.在X点时,由H2O电离出的c(H+)相等,c(M+)=c(R+) |
| B.稀释前,c(ROH)=10c(MOH) |
C.稀释ROH溶液过程中 减小 减小 |
| D.稀释ROH溶液过程中,溶液中所有微粒浓度均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将浓度为0.1mol·L-1的CH3COOH溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.Ka(CH3COOH) | C.c(CH3COO-) | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数
从以上表格中判断下列说法正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A.在冰醋酸中这四种酸都完全电离 |
| B.在冰醋酸中高氯酸是这四种酸中最弱的酸 |
| C.在冰醋酸中硫酸的电离方程式为H2SO4=2H+ +SO42- |
| D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下0.1 mol·L-1的二元酸H2A溶液的pH=4.0。在标准状况下,将2.24 L H2A气体通入到100 mL 1.5 mol·L-1NaOH溶液中,充分反应后(假设溶液体积不发生变化),下列关系式不正确的是
| A.c(Na+)+c(H+)= 2c(A2-)+c(OH-)+c(HA-) |
| B.c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
| C.c(Na+)>c(HA-)>c(A2-)>c(OH-)>c(H+) |
| D.c(A2-)+c(HA-)+c(H2A)="1.0" mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,用1mol•L-1的NaOH溶液调节0.10L1mol•L-1H2C2O4溶液的pH,溶液中H2C2O4、HC2O 及C2O
及C2O 的物质的量浓度变化如图所示。
的物质的量浓度变化如图所示。

下列说法错误的是
 及C2O
及C2O 的物质的量浓度变化如图所示。
的物质的量浓度变化如图所示。
下列说法错误的是
| A.H2C2O4的Ka1=1×10-4 |
B.Y点:c(Na+)<3c(C2O ) ) |
| C.Z点:由水电离出的H+浓度约为10-4mol•L-1 |
D.1mol•L-1的NaHC2O4溶液中:c(Na+)>c(HC2O )>c(C2O )>c(C2O ) ) |
您最近一年使用:0次

 溶液便可鉴别亚硝酸钠和食盐
溶液便可鉴别亚硝酸钠和食盐 与足量氨水反应的离子方程式
与足量氨水反应的离子方程式 

 减小
减小 一元弱酸
一元弱酸 中逐滴加入
中逐滴加入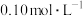 的
的 溶液,溶液
溶液,溶液 随加入
随加入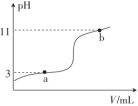

 时,
时,