向盛有1 mL 0.1 mol/L MgCl2溶液的试管中滴加1 mL 0.2 mol/L氨水,观察到有白色沉淀生成,再滴加1 mL 0.1 mol/L FeCl3溶液,发现白色沉淀转化为红褐色沉淀。由以上现象可以推知,下列叙述正确的是
| A.生成白色沉淀的离子方程式是:Mg2++2OH-=Mg(OH)2↓ |
| B.白色沉淀转化为红褐色沉淀的离子方程式是:3Mg(OH)2+2Fe3+==3Mg2++2Fe(OH)3 |
| C.上述实验说明Mg(OH)2的Ksp小于Fe(OH)3的Ksp |
| D.最后所得的溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(Mg2+)>c(Fe3+)>c(OH-)>c(H+) |
2011·浙江宁波·一模 查看更多[2]
更新时间:2016-12-09 01:43:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列相关实验能达到预期目的的是
| 相关实验 | 预期目的 | |
| A | 不同温度下,取0.1 mol·L-1KI溶液,向其中先加入0.1 mol·L-1的硫酸,再加入淀粉溶液,发生反应4H++O2+4I- =2I2+2H2O | 探究溶液出现蓝色的时间与温度的关系 |
| B | 相同温度下,测定等浓度的Na2CO3和CH3COONa的pH | 比较H2CO3和CH3COOH酸性强弱 |
| C | 在加热搅拌的条件下向溶液中加入足量的MgCO3,过滤后,再向滤液中加入适量盐酸 | 除去MgCl2酸性溶液中的Fe3+ |
| D | 向5mL0.1 mol·L-1AgNO3溶液中滴几滴0.1mol·L-1NaCl溶液,生成白色沉淀,再滴加几滴0.1 mol·L-1KI溶液,观察沉淀颜色变化 | 探究AgCl沉淀能否转化为 AgI沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】根据下列图示所得出的结论正确的是
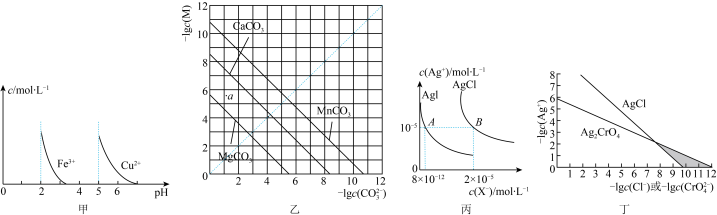

| A.由图甲可知,除去CuSO4溶液中的Fe3+可加入适量NaOH溶液调节pH至4左右 |
B.图乙是一定温度下三种碳酸盐的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO ) ) |
| C.图丙是室温下AgCl和AgI的饱和溶液中离子浓度的关系曲线,该温度下反应AgCl(s)+I-(aq)⇌AgI(s)+Cl-(aq)的平衡常数K=2.5×106 |
| D.图丁是室温下AgCl和Ag2CrO4的沉淀溶解平衡曲线,阴影区域中的点可以同时生成Ag2CrO4沉淀和AgCl沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验方案能达到实验目的的是
| 实验目的 | 实验方案 | |
| A | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| B | 证明酸性条件下H2O2氧化性强于I2 | 向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝;再加入10%的H2O2溶液,溶液立即变蓝色 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明Mg(OH)2沉淀可转化为Fe(OH)3沉淀 | 向2 mL1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式正确的是
A.向NaClO溶液中滴加少量 溶液: 溶液: |
B.向 溶液中加入NiO粉末生成红褐色沉淀: 溶液中加入NiO粉末生成红褐色沉淀: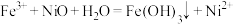 |
C.向 溶液中加入等体积的 溶液中加入等体积的 溶液,产生白色沉淀: 溶液,产生白色沉淀: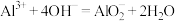 |
D.向含 的稀硫酸中加入铜粉得到蓝色溶液: 的稀硫酸中加入铜粉得到蓝色溶液: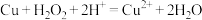 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学是以实验为基础的科学。下列实验操作正确且能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 检验丙烯醛中是否含有碳碳双键 | 向丙烯醛溶液中滴加溴水,溶液褪色 |
| B | 比较Ksp(CuS)和Ksp(ZnS)的大小 | 向浓度均为0.1mol•L-1的CuSO4和ZnSO4的混合溶液中滴加Na2S溶液,观察现象 |
| C | 检验溶液中是否含有K+ | 用洁净的铂丝蘸取某溶液在酒精灯火焰上灼烧,观察火焰颜色 |
| D | 判断Fe(NO3)2固体是否变质 | 取少量固体溶于蒸馏水,滴加少量稀硫酸,再滴入KSCN溶液,溶液变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
| B | 室温下,向NaCl和KI混合溶液中滴加AgNO3溶液,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的弱 |
| D | 室温下,用pH试纸测得:0.1mol·L–1Na2SO3溶液的pH约为10;0.1mol·L–1NaHSO3溶液的pH约为5 | HSO 结合H+的能力比SO 结合H+的能力比SO 的强 的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验中物质的颜色变化与氧化还原反应无关 的是
| A.将Na2O2粉末露置在空气中,固体由淡黄色变为白色 |
B.向 悬浊液中滴加FeCl3溶液,固体由白色变为红褐色 悬浊液中滴加FeCl3溶液,固体由白色变为红褐色 |
| C.向K2Cr2O7酸性溶液中加入乙醇,溶液由橙色变为绿色 |
| D.向KI溶液中通入少量氯气,溶液由无色变为棕黄色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验中,对应的操作、现象及实验原理或结论均正确的是
| 实验目的 | 操作和现象 | 实验原理或结论 | |
| A | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 向1mLlmol·L-1MgCl2溶液中滴加2滴2mol·L-1NaOH溶液,生成白色沉淀;再滴加2滴1mol·L-1'FeCl3溶液,白色沉淀变成红褐色沉淀 | 3Mg(OH)2(s)+2Fe3+(aq) 2Fe(OH)3(s)+3Mg2+(aq) 2Fe(OH)3(s)+3Mg2+(aq) |
| B | 比 较 HClO 和CH3COOH 的酸性 | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 酸越弱,酸根离子水解程度越大,其盐溶液碱性越强 |
| C | 提纯混有少量硝酸钾的氯化钠固体 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
| D | 检验某溶液中是否含有SO42- | 向该溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,将0.1mol·L-1AgNO3溶液和0.1mol·L-1NaCl溶液等体积充分混合,一段时间后过滤,得滤液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为0.1mol·L-1的Na2S溶液和Na2SO4溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列说法正确的是
| A.0.1mol·L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) |
B.过滤后所得清液中一定存在:c(Ag+)= 且c(Ag+)> 且c(Ag+)> |
| C.沉淀b中滴加氨水发生反应的离子方程式:AgCl+2NH3∙H2O=[Ag(NH3)2]++Cl-+2H2O |
| D.从实验现象可以得出该温度下Ksp(Ag2S)>Ksp(Ag2SO4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向苯酚钠溶液中滴加NaHSO3溶液,溶液变浑浊 | 苯酚酸性弱于H2SO3酸性 |
| B | 向AgNO3溶液中逐滴加入浓度均为0.05 mol/L的NaI、NaCl混合溶液,有黄色沉淀生成 |  |
| C | 向FeCl3溶液中加入Cu粉,Cu粉溶解 | Cu的还原性大于Fe |
| D | 向1 mL0.1 mol/LKI溶液中加入0.1 mol/L的FeCl3溶液5 mL,振荡,用苯萃取2~3次后,取下层溶液滴加5滴KSCN溶液,出现血红色 | 2Fe3++2I-=2Fe2++I2有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 )为原料制备
)为原料制备 的流程如下 :
的流程如下 :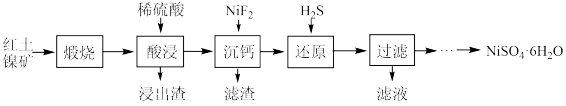
 、CaO和
、CaO和 和
和 产生。
产生。 、
、 、
、
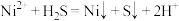
 是可以循环使用的物质
是可以循环使用的物质 浓度均为
浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中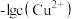 和
和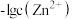 与
与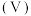 的关系如图所示[已知:
的关系如图所示[已知: ,
,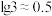 ]。下列说法正确的是
]。下列说法正确的是
 :
: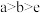

 为滴定
为滴定 点纵坐标约为33.9
点纵坐标约为33.9

