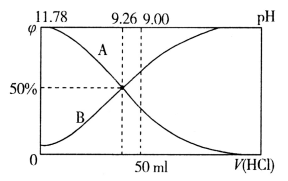
常温下向100mL 0.2mol·L-1的氨水中逐滴加入0.2mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O的物质的量分数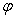 与加入盐酸的体积V的关系如图所示,下列说法错误的是
与加入盐酸的体积V的关系如图所示,下列说法错误的是
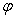 与加入盐酸的体积V的关系如图所示,下列说法错误的是
与加入盐酸的体积V的关系如图所示,下列说法错误的是
| A.表示NH3·H2O物质的量分数变化的曲线是A |
| B.NH3·H2O的电离常数为10-4.74 mol·L-1 |
| C.当加入盐酸体积为50ml时,溶液中c(NH4+)-c(NH3·H2O)=2×(10-5-10-9)mol·L-1 |
| D.pH=9.26时的溶液中,NH4+的水解程度等于NH3·H2O的电离程度 |
更新时间:2018-04-28 09:56:59
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 时,配制一组
时,配制一组 的混合溶液,溶液中
的混合溶液,溶液中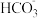 、
、 、
、 、
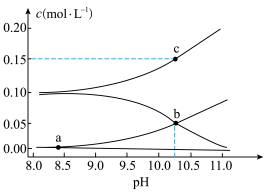
、 的浓度与溶液pH的关系曲线如下图所示。下列说法正确的是
的浓度与溶液pH的关系曲线如下图所示。下列说法正确的是
 时,配制一组
时,配制一组 的混合溶液,溶液中
的混合溶液,溶液中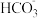 、
、 、
、 、
、 的浓度与溶液pH的关系曲线如下图所示。下列说法正确的是
的浓度与溶液pH的关系曲线如下图所示。下列说法正确的是 
A.该温度下, 的电离平衡常数 的电离平衡常数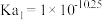 |
B.a点: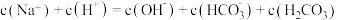 |
C.b点: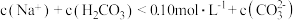 |
D.向c点所表示的溶液中滴加等体积 的NaOH溶液: 的NaOH溶液: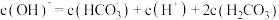 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下向90mL蒸馏水中滴入10mL2mol/LHA溶液,已知溶液中的氢离子浓度c(H+)和温度随HA溶液体积变化曲线如图所示,下列说法不正确的是
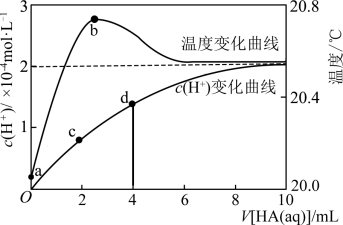

A.常温下 |
B. 过程中温度升高是由于 过程中温度升高是由于 电离放热 电离放热 |
C.在d点时加入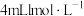 的 的 溶液时存在 溶液时存在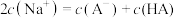 |
D.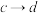 过程中水的电离程度逐渐减小 过程中水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】向 时,体积均为20mL、浓度均为
时,体积均为20mL、浓度均为 的两种酸HX、HY溶液中分别滴加
的两种酸HX、HY溶液中分别滴加 的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
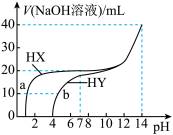
 时,体积均为20mL、浓度均为
时,体积均为20mL、浓度均为 的两种酸HX、HY溶液中分别滴加
的两种酸HX、HY溶液中分别滴加 的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是

A.HX与NaOH溶液反应的离子方程式为: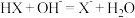 |
B. 的数量级约为 的数量级约为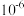 |
C.b点时: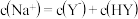 |
D.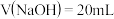 时,两种反应后的溶液中 时,两种反应后的溶液中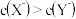 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】苯甲酸钠(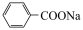 ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于 。已知25℃时,HA的
。已知25℃时,HA的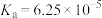 ,H2CO3的
,H2CO3的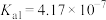 ,
, 。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是
。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是
注:温度为25℃,不考虑饮料中其他成分
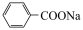 ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于 。已知25℃时,HA的
。已知25℃时,HA的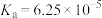 ,H2CO3的
,H2CO3的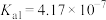 ,
, 。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是
。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO2气体。下列说法正确的是注:温度为25℃,不考虑饮料中其他成分
| A.充CO2的饮料比不充的抑菌能力高 |
B.提高 CO2充气压力,饮料中 不变 不变 |
C.当pH为5.0时,饮料中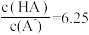 |
D.碳酸饮料中各种粒子的浓度关系为: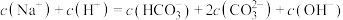 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,用pH=m的盐酸滴定20mlpH=n的MOH溶液,且m+n=14,混合溶液的pH与盐酸体积(V)的关系如图所示。下列说法正确的是
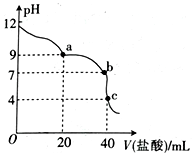

| A.Kb(MOH)的数量级为10—11 | B.由c点可算得m=14/3 |
| C.a点: c(Cl-)>c(M+)>(OH-)>c(H+) | D.b点溶液呈中性,此时c(Cl-)=c(M+) |
您最近一年使用:0次

 的
的 、
、 的混合溶液中存在:
的混合溶液中存在: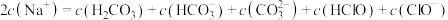
 碳酸电离常数为
碳酸电离常数为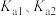 ,则
,则 的碳酸钠溶液中,
的碳酸钠溶液中,
 溶液中加入少量
溶液中加入少量 固体,溶液中
固体,溶液中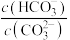 值减小
值减小 的醋酸溶液和
的醋酸溶液和 的硫酸溶液,
的硫酸溶液, 约等于20倍
约等于20倍


