实验室中有6瓶失去标签的白色固体:纯碱、氢氧化镁、氯化钡、硫酸铝、硫酸氢钠、氯化钾。除蒸馏水、试管和胶头滴管外,无其他任何试剂和仪器。某学生通过以下实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,有一支试管中的现象和其他5支明显不同,此试管中的现象是________________________ ,
据此现象鉴别出的一种物质是__________ 。
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三种物质的化学式依次是________________ 。
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为__________________ 。
③在两两混合时,能最终确定B、E成分的实验现象及结论是_____________________ 。
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式为________ ,其溶液显酸性的原因是___________________ 。
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,有一支试管中的现象和其他5支明显不同,此试管中的现象是
据此现象鉴别出的一种物质是
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三种物质的化学式依次是
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为
③在两两混合时,能最终确定B、E成分的实验现象及结论是
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式为
2019高三·全国·专题练习 查看更多[2]
更新时间:2018-09-12 20:48:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】高中化学课本必修一中出现的部分物质间的转化关系如下图所示(部分物质已省略。已知A→B是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
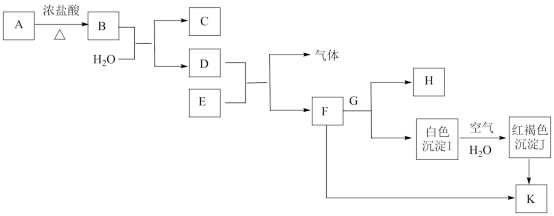
(1)E和H的化学式为:E___________ ;H___________ 。
(2)检验K溶液中阳离子的试剂是___________ 。若K中含有F的杂质,应加入___________ (填化学式)除杂。
(3)I转化为J的化学方程式为___________ 。
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
(5)当前,新冠病毒变异毒株奥密克戎来势汹汹,化学消毒剂在疫情防控中起着重要作用。
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为___________ 。
②C可以杀菌、消毒,但不稳定,难以保存,原因是___________ (用化学方程式表示)。
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是___________ 。
④ 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为___________ 。

(1)E和H的化学式为:E
(2)检验K溶液中阳离子的试剂是
(3)I转化为J的化学方程式为
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是___________(填字母序号)。
A.胶体L的分散质粒子直径为 | B.胶体L比K的饱和溶液颜色深 |
| C.胶体L是均一的分散系 | D.胶体L具有丁达尔效应 |
①目前,很多自来水厂用氯气来杀菌、消毒。A→B的离子反应方程式为
②C可以杀菌、消毒,但不稳定,难以保存,原因是
③将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是
④
 为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠(
为国际公认的高效安全灭菌消毒剂之一、常温下,亚氯酸钠( )固体与B反应可得到
)固体与B反应可得到 和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
和NaCl,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】单质A、B、C在一定条件下,可以按下面的流程进行反应。已知单质A、B常温下分别为无色气体和黄绿色气体,单质C是常见的金属,D的水溶液常温下能与单质C反应生成F和单质A。
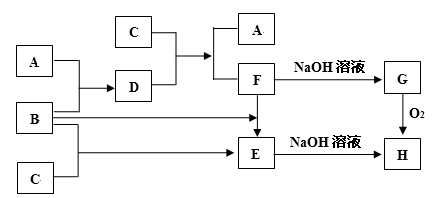
请完成下列填空:
(1)写出单质B的化学式_____ ,D物质的电子式_____ 。
(2)写出E→H的化学方程式___________ 。
(3)写出D+C→F+A的离子方程式____________ 。

请完成下列填空:
(1)写出单质B的化学式
(2)写出E→H的化学方程式
(3)写出D+C→F+A的离子方程式
您最近一年使用:0次
【推荐3】短周期主族元素V、W、X、Y、Z的原子序数依次增大。由这五种元素组成的九种物质中,A、B、C是气体单质,其余均为化合物;A是黄绿色气体,甲是能使湿润的红色石蕊试纸变蓝的无色气体,乙是人体中 含量最大的化合物,丙是淡黄色固体。它们的转化关系如图所示。回答下列问题:

(1)甲的化学式为___________ 。
(2)乙和丙反应的化学方程式为___________ 。
(3)气体单质B的电子式为___________ 。
(4)元素W、X、Y、Z的氢化物中熔点最高的是___________ 。
(5)实验室用高锰酸钾制备气体A的离子反应方程式为___________ 。
(6)在微电子工业中,甲的水溶液可作刻蚀剂V2X2的清除剂,所发生反应的产物不污染环境,该反应的化学方程式为___________ 。

(1)甲的化学式为
(2)乙和丙反应的化学方程式为
(3)气体单质B的电子式为
(4)元素W、X、Y、Z的氢化物中熔点最高的是
(5)实验室用高锰酸钾制备气体A的离子反应方程式为
(6)在微电子工业中,甲的水溶液可作刻蚀剂V2X2的清除剂,所发生反应的产物不污染环境,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D均为中学化学中的常见物质,它们有如图所示转化关系。A是一种常见金属,它可以与氢氧化钠溶液反应放出氢气。回答下列问题:

(1)写出C的化学式:_______________ 。
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:_____________________________ 。
(3)写出D→B的化学方程式:__________________________________ 。
(4)写出A和NaOH溶液反应的离子方程式:___________________________________ 。

(1)写出C的化学式:
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:
(3)写出D→B的化学方程式:
(4)写出A和NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】金属铝在酸性或碱性溶液中均可与 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:
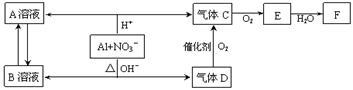
已知:气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题
(1)A和B两溶液混合产生白色沉淀,产生该沉淀的离子反应方程式为_____________________ 。
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的电子式__________ 。
(3)完成并配平下列离子方程式:Al+ +OH-+H2O——
+OH-+H2O——__________ +_______ 。
(4)Al与 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是________ 。
 发生氧化还原反应,转化关系如下:
发生氧化还原反应,转化关系如下:
已知:气体D和F反应可生成盐,气体D和A溶液反应生成白色沉淀。
请回答下列问题
(1)A和B两溶液混合产生白色沉淀,产生该沉淀的离子反应方程式为
(2)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C、E转化为无毒的气态单质,该单质的电子式
(3)完成并配平下列离子方程式:Al+
 +OH-+H2O——
+OH-+H2O——(4)Al与
 在酸性条件下反应,Al与被还原的
在酸性条件下反应,Al与被还原的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E是1—18号元素组成的中学常见的物质,存在如图所示的转化关系(部分生成物和反应条件略去,反应①在常温下进行)
已知: Al3++3AlO2-+6H2O=4Al(OH)3↓
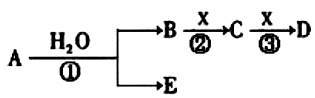
(1)若A为单质,X为一种无色无味气体,且B与D能反应生成C,则A为__________ ;B与D反应的离子方程式为____________________ ;
(2)若A为化合物, X为一种常见的黑色固体单质,且B与D能反应生成C,则A与水反应的离子方程式为:____________________ ;
(3)若D为白色胶状沉淀,与A摩尔质量相等,则反应②的离子方程式为___________________ ;
已知: Al3++3AlO2-+6H2O=4Al(OH)3↓

(1)若A为单质,X为一种无色无味气体,且B与D能反应生成C,则A为
(2)若A为化合物, X为一种常见的黑色固体单质,且B与D能反应生成C,则A与水反应的离子方程式为:
(3)若D为白色胶状沉淀,与A摩尔质量相等,则反应②的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。
(1)M在元素周期表中的位置为________________ 。
(2)X与Y按原子个数比2∶1构成的物质的电子式为________________ ;所含化学键类型_________ 。
(3)X+、 Y2-、M2-离子半径大小顺序为_____________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式:______________________________________ 。
Ⅱ.如下图转化关系: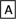
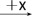
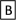
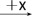
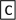
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为_______________________ 。
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为___________ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比2∶1构成的物质的电子式为
(3)X+、 Y2-、M2-离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式:
Ⅱ.如下图转化关系:
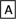
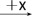
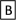
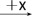
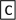
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】
(1)AgNO3的水溶液呈___ (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):____________________ ;
(2)向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是有气泡,并有白色沉淀生成,有关的离子方程式________________________ .
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离反应的平衡常数值为________________ (已知:N2H4+H+ N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为_________ 。
(4)通过控制溶液的pH对工业废水中的金属离子进行分离。图3是某些金属氢氧化物在不同浓度和pH时的沉淀——溶解图象,图中直线上的点表示平衡状态。当溶液中的离子浓度小于1×10-5 mol·L-1时,认为该离子沉淀完全。

①相同条件下,Fe(OH)3、Al(OH)3、Cr(OH)3三种物质的溶度积常数最大的是_______ ,图中A、B、C三点中表示Fe(OH)3的沉淀速率大于溶解速率的是______________ 。
②由图可得Fe(OH)2的溶度积的值为__________________________ 。
(1)AgNO3的水溶液呈
(2)向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是有气泡,并有白色沉淀生成,有关的离子方程式
(3)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离反应的平衡常数值为
 N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为(4)通过控制溶液的pH对工业废水中的金属离子进行分离。图3是某些金属氢氧化物在不同浓度和pH时的沉淀——溶解图象,图中直线上的点表示平衡状态。当溶液中的离子浓度小于1×10-5 mol·L-1时,认为该离子沉淀完全。

①相同条件下,Fe(OH)3、Al(OH)3、Cr(OH)3三种物质的溶度积常数最大的是
②由图可得Fe(OH)2的溶度积的值为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钴广泛应用于电池、合金等领域。以钴渣(主要含 和
和 ,还含有
,还含有 、
、 等元素以及
等元素以及 、炭、有机物)为原料制备钴的流程如图所示:
、炭、有机物)为原料制备钴的流程如图所示:
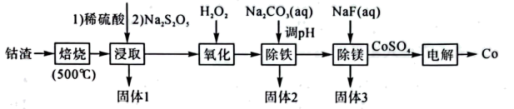
已知:① (焦亚硫酸钠)有强还原性。
(焦亚硫酸钠)有强还原性。
②常温时,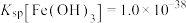 ,
,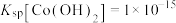 ,
,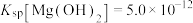 ,
,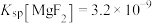 ,
, 。
。
③溶液中离子的浓度小于 可认为已除尽。
可认为已除尽。
回答下列问题:
(1)“焙烧”的目的是___________ 。固体1、固体3的主要成分分别为___________ 、___________ (均填化学式)。
(2) 的作用是
的作用是___________ 。“除铁”过程中发生反应的离子方程式为___________ 。
(3)“氧化”后,测得溶液中 和
和 的物质的量浓度分别为
的物质的量浓度分别为 和
和 ,则常温时“除铁”应控制溶液的
,则常温时“除铁”应控制溶液的 范围为
范围为___________ 。(设加入 溶液时体积变化忽略不计)。
溶液时体积变化忽略不计)。
(4)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图所示。
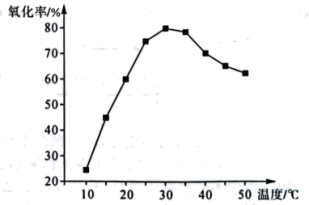
温度在 后,随着温度升高氧化率下降可能的原因是
后,随着温度升高氧化率下降可能的原因是___________ 。
(5)在“除镁”时,若 过低,
过低, 的去除率将会下降,原因是
的去除率将会下降,原因是___________ 。
 和
和 ,还含有
,还含有 、
、 等元素以及
等元素以及 、炭、有机物)为原料制备钴的流程如图所示:
、炭、有机物)为原料制备钴的流程如图所示:
已知:①
 (焦亚硫酸钠)有强还原性。
(焦亚硫酸钠)有强还原性。②常温时,
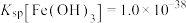 ,
,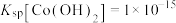 ,
,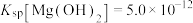 ,
,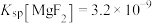 ,
, 。
。③溶液中离子的浓度小于
 可认为已除尽。
可认为已除尽。回答下列问题:
(1)“焙烧”的目的是
(2)
 的作用是
的作用是(3)“氧化”后,测得溶液中
 和
和 的物质的量浓度分别为
的物质的量浓度分别为 和
和 ,则常温时“除铁”应控制溶液的
,则常温时“除铁”应控制溶液的 范围为
范围为 溶液时体积变化忽略不计)。
溶液时体积变化忽略不计)。(4)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图所示。

温度在
 后,随着温度升高氧化率下降可能的原因是
后,随着温度升高氧化率下降可能的原因是(5)在“除镁”时,若
 过低,
过低, 的去除率将会下降,原因是
的去除率将会下降,原因是
您最近一年使用:0次



