在1L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)  M(g)+N(g),所得实验数据如下表,下列说法不正确的是
M(g)+N(g),所得实验数据如下表,下列说法不正确的是
 M(g)+N(g),所得实验数据如下表,下列说法不正确的是
M(g)+N(g),所得实验数据如下表,下列说法不正确的是| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.10 | 0.10 | 0.09 |
| ② | 800 | 0.20 | 0.20 | 0.10 |
| ③ | 900 | 0.10 | 0.15 | a |
| A.正反应为放热反应 |
| B.实验①中,若5min时测得n(M)=0.05mol,则0~5min时间内,用N表示的平均反应速率v(N)= 0.01mol/(L•min) |
| C.实验②中,该反应的平衡常数K=1.0 |
| D.实验③中,达到平衡时,a大于0.06 |
更新时间:2018-12-05 10:25:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】一定温度下,在 2 L 的恒容密闭容器中发生反应 A(g)+2B(g)  3C(g)。反应过程中的部分数据如下表所示:
3C(g)。反应过程中的部分数据如下表所示:
下列说法正确的是
 3C(g)。反应过程中的部分数据如下表所示:
3C(g)。反应过程中的部分数据如下表所示: | n(A) | n(B) | n(C) |
| 0 | 2.0 | 2.4 | 0 |
| 5 | 0.9 | ||
| 10 | 1.6 | ||
| 15 | 1.6 |
| A.0~5 min 用 A 表示的平均反应速率为 0.09 mol·L−1·min−1 |
| B.容器内压强不变,说明反应已达到平衡状态 |
| C.达到平衡状态时 c(C)=0.6 mol·L−1 且不再发生变化 |
| D.若保持容积不变,反应开始时加入反应物的同时再充入少量氦气(不参与反应),该反应达到平衡的时间会延长 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某研究小组欲利用甲烷消除NO2污染,发生反应: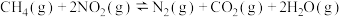 。在2L密闭容器中,控制不同温度,分别加入
。在2L密闭容器中,控制不同温度,分别加入 和
和 ,测得n(CH4)随时间变化的有关实验数据见下表。
,测得n(CH4)随时间变化的有关实验数据见下表。
下列说法正确的是
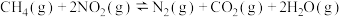 。在2L密闭容器中,控制不同温度,分别加入
。在2L密闭容器中,控制不同温度,分别加入 和
和 ,测得n(CH4)随时间变化的有关实验数据见下表。
,测得n(CH4)随时间变化的有关实验数据见下表。| 组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 30 |
| ① |  | n(CH4) | 1.00 | 0.70 | 0.50 | 0.40 |
| ② |  | n(CH4) | 1.00 | 0.60 | 0.36 | 0.36 |
A.①组中,0~20min内,用NO2表示的反应速率为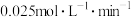 |
| B.由实验数据可知,实验控制的温度:T2<T1 |
| C.反应在20min时,①②组中反应均未达到平衡状态 |
| D.②组在30min时容器内物质的总物质的量仍为3mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关实验现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 用玻璃棒蘸取 盐酸,滴在湿润的pH试纸中央 盐酸,滴在湿润的pH试纸中央 | 试纸变为红色 | 测定盐酸的pH |
| B | 氯化亚铁溶液中有氯化铜杂质,加入铁屑除杂 | 有紫红色金属析出 | 铁能置换Cu单质 |
| C | 将充满 的密闭玻璃球浸泡在热水中 的密闭玻璃球浸泡在热水中 | 红棕色变深 |  的 的 |
| D | 向 和 和 的混合溶液中,加入 的混合溶液中,加入 固体 固体 | 血红色溶液变浅 | 增大 的浓度,平衡逆向移动 的浓度,平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应:2NO2(红棕色) N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器活塞过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器活塞过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是

 N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器活塞过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器活塞过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
| A.b点的操作是拉伸注射器活塞 |
| B.d点:v(正)>v(逆) |
| C.c点与a点相比,n(NO2)增大 |
| D.若不忽略体系温度变化,且没有能量损失,则T(b)<T(c) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】Au/Fe2O3可用作反应CO(g)+H2O CO2(g)+H2(g)的催化剂。对于反应CO(g)+H2O(g)
CO2(g)+H2(g)的催化剂。对于反应CO(g)+H2O(g)  CO2(g)+H2(g),下列有关说法
CO2(g)+H2(g),下列有关说法不正确 的是
 CO2(g)+H2(g)的催化剂。对于反应CO(g)+H2O(g)
CO2(g)+H2(g)的催化剂。对于反应CO(g)+H2O(g)  CO2(g)+H2(g),下列有关说法
CO2(g)+H2(g),下列有关说法| A.加入催化剂Au/Fe2O3,反应的焓变ΔH不变 |
| B.升高温度,反应体系的活化分子百分数增多 |
| C.向固定容积的反应体系中充入氦气,反应速率加快 |
| D.温度不变,增大反应H2O与CO(g)投料比,平衡常数K不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2和CO2: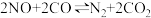
 ,下列对此反应的叙述中正确的是
,下列对此反应的叙述中正确的是
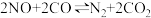
 ,下列对此反应的叙述中正确的是
,下列对此反应的叙述中正确的是| A.改变温度一定加快化学反应速率 |
| B.增大压强能使该反应的化学平衡常数K增大 |
| C.使用光催化剂能增大NO的转化率 |
| D.CO2的生成速率与CO2的分解速率相等,说明该反应达到化学平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】可逆反应2NO2 (g) ⇌N2O4 (g) ΔH= −56.9 kJ·mol−1在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。某同学的部分实验报告如下。
下列说法不正确的是
| 1.向左侧烧杯中加入NH4NO3晶体,甲瓶的红棕色变浅。 2.向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。 |
下列说法不正确的是
| A.甲瓶的红棕色变浅,说明平衡2NO2 (g)⇌N2O4 (g)向正反应方向移动 |
| B.可根据现象判断NH4NO3晶体溶于水吸热,CaO固体溶于水放热 |
| C.甲瓶中反应的化学平衡常数(K)增大 |
| D.乙瓶中由于反应的化学平衡常数(K)改变,使Qc<K,平衡发生移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应: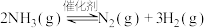 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
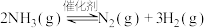 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如下表所示,下列说法正确的是| 编号 | 时间/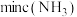 / /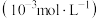 表面积 表面积 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.实验①,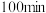 时处于平衡状态 时处于平衡状态 |
B.实验②,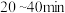 , ,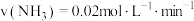 |
C.实验②, 时处于平衡状态, 时处于平衡状态,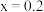 |
D.相比实验①,实验③增加催化剂的表面积,反应③中 的平衡转化率增大 的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
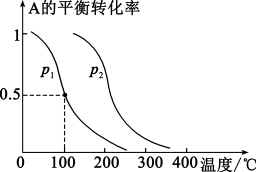
【推荐2】一定条件下,在容积为2 L的密闭容器中充入1 mol A和2 mol B,发生反应A(g) + 2B(g)  C(g) ΔH。A的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
C(g) ΔH。A的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
 C(g) ΔH。A的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
C(g) ΔH。A的平衡转化率与温度、压强的关系如图所示。下列说法错误的是
| A.该反应的正反应是放热反应 |
| B.由图可知:p2 > p1 |
| C.温度为100℃,压强为p1时,若向该容器中投入2 mol A,2 mol B,2 mol C,反应逆向进行 |
| D.升高温度,该反应平衡常数的值减小 |
您最近一年使用:0次



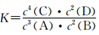

 HCHO(g)+H2 (g),在T℃下,向2 L恒容密闭容器中通入3 mol CH3OH(g),测得HCHO(g)的体积分数随时间变化的关系如图所示。下列有关说法错误的是
HCHO(g)+H2 (g),在T℃下,向2 L恒容密闭容器中通入3 mol CH3OH(g),测得HCHO(g)的体积分数随时间变化的关系如图所示。下列有关说法错误的是


