室温时,测得纯水中的c(H+)=1.0×10-7mol·L-1,则c(OH-)为
| A.1.0× 10-7 mol·L-1 | B.0.1×10-7 mol·L-1 |
| C.1.0×10-14/2.0×10-7 mol·L-1 | D.无法确定 |
更新时间:2019-01-01 08:18:34
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于水的说法中不正确 的是。
| A.水是含极性键的极性分子 |
B.水的电离方程式为 |
| C.纯水中加入少量酸,水的电离受到抑制 |
| D.升高温度,水的电离程度增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列属于强电解质且溶解于水时,电离出的离子能使水的电离平衡向左移动的是
| A.NH3 | B.H2S | C.NaHSO4 | D.MgCl2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】25 ℃时,水的电离达到平衡:H2O H++OH- ΔH>0,下列叙述正确的是
H++OH- ΔH>0,下列叙述正确的是
 H++OH- ΔH>0,下列叙述正确的是
H++OH- ΔH>0,下列叙述正确的是| A.向水中加入少量固体硫酸氢钠,c平(H+)增大,KW不变 |
| B.向水中加入稀氨水,平衡逆向移动,c平(OH-)降低 |
| C.向水中加入少量固体钠,平衡逆向移动,c平(H+)降低 |
| D.将水加热,KW增大,c平(OH-)不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关说法,正确的是( )
| A.电解质溶于水一定放出热量 |
| B.可逆反应在加热时正、逆反应速率都增大 |
| C.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
| D.25℃时,0.01mol/L的氢氧化钠溶液中,水电离的c(H+)与水电离的c(OH-)的积为1.0×10-14 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.Cl2和SO2都具有漂白性,因为二者都有强氧化性 |
| B.铜锌原电池中,锌电极发生氧化反应 |
| C.合成氨生产中将NH3液化分离,可加快正反应速率 |
| D.常温下,pH均为5的盐酸与NH4Cl溶液中,水的电离程度相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是
| A.常温下,2.0×10-4mol/L的盐酸稀释104倍,c(H+)=2.0×10-3mol/L |
| B.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
| C.常温下,pH=3的醋酸溶液中加入少量醋酸钠固体,溶液pH不变 |
| D.将KCl溶液从常温加热至60℃,溶液的pH变小但仍保持中性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】常温下向0.1 HF溶液中加入少量水,下列各项增大的是
HF溶液中加入少量水,下列各项增大的是
①水的电离程度 ②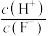 ③
③ ④
④
 HF溶液中加入少量水,下列各项增大的是
HF溶液中加入少量水,下列各项增大的是①水的电离程度 ②
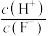 ③
③ ④
④
| A.③④ | B.①②④ | C.①② | D.仅有① |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】常温下,用0.1 mol·L-1的CH3COOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴加V mL CH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是( )
A.Ka= | B.V= | C.Ka= | D.Ka= |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】常温下,酸性:H2CO3>H2S。H2S与足量Na2CO3(aq)反应的离子方程式为
A.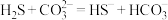 |
B.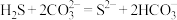 |
C.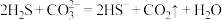 |
D.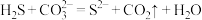 |
您最近一年使用:0次

 )资源打造全产业链,把氟化工作为未来重要的支柱产业培育。下列叙述错误的是
)资源打造全产业链,把氟化工作为未来重要的支柱产业培育。下列叙述错误的是 H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是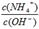 增大
增大

