在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) +Y(g) 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
下列说法不正确的是
 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前2min的平均速率v(Z)=4.0×10-3mol/(L·min) |
| B.其他条件不变,升高温度,反应达到新平衡前v(正)<v(逆) |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
更新时间:2019-02-22 13:55:14
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表:
下列说法正确的是
 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表: 反应时间 | 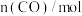 | 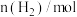 |
| 0 | 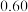 | 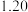 |
| 20 | 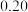 | |
| 30 |  |
A.反应在 内的平均速率为 内的平均速率为 |
B.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
C.保持其他条件不变,再向平衡体系中同时通入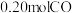 、 、 、 、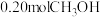 ,达到新平衡前 ,达到新平衡前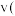 正 正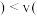 逆 逆 |
D.相同温度下,若起始时向容器中充入 ,达到平衡时 ,达到平衡时 转化率大于 转化率大于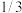 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将 4 mol A 气体和 2 mol B 气体在 2 L 的定容容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
 2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )
2C(g) △H<0 ,经 2 s(秒)后测得 C 的浓度为 0. 6 mol·L-1 ,现有下列几种说法:①用物质 A 表示的反应的平均速率为 0.3 mol·L-1•s-1;②达到平衡状态时,升高温度,平衡逆向移动,化学平衡常数K减小;③2 s 时物质 A 的转化率为70% ;④达平衡时,增加A物质的量,平衡正向移动,A的转化率降低;⑤当B和C的生成速率相等时,该反应达到平衡状态。其中不正确的是( )| A.①③ | B.②⑤ | C.③⑤ | D.②③ |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为:
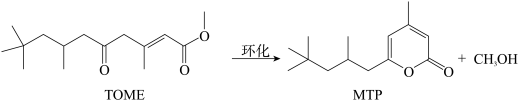
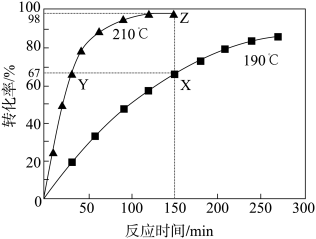
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计。下列说法错误的是


为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计。下列说法错误的是
| A.X、Y两点的MTP的物质的量浓度相等 |
| B.X、Z两点的瞬时速率大小为v(X)>v(Z) |
C.若Z点处于化学平衡,则210℃时反应的平衡常数K=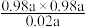 mol/L mol/L |
D.190℃时,0~150 min之间的MTP的平均反应速率为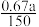 mol/(L·min) mol/(L·min) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】向体积均为2L的两个恒容容器中分别充入2molX和1molY发生反应: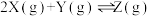 △H,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
△H,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
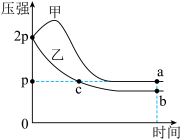
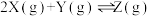 △H,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
△H,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
| A.△H>0 | B.反应速率: |
C.气体的总物质的量: | D.a点平衡常数:K>48 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于可逆反应mA(s)+nB(g) eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
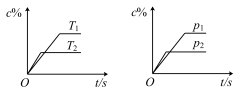
 eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
eC(g)+fD(g),当反应过程中其他条件不变时,C的质量分数(c%)与温度(T)和压强(p)的关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的质量分数将增大 |
| B.达到平衡后,增加A的量有利于化学平衡向正方向移动 |
| C.化学方程式中n>e+f |
| D.达到平衡后,若升高温度,化学平衡向逆方向移动 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】在恒温时,一固定容积的容器内发生如下反应: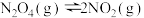 达到平衡时,再向容器内通入一定量的
达到平衡时,再向容器内通入一定量的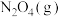 ,重新达到平衡后,与第一次平衡时相比,
,重新达到平衡后,与第一次平衡时相比, 的体积分数
的体积分数
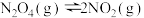 达到平衡时,再向容器内通入一定量的
达到平衡时,再向容器内通入一定量的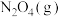 ,重新达到平衡后,与第一次平衡时相比,
,重新达到平衡后,与第一次平衡时相比, 的体积分数
的体积分数| A.不变 | B.增大 | C.减小 | D.无法判断 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定条件下,两体积均为1L的恒容密闭容器中发生反应:CO(g)+2H2(g) CH3OH(g)△H,容器中各物质起始量如表:
CH3OH(g)△H,容器中各物质起始量如表:
下列说法正确的是
 CH3OH(g)△H,容器中各物质起始量如表:
CH3OH(g)△H,容器中各物质起始量如表:| 容器 | 温度 | CO | H2 | CH3OH | H2平衡转化率 |
| Ⅰ | T℃ | amol | 2mol | 0mol | 50% |
| Ⅱ | T℃ | 0.5mol | 1mol | 0mol | 50% |
| A.a=1 |
| B.容器Ⅰ中5min后达到平衡,则该段时间v(CO)=0.01mol•L-1•min-1 |
| C.若温度升高,该反应平衡平衡常数K变为1,则△H<0 |
| D.T时,若起始时向容器中充入CO、H2、CH3OH各1mol,则v逆>v正 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】初始温度为t℃,向三个密闭的容器中按不同方式投入反应物,发生如下反应:4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1,测得反应的相关数据如下:
下列说法正确的是
| 容器 | 容器类型 | 初始体积 | 初始压强/Pa | 反应物投入量/mol | 平衡转化率 | 平衡时Cl2的物质的量/mol | |||
| HCl | O2 | Cl2 | H2O | ||||||
| I | 恒温恒容 | 1L | 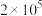 | 4 | 1 | 0 | 0 | α1(HCl) | 1 |
| II | 绝热恒容 | 1L | p2 | 0 | 0 | 2 | 2 | α2(Cl2) | a |
| III | 恒温恒压 | 2L | p3 | 8 | 2 | 0 | 0 | α3(HCl) | b |
| A.反应4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(l)的ΔH>-116kJ·mol-1 |
| B.a>1,b>2 |
| C.p2=1.6×105Pa,p3=4×105Pa |
| D.α1(HCl)+α2(Cl2)>1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】一定温度下,向2L恒容密闭容器中加入2molMoS2、4molH2及4molNa2CO3,发生反应: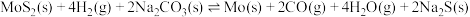 ,10min时达到平衡,测得气体的起始压强与平衡压强之比为4∶5。下列说法正确的是
,10min时达到平衡,测得气体的起始压强与平衡压强之比为4∶5。下列说法正确的是
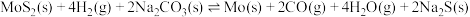 ,10min时达到平衡,测得气体的起始压强与平衡压强之比为4∶5。下列说法正确的是
,10min时达到平衡,测得气体的起始压强与平衡压强之比为4∶5。下列说法正确的是A.该反应的平衡常数表达式为 |
B.0~10min内,用CO表示的平均反应速率 |
| C.增加MoS2的物质的量,可以提高H2的平衡转化率 |
| D.10min时,向容器中再加入2molH2O(g)、2molH2(g)及1molCO(g),平衡逆向移动 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】将一定量的氨基甲酸铵固体置于特制的密闭真空容器中(容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:
2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:
下列说法中正确的是
 2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:
2NH3(g)+CO2(g)。实验测得不同温度下的部分平衡数据如下表:| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | p1 | 12.0 | p2 | 24.0 |
| 平衡气体总浓度/10−3 mol·L−1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.混合气体的平均相对分子质量——M不再随时间变化时反应达平衡状态 |
| B.15.0 ℃时NH2COONH4(s)分解的平衡常数为2.0×10−9(mol/L)3 |
| C.该反应∆H>0,p2=2p1 |
| D.若在恒温下将平衡体系体积减半,再达平衡后,c(NH3)和c(CO2)均比原平衡大 |
您最近半年使用:0次

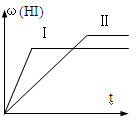
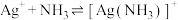
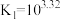
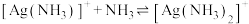

 、
、 、
、 的分布分数
的分布分数 与
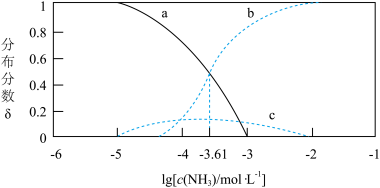
与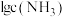 关系如下图所示,下列说法正确的是{例如:分布分数
关系如下图所示,下列说法正确的是{例如:分布分数 }
}
 的平衡常数
的平衡常数
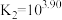
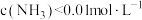 时,银元素主要以
时,银元素主要以

