0.02mol·L—1的HCN溶液与0.02mol·L—1的NaCN溶液等体积混合,已知混合溶液中C(CN-)<C(Na+),则下列关系中,正确的是:
| A.C(Na+)>C(CN-)>C( H+)>C(OH-) |
| B.C(HCN)+C (CN-)=0.04mol·L-1 |
| C.C(CN-)>C(HCN) |
| D.C(Na+)+C(H+)= C(CN-)+C(OH-) |
2011高二·福建龙岩·学业考试 查看更多[10]
甘肃省武威市天祝藏族自治县第一中学2022-2023学年高二下学期开学考试化学试题山西省朔州市应县第一中学校2019-2020学年高二上学期第三次月考化学试题2019-2020学年上海市黄浦区大同中学高二(上)10月月考化学试卷吉林省通化市第十四中学2018-2019学年高二上学期期末考试化学试题广东省深圳市罗湖区2017-2018学年高二上学期期末模拟化学试题(已下线)2010-2011学年福建省龙岩一中高二第四学段模块考试化学试卷2016届内蒙古鄂尔多斯市第三中学高三上学期第四次考试化学试卷(已下线)2013-2014湖北省黄石市秋季高二化学期中统考试卷(已下线)2013届山东省德州市某中学高三12月月考化学试卷(已下线)2012届山东省桓台第二中学高三12月模块检测化学试卷
更新时间:2016-12-09 02:06:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法错误的是( )
①NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的值增大
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol·L-1氨水中滴加0.1 mol·L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol·L-1
④向0.1 mol·L-1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(NH4+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(OH-)=c(H+)+2c(H2S)+c(HS-)
①NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的值增大
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol·L-1氨水中滴加0.1 mol·L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol·L-1
④向0.1 mol·L-1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(NH4+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(OH-)=c(H+)+2c(H2S)+c(HS-)
| A.①④ | B.②④ |
| C.①③ | D.②⑤ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,向15mL 0.1mol·L-1的氢氧化钠溶液中逐滴滴入0.1mol·L-1的CH3COOH溶液,加入CH3COOH溶液的体积与混合溶液pH的关系如图所示(混合过程中忽略溶液体积变化)。下列分析不正确的是
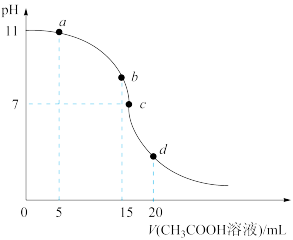

| A.溶液的导电能力:d>c>a |
B.c点对应溶液中,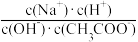 =1 =1 |
| C.a点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.a、b、c、d四点对应溶液中均有c(CH3COO-)+c(CH3COOH)+c(Na+)=0.1mol•L-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,向浓度均为0.1 mol/L、体积均为100mL的两种一元酸HX、HY溶液中,分别加入NaOH的稀溶液,lg[c(H+)/c(OH-)]随加入NaOH的物质的量的变化如图所示。下列说法正确的是
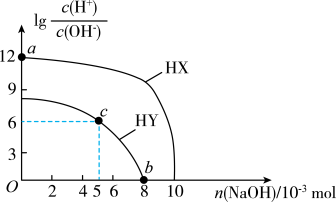

| A.a点溶液的pH=2 |
| B.c点溶液中:c(Yˉ)>c(Na+)>c(HY)>c(H+)>c(OHˉ) |
| C.b点溶液中:c(Yˉ)+c(HY)=c(Na+) |
| D.水的电离程度:a<b<c |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.相同温度下,等pH的盐酸和醋酸加水稀释10倍后,c(Cl-)<c(CH3COO-) |
| B.0.1 mol·L-1的KA溶液pH=6.5,则HA为弱酸 |
C.常温下pH=3的盐酸和pH=11的氨水等体积混合:c(Cl-)+c(H+)=c(NH )+c(OH-) )+c(OH-) |
D.某温度下,向氨水中通入CO2,随着CO2的通入,  不断增大 不断增大 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】M(OH)2是一种二元弱碱,利用pH传感器探究NaOH溶液与H2SO4、MSO4混合溶液发生反应的离子反应顺序,绘得三份曲线图如图。已知实验使用的NaOH溶液浓度和滴速相同;图a和b中H2SO4溶液和MSO4溶液浓度相同;混合溶液中两溶质的浓度也相同。
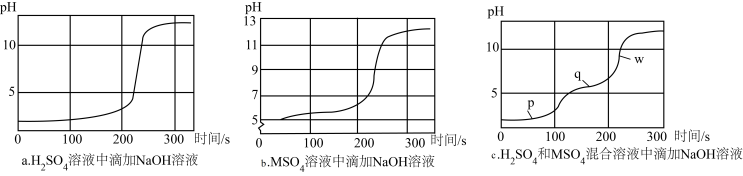
下列说法错误的是

下列说法错误的是
| A.混合溶液中滴加NaOH溶液,H2SO4先于MSO4发生反应 |
| B.p、q、w三个时点的c(M2+):p>q>w |
C.w点:c(Na+)>c(SO )>c(OH-)>c(M2+) )>c(OH-)>c(M2+) |
D.q点时溶液离子浓度:c(SO )+c(OH-)=c(M2+)+c(H+)+c(Na+) )+c(OH-)=c(M2+)+c(H+)+c(Na+) |
您最近半年使用:0次



