M(OH)2是一种二元弱碱,利用pH传感器探究NaOH溶液与H2SO4、MSO4混合溶液发生反应的离子反应顺序,绘得三份曲线图如图。已知实验使用的NaOH溶液浓度和滴速相同;图a和b中H2SO4溶液和MSO4溶液浓度相同;混合溶液中两溶质的浓度也相同。
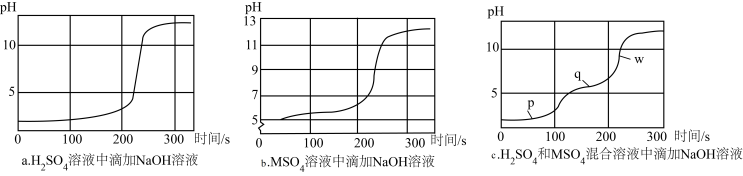
下列说法错误的是

下列说法错误的是
| A.混合溶液中滴加NaOH溶液,H2SO4先于MSO4发生反应 |
| B.p、q、w三个时点的c(M2+):p>q>w |
C.w点:c(Na+)>c(SO )>c(OH-)>c(M2+) )>c(OH-)>c(M2+) |
D.q点时溶液离子浓度:c(SO )+c(OH-)=c(M2+)+c(H+)+c(Na+) )+c(OH-)=c(M2+)+c(H+)+c(Na+) |
更新时间:2022-03-06 20:23:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,向

 溶液和
溶液和

 溶液中滴加
溶液中滴加
 溶液的过程中,pH和导电能力的变化如下图所示,下列说法
溶液的过程中,pH和导电能力的变化如下图所示,下列说法不正确 的是



 溶液和
溶液和

 溶液中滴加
溶液中滴加
 溶液的过程中,pH和导电能力的变化如下图所示,下列说法
溶液的过程中,pH和导电能力的变化如下图所示,下列说法
A. | B. |
C.导电能力图是向盐酸中滴加 | D. 和 和 对应的溶液中水的电离能力相同 对应的溶液中水的电离能力相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在某温度时,将nmol/L氨水滴入10mL1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是


| A.Kw的比较:a点>b点 | B.氨水的浓度等于1.0mol/L |
| C.水的电离程度:a<b<c<d | D.c点:c(Cl-)=c( )>c(H+)=c(OH-) )>c(H+)=c(OH-) |
您最近一年使用:0次
【推荐3】某温度下,AgCl和Ag2CrO4(砖红色沉淀)的沉淀溶解平衡曲线如图所示。下列说法正确的是
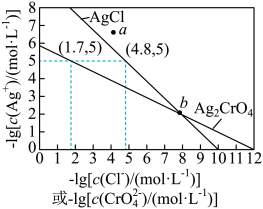

| A.a点条件下能生成Ag2CrO4沉淀,也能生成AgCl沉淀 |
B.b点时,c(Cl-)=c(CrO ),Ksp(AgCl)=Ksp(Ag2CrO4) ),Ksp(AgCl)=Ksp(Ag2CrO4) |
C.Ag2CrO4(s)+2Cl-(aq) 2AgCl(s)+CrO 2AgCl(s)+CrO (aq)的平衡常数K=10-7.9 (aq)的平衡常数K=10-7.9 |
| D.用AgNO3标准溶液滴定未知浓度NaCl溶液时可以用K2CrO4作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,0.02mol·L-1NaHSO3溶液的pH=3。下列说法正确的是
| A.加水稀释10倍后,溶液的pH=4 |
| B.c(SO32-)+c(OH-)=c(H2SO3)+c(HSO3-) |
| C.2c(SO32-)+c(HSO3-)+c(H2SO3)=0.02mol·L-1 |
| D.c(H+)×c(SO32-)/c(HSO3-)约为5×10-5mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,向饱和氯水中逐滴滴入0.1 mol/L的氢氧化钠溶液,pH变化如下图所示,下列有关叙述正确的是
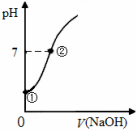

| A.①点所示溶液中只存在HClO的电离平衡 |
B.①点所示溶液中: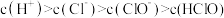 |
C.②点所示溶液中: |
| D.①到②水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】H2CO3和H2C2O4都是二元弱酸,不同pH环境下它们不同形态的粒子的组成百分率如图所示:下列说法正确的是


| A.在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) |
B.反应 HCO3-+H2O H2CO3+OH-的平衡常数为 H2CO3+OH-的平衡常数为 |
| C.0.1 mol/L NaHC2O4溶液中c(C2O4-)+c(H2C2O4)=0.1 mol/L |
| D.往Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+ HC2O4- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】向某Na2A、NaHA的混合液中加入CaCl2固体(忽略溶液体积、温度的变化),测出溶液中离子浓度变化如图所示。已知:Ksp(CaA)=2×10−9,H2A为二元弱酸,Ca(HA)2易溶于水且溶液呈碱性。下列说法正确的是


| A.X、Y、Z三点对应溶液pH大小顺序为:X<Y<Z |
| B.X点溶液中可能存在:c(OH-)=c(H+) |
| C.Y点溶液中c(HA-)=2×10−2 mol∙L−1 |
| D.向Z点溶液中通入HCl气体,可以使Z点溶液向Y点溶液转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,向一定体积 的氨水中逐滴加入等浓度的盐酸,溶液中
的氨水中逐滴加入等浓度的盐酸,溶液中 与
与 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是

 的氨水中逐滴加入等浓度的盐酸,溶液中
的氨水中逐滴加入等浓度的盐酸,溶液中 与
与 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
A.M点的 浓度等于N点的 浓度等于N点的 浓度 浓度 |
B.Q点溶液中, |
| C.M点溶液的导电性小于Q点溶液的导电性 |
D.N点溶液加水稀释, 变小 变小 |
您最近一年使用:0次

 溶液的性质。
溶液的性质。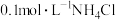 溶液的
溶液的
 溶液等体积混合,产生白色沉淀
溶液等体积混合,产生白色沉淀 氨水中滴加
氨水中滴加 盐酸
盐酸
 的水解
的水解



