元素的基态原子的核外电子有3种能量状态、5种空间状态,X是其中第一电离能最小的元素;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。
(1)X基态原子的电子排布式为___________ 。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是___________ 。
(3)在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是___________ 。
(4)Y与X可形成YX32−。
①YX32−的立体构型为___________ (用文字描述)。
②写出一种与YX32−互为等电子体的分子的化学式___________ 。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2,该配合物加热时,首先失去配离子中的配体是___________ (写化学式)。
(6)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为______ 。其晶胞边长为540.0 pm,密度为________ g·cm−3(列式并计算),a位置Y与b位置Z之间的距离为_______ pm(列式表示)。

(1)X基态原子的电子排布式为
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是
(3)在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是
(4)Y与X可形成YX32−。
①YX32−的立体构型为
②写出一种与YX32−互为等电子体的分子的化学式
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2,该配合物加热时,首先失去配离子中的配体是
(6)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为

更新时间:2019-04-09 11:04:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
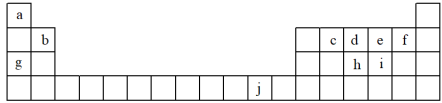
【推荐1】下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)写出元素f简单离子的结构示意图_______ 。
(2)在c6a6分子中,元素c为_______ 杂化,该分子键角是_______ 。
(3)ci2分子的电子式为_______ ,ci2与ce2比较,沸点较高的是_______ (写分子式)。
(4)第一电离能:h_______ i;电负性:g_______ b(填“>”、“<”或“=”)。
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述正确的是_______ (填编号)。
①j位于元素周期表中第四周期、ⅠB族,属于ds区元素
②d的基态原子中,2p能级为半充满,属于p区元素
③最外层电子排布式为4s1,一定属于ⅠA族
④最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是_______ ,写出蓝色沉淀溶解在氨水中的离子方程式_______ 。
(1)写出元素f简单离子的结构示意图
(2)在c6a6分子中,元素c为
(3)ci2分子的电子式为
(4)第一电离能:h
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述正确的是
①j位于元素周期表中第四周期、ⅠB族,属于ds区元素
②d的基态原子中,2p能级为半充满,属于p区元素
③最外层电子排布式为4s1,一定属于ⅠA族
④最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
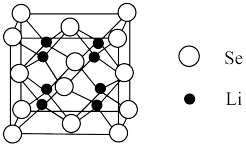
【推荐2】一种新型可充电电池的正极材料由锂、硒两种元素组成,其晶胞结构如图,已知该立方晶胞参数为anm,Se位于晶胞的顶角与面心,Li位于晶胞内。_______ 。
(2)每个Li周围距离相等且最近的Se有_______ 个。每个Se周围距离相等且最近的Li有_______ 个。
(3)该立方晶胞的密度为________ g•cm-3(设NA为阿伏加德罗常数,用含a和NA的代数式表示,1nm=1×10-7cm),在下列方框中写出计算过程。
(2)每个Li周围距离相等且最近的Se有
(3)该立方晶胞的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】碱金属及其化合物在科学研究、生产生活中有广泛应用。请回答下列问题:
(1)基态钠原子核外电子占据能级数为________ ,核外电子共有________ 种不同的运动状态。
(2)与K同周期的元素中,最外层电子数与K相同的为________ (写元素符号)。
(3)在同周期元素中,碱金属元素的________ (填“电负性”“原子半径”或“第一电离能”)最小。
(4)氢化钠晶胞类似氯化钠晶胞(晶胞结构如图1所示)。设氢化钠晶体中钠离子半径为 ,氢离子半径为
,氢离子半径为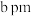 ,并且它们在晶体中紧密堆积,则氢化钠晶胞中离子的空间利用率为
,并且它们在晶体中紧密堆积,则氢化钠晶胞中离子的空间利用率为________ 。 、
、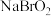 、
、 、
、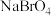 四种钠盐中,Br的杂化方式均为
四种钠盐中,Br的杂化方式均为________ 。
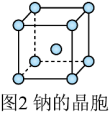
(6)钠晶胞结构如图2所示,配位数为________ 。若钠晶胞的边长为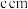 ,
, 代表阿伏加德罗常数的值,则钠晶体的密度为
代表阿伏加德罗常数的值,则钠晶体的密度为________  。
。
(1)基态钠原子核外电子占据能级数为
(2)与K同周期的元素中,最外层电子数与K相同的为
(3)在同周期元素中,碱金属元素的
(4)氢化钠晶胞类似氯化钠晶胞(晶胞结构如图1所示)。设氢化钠晶体中钠离子半径为
 ,氢离子半径为
,氢离子半径为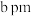 ,并且它们在晶体中紧密堆积,则氢化钠晶胞中离子的空间利用率为
,并且它们在晶体中紧密堆积,则氢化钠晶胞中离子的空间利用率为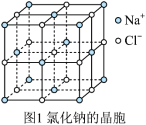
 、
、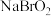 、
、 、
、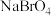 四种钠盐中,Br的杂化方式均为
四种钠盐中,Br的杂化方式均为(6)钠晶胞结构如图2所示,配位数为
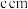 ,
, 代表阿伏加德罗常数的值,则钠晶体的密度为
代表阿伏加德罗常数的值,则钠晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
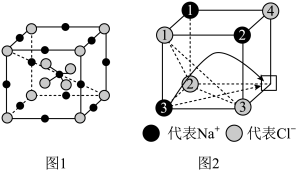
【推荐1】快离子导体是一类具有优良离子导电能力的固体电解质。图1(Li3SBF4)和图2是潜在的快离子导体材料的结构示意图。回答下列问题:
(1)S+2e-=S2-过程中,获得的电子填入基态S原子的____ (填轨道符号)。
(2)BF3+NH3=NH3BF3的反应过程中,形成化学键时提供电子的原子轨道符号是____ ;产物分子中采取sp3杂化轨道形成化学键的原子是____ 。
(3)基态Li+、B+分别失去一个电子时,需吸收更多能量的是____ ,理由是____ 。
(4)图1所示的晶体中,锂原子处于立方体的位置____ ;若其晶胞参数为apm,则晶胞密度为____ g•cm-3(列出计算式即可)。
(5)当图2中方格内填入Na+时,恰好构成氯化钠晶胞的 ,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由
,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由____ 个Cl-构成,空隙的空间形状为____ 。

(1)S+2e-=S2-过程中,获得的电子填入基态S原子的
(2)BF3+NH3=NH3BF3的反应过程中,形成化学键时提供电子的原子轨道符号是
(3)基态Li+、B+分别失去一个电子时,需吸收更多能量的是
(4)图1所示的晶体中,锂原子处于立方体的位置
(5)当图2中方格内填入Na+时,恰好构成氯化钠晶胞的
 ,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由
,且氯化钠晶胞参数a=564pm。氯化钠晶体中,Cl-按照A1密堆方式形成空隙,Na+填充在上述空隙中。每一个空隙由
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(CH3NH3)PbI3作为最典型的有机金属卤化物,一直是太阳能电池研究的宠儿。回答下列问题:
(1)基态Pb原子的价电子排布式为___________ ,N能层电子数有___________ 个。
(2)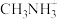 中第一电离能最大的元素是
中第一电离能最大的元素是___________ (填元素符号),该离子中的化学键是由___________ (填标号)原子轨道重叠形成的。
a.sp2与sp2 b.sp3与sp c.sp3与sp3 d.sp3与s e.s与s
(3) 的VSEPR模型如下图,中心I原子的杂化方式是
的VSEPR模型如下图,中心I原子的杂化方式是_______ (填“sp3”、“sp”、“sp3d”或“sp3d2”)。 的空间构型为
的空间构型为______ 。
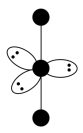
(4)PbF4的熔点显著高于PbCl4的原因是_______ 。
(5)(CH3NH3)PbI3晶体属于钙钛矿型结构(如图所示),Pb2+周围距离最近且相等的I-数目有______ 个。若将A离子作为晶胞的体心另取晶胞Y,则I处于晶胞Y中的______ ,晶胞中A、B之间的距离为apm,(CH3NH3)PbI3式量为M,该物质的密度ρ=______ g▪cm-3(列出计算式,设NA为阿伏加德罗常数的值)。

(1)基态Pb原子的价电子排布式为
(2)
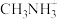 中第一电离能最大的元素是
中第一电离能最大的元素是a.sp2与sp2 b.sp3与sp c.sp3与sp3 d.sp3与s e.s与s
(3)
 的VSEPR模型如下图,中心I原子的杂化方式是
的VSEPR模型如下图,中心I原子的杂化方式是 的空间构型为
的空间构型为
(4)PbF4的熔点显著高于PbCl4的原因是
(5)(CH3NH3)PbI3晶体属于钙钛矿型结构(如图所示),Pb2+周围距离最近且相等的I-数目有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】早在几千年前,人类就掌握了发酵法酿酒的技术。各类酒中都含有浓度不等的乙醇( ),乙醇可以与酸性高锰酸钾(
),乙醇可以与酸性高锰酸钾( )溶液或酸性重铬酸钾(
)溶液或酸性重铬酸钾( )溶液反应,被氧化成乙酸(
)溶液反应,被氧化成乙酸( )。回答下列问题:
)。回答下列问题:
(1)基态K原子的价电子轨道表示式为___________ 。
(2)离子半径:Mn3+___________ (填“>”或“<”) Mn2+。
(3)C、H、O形成的化合物中:
①稳定性:H2O___________ (填“>”“<”或“=”) CH4。
②沸点:CH2CH2OH___________ (填“>”“<”或“=”) CH3COOH。
(4)第一电离能:Mn___________ (填“>”“<”或“=”)Cr,判断的理由为___________ 。
(5)乙醇与酸性高锰酸钾(KMnO4)溶液反应的离子方程式为___________ 。
(6)重铬酸钾(K2Cr2O7)溶液与浓盐酸混合会产生氯气,该反应中,每生成0.1mol氯气,此时转移的电子的物质的量为___________ mol。
 ),乙醇可以与酸性高锰酸钾(
),乙醇可以与酸性高锰酸钾( )溶液或酸性重铬酸钾(
)溶液或酸性重铬酸钾( )溶液反应,被氧化成乙酸(
)溶液反应,被氧化成乙酸( )。回答下列问题:
)。回答下列问题:(1)基态K原子的价电子轨道表示式为
(2)离子半径:Mn3+
(3)C、H、O形成的化合物中:
①稳定性:H2O
②沸点:CH2CH2OH
(4)第一电离能:Mn
(5)乙醇与酸性高锰酸钾(KMnO4)溶液反应的离子方程式为
(6)重铬酸钾(K2Cr2O7)溶液与浓盐酸混合会产生氯气,该反应中,每生成0.1mol氯气,此时转移的电子的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层电子数相同。回答下列问题:
(1)单质M的晶体类型为___________ ,晶体中原子间通过___________ 作用形成面心立方密堆积。
(2)元素Y是___________ (填元素符号),其基态原子的核外电子排布式为___________ ,其同周期元素中,第一电离能最大的是___________ (写元素符号),元素Y与碳原子构成的化合物 的立体构型为
的立体构型为___________ 。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
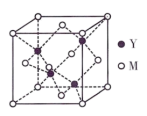
①该化合物的化学式为___________ 。
②该化合物难溶于水但易溶于氨水,其原因是___________ 。此化合物的氨水溶液遇到空气则被氧化为深蓝色,则该深蓝色溶液中阳离子的化学式为___________ 。
(1)单质M的晶体类型为
(2)元素Y是
 的立体构型为
的立体构型为(3)M与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为
②该化合物难溶于水但易溶于氨水,其原因是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】化合物F可以用于治疗哮喘、支气管炎、风湿等疾病。其一种合成路线如图:
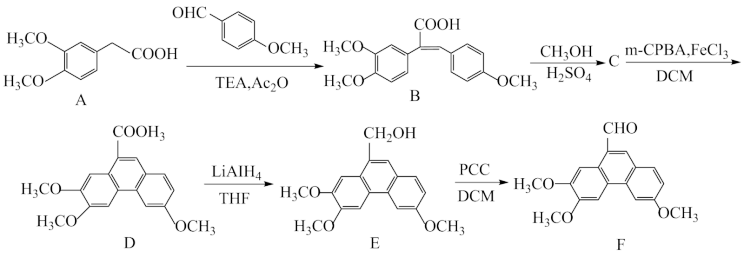
已知:CH2=CH-COOH+HBr→BrCH2-CH2COOH
(1)一个A分子中采用sp3杂化方式的碳原子数目____ 。
(2)A→B经历两步反应,第二步是消去,第一步反应类型为____ 。
(3)C分子式为C19H20O5,则C的结构简式为____ 。
(4)H是F的同系物,相对分子质量比F小28,请写出同时符合下列条件的H的一种同分异构体的结构简式:____ 。
①分子中含有两个苯环;
②既能发生银镜反应又能发生水解,且水解得到的产物能与FeCl3溶液发生显色反应;
③其核磁共振氢谱有4组吸收峰,峰的面积比为1:1:2:2。
(5)设计以 、
、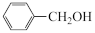 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图____ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

已知:CH2=CH-COOH+HBr→BrCH2-CH2COOH
(1)一个A分子中采用sp3杂化方式的碳原子数目
(2)A→B经历两步反应,第二步是消去,第一步反应类型为
(3)C分子式为C19H20O5,则C的结构简式为
(4)H是F的同系物,相对分子质量比F小28,请写出同时符合下列条件的H的一种同分异构体的结构简式:
①分子中含有两个苯环;
②既能发生银镜反应又能发生水解,且水解得到的产物能与FeCl3溶液发生显色反应;
③其核磁共振氢谱有4组吸收峰,峰的面积比为1:1:2:2。
(5)设计以
 、
、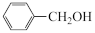 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】现有原子序数依次递增且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子在基态时其最外层电子数是其内层电子数的2倍,Q原子在基态时其 原子轨道上有2个成对电子,W元素的原子中
原子轨道上有2个成对电子,W元素的原子中 能级上有1个成对电子,W元素是人体不可缺少的微量元素,缺少它可造成贫血。回答下列问题:
能级上有1个成对电子,W元素是人体不可缺少的微量元素,缺少它可造成贫血。回答下列问题:
(1)化合物 的结构式为
的结构式为_______ ,中心原子杂化类型为_______ ,化合物 的键角为
的键角为_______ ,中心原子杂化类型为_______ ,化合物 的沸点比化合物
的沸点比化合物 的高,其主要原因是
的高,其主要原因是_______ 。
(2)X与Q可形成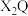 分了,该分子的电子式为
分了,该分子的电子式为_______ ,该分子是_______ (填“极性”或“非极性”)分子。
(3)Y与Q可形成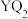 分子,
分子, 分子中含有的
分子中含有的 键数目为
键数目为_______ (设 为阿伏加德罗常数值)。
为阿伏加德罗常数值)。
(4)基态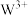 的电子排布式为
的电子排布式为_______ 。
 原子轨道上有2个成对电子,W元素的原子中
原子轨道上有2个成对电子,W元素的原子中 能级上有1个成对电子,W元素是人体不可缺少的微量元素,缺少它可造成贫血。回答下列问题:
能级上有1个成对电子,W元素是人体不可缺少的微量元素,缺少它可造成贫血。回答下列问题:(1)化合物
 的结构式为
的结构式为 的键角为
的键角为 的沸点比化合物
的沸点比化合物 的高,其主要原因是
的高,其主要原因是(2)X与Q可形成
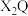 分了,该分子的电子式为
分了,该分子的电子式为(3)Y与Q可形成
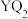 分子,
分子, 分子中含有的
分子中含有的 键数目为
键数目为 为阿伏加德罗常数值)。
为阿伏加德罗常数值)。(4)基态
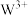 的电子排布式为
的电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】镍与砷或硼等元素可形成多种具有超导电性等特殊性质的化合物,如CaNi2As2等。回答下列问题:
(1)基态Ni2+的价电子排布式为___________ ;熔点:Ni比Ca___________ (填“高"或“低”)。
(2)AsCl3的空间构型为___________ ;AsCl3的键角比BCl3的小,原因是________ ;AsCl3的沸点比BCI3的高,这是因为___________ 。
(3)KBH4中存在的作用力有___________(填标号)。
(4)Y(钇)、Ni、B、C形成的一种具有超导电性的化合物的结构属于四方晶系,其结构如下图所示,则该化合物的化学式为___________ ;已知晶胞参数a=b=352.59pm,c=1053.9pm,设Y、Ni的原子半径分别为rYpm和rNipm,则金属原子的空间占有率为___________ %(列出计算表达式)。
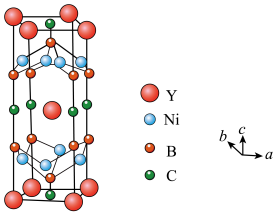
(1)基态Ni2+的价电子排布式为
(2)AsCl3的空间构型为
(3)KBH4中存在的作用力有___________(填标号)。
| A.离子键 | B.氢键 | C.σ键 | D.配位键 |

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】据《自然·通讯》(Nature Communications)报道,我国科学家发现了硒化铜纳米催化剂在二氧化碳电化学还原法生产甲醇过程中催化效率高。铜和硒等元素化合物在生产、生活中应用广泛。
请回答下列问题:
(1)基态硒原子的价电子排布式为_______ ;硒所在主族元素的简单氢化物中沸点最低的是_______ (填化学式)。
(2)电还原法制备甲醇的原理为2CO2+4H2O 2CH3OH+3O2。
2CH3OH+3O2。
①写出该反应中由极性键构成的非极性分子的结构式_______ ;
②1mol CH3OH含有_______ 个共价键。
(3)苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为Π (右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
(右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为_______ ,Se的杂化方式为_______ 。
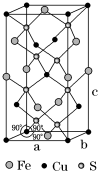
(4)黄铜矿由Cu+、Fe3+、S2-构成,其四方晶系晶胞结构如图所示。则Cu+的配位数为_______ ;若晶胞参数a=b=524 pm,c=1032 pm,用NA表示阿伏加德罗常数的值,该晶系晶体的密度是_______ g·cm-3(不必计算或化简,列出计算式即可)。
请回答下列问题:
(1)基态硒原子的价电子排布式为
(2)电还原法制备甲醇的原理为2CO2+4H2O
 2CH3OH+3O2。
2CH3OH+3O2。①写出该反应中由极性键构成的非极性分子的结构式
②1mol CH3OH含有
(3)苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为Π
 (右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为
(右下角“6”表示6个原子,右上角“6”表示6个共用电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,可表示为
(4)黄铜矿由Cu+、Fe3+、S2-构成,其四方晶系晶胞结构如图所示。则Cu+的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni、Cu等元素。回答下列问题:
(1)写出基态 的电子排布式:
的电子排布式:_______ 。
(2)P元素第一电离能大于S,原因为_______ 。
(3)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是_______ 。
(4)氮化硼(BN)晶体存在如下图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。
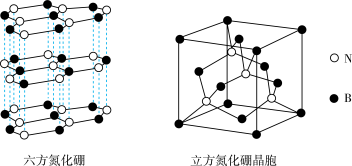
六方氮化硼的晶体类型为_______ ;立方氮化硼晶胞的密度为ρ g·cm ,晶胞的边长为acm。则阿伏加德罗常数的表达式为
,晶胞的边长为acm。则阿伏加德罗常数的表达式为_______ 。
(5)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是_______(填标号)。
(1)写出基态
 的电子排布式:
的电子排布式:(2)P元素第一电离能大于S,原因为
(3)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是(4)氮化硼(BN)晶体存在如下图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。

六方氮化硼的晶体类型为
 ,晶胞的边长为acm。则阿伏加德罗常数的表达式为
,晶胞的边长为acm。则阿伏加德罗常数的表达式为(5)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是_______(填标号)。
A. | B. |
C. | D. |
您最近一年使用:0次



