研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。回答下列问题:
(1)CO可用于高炉炼铁。
已知:Fe3O4(s)+4CO(g)====3Fe(s)+4CO2(g) △H=akJ·mol-1
3Fe2O3(s)+CO(g)====2Fe3O4(s)+CO2(g) △H=bkJ·mol-1
则反应Fe2O3(s)+3CO(g)====2Fe(s)+3CO2(g)的△H=____________ kJ·mol-1(用含a、b的代数式表示)
(2)一定条件下,CO2和CO可以互相转化。某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
甲容器15min后达到平衡,此时CO2的转化率为75%。则0~15min内平均反应速率v(H2)=____________ ,该温度下反应的平衡常数K=____________ 。欲使平衡后乙容器与甲容器中相同气体的体积分数分别相等,则ω、x、y、z需满足的关系是y=____________ ,(用含x、w的代数式表示),且___________ 。
(3)已知反应C6H5CH2CH3(g)+CO2(g) C6H5CH=CH2(g)+CO(g)+H2O(g) △H。温度、压强对乙苯的平衡转化率的影响如下图所示:
C6H5CH=CH2(g)+CO(g)+H2O(g) △H。温度、压强对乙苯的平衡转化率的影响如下图所示:
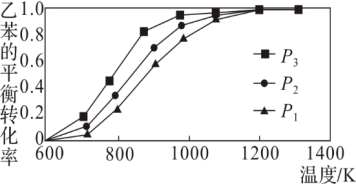
则该反应的△H___________ 0(填“>”“<”或“=”),压强p1、p2、p3从大到小的顺序是___________ 。
(4)CO可被NO2氧化:CO+NO2 CO2+NO。当温度高于225℃时,反应速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分别为正、逆反应速率常数。则k正、k逆与该反应的平衡常数K之间的关系为K=
CO2+NO。当温度高于225℃时,反应速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分别为正、逆反应速率常数。则k正、k逆与该反应的平衡常数K之间的关系为K=___________ 。
(1)CO可用于高炉炼铁。
已知:Fe3O4(s)+4CO(g)====3Fe(s)+4CO2(g) △H=akJ·mol-1
3Fe2O3(s)+CO(g)====2Fe3O4(s)+CO2(g) △H=bkJ·mol-1
则反应Fe2O3(s)+3CO(g)====2Fe(s)+3CO2(g)的△H=
(2)一定条件下,CO2和CO可以互相转化。某温度下,在容积为2L的密闭容器按甲、乙两种方式投入反应物发生反应:CO2(g)+H2(g)
 CO(g)+H2O(g)。
CO(g)+H2O(g)。| 容器 | 反应物 |
| 甲 | 8molCO2(g)、16molH2(g) |
| 乙 | ωmolCO2(g)、xmolH2(g)、ymolCO(g)、zmolH2O(g) |
甲容器15min后达到平衡,此时CO2的转化率为75%。则0~15min内平均反应速率v(H2)=
(3)已知反应C6H5CH2CH3(g)+CO2(g)
 C6H5CH=CH2(g)+CO(g)+H2O(g) △H。温度、压强对乙苯的平衡转化率的影响如下图所示:
C6H5CH=CH2(g)+CO(g)+H2O(g) △H。温度、压强对乙苯的平衡转化率的影响如下图所示:
则该反应的△H
(4)CO可被NO2氧化:CO+NO2
 CO2+NO。当温度高于225℃时,反应速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分别为正、逆反应速率常数。则k正、k逆与该反应的平衡常数K之间的关系为K=
CO2+NO。当温度高于225℃时,反应速率v正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分别为正、逆反应速率常数。则k正、k逆与该反应的平衡常数K之间的关系为K=
更新时间:2019-05-06 09:58:47
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】化学能在一定条件下能够转化为电能,构成原电池。
(1)根据构成原电池的本质判断,如下反应可以设计成原电池的是(填序号)______ 。
A.NaOH+HCl=NaCl+H2O B.Na2CO3+2HCl=2NaCl+H2O+CO2↑
C.2H2O=2H2↑+O2↑ D.Cu+2AgNO3=2Ag+Cu(NO3)2
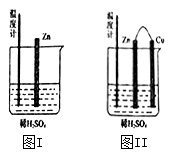
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验。有关实验现象,下列说法正确的是:_______ (填序号)
A.图I和图II的气泡均产生在锌棒表面
B.图II中产生气体的速度比I快
C.图I中温度计的示数高于图II的示数
D.图I和图II中温度计的示数相等,且均高于室温
(3)大气污染越来越成为人们关注的问题.烟气中的NOx必须脱除(即脱硝)后才能排放。已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=一890.3kJ·mol-l
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1
CH4可用于脱硝,写出该反应热化学反应式________ 。
(4)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极反应式为:__________ 。
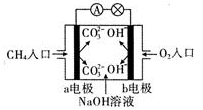
②电池工作一段时间后电解质溶液的pH________ (填“增大”“减小”或“不变”)。
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃料电池。试写出该电池的正极反应式_________ 。
(1)根据构成原电池的本质判断,如下反应可以设计成原电池的是(填序号)
A.NaOH+HCl=NaCl+H2O B.Na2CO3+2HCl=2NaCl+H2O+CO2↑
C.2H2O=2H2↑+O2↑ D.Cu+2AgNO3=2Ag+Cu(NO3)2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验。有关实验现象,下列说法正确的是:
A.图I和图II的气泡均产生在锌棒表面
B.图II中产生气体的速度比I快
C.图I中温度计的示数高于图II的示数
D.图I和图II中温度计的示数相等,且均高于室温

(3)大气污染越来越成为人们关注的问题.烟气中的NOx必须脱除(即脱硝)后才能排放。已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=一890.3kJ·mol-l
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1
CH4可用于脱硝,写出该反应热化学反应式
(4)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极反应式为:

②电池工作一段时间后电解质溶液的pH
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃料电池。试写出该电池的正极反应式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】I.若已知: Cu(OH)2 (s) ⇌ Cu2+ (aq)+2OH—(aq) △H= akJ/mol
H2O(l) ⇌H+(aq) + OH—(aq) △H= bkJ/mol
请写出Cu2+发生水解反应的热化学方程式________________________________ ,该反应的平衡常数为_______ ,已知:25℃时, Ksp[Cu(OH)2]=2.0×10-20 mol3/L3
II.室温下,现有①0. 2 mol/L NaOH溶液、②0.2 mol/L HX溶液,两溶液等体积混合后,测得溶液pH=8则:
(1)上述混合液中各离子浓度由大到小的顺序为_______________________
(2)pH=12的NaOH溶液与pH=2的HX等体积混合,混合后溶液显______ 性(填“酸”、“碱”或“中”)。
III. NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图。

该电池在使用过程中正极反应为:O2+4e-+2N2O5=4NO3—,石墨I电极上生成氧化物Y,其电极反应为:______________________________ 。
H2O(l) ⇌H+(aq) + OH—(aq) △H= bkJ/mol
请写出Cu2+发生水解反应的热化学方程式
II.室温下,现有①0. 2 mol/L NaOH溶液、②0.2 mol/L HX溶液,两溶液等体积混合后,测得溶液pH=8则:
(1)上述混合液中各离子浓度由大到小的顺序为
(2)pH=12的NaOH溶液与pH=2的HX等体积混合,混合后溶液显
III. NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图。

该电池在使用过程中正极反应为:O2+4e-+2N2O5=4NO3—,石墨I电极上生成氧化物Y,其电极反应为:
您最近一年使用:0次
【推荐3】雾霾天气频繁出现,严重影响人们的生活和健康。其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)汽车尾气中NOx和CO的生成:已知汽缸中生成NO的反应为:N2(g)+O2(g) 2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是
2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是________
A.混合气体的密度不再变化
B.容器内的压强不再变化
C.N2、O2、NO的物质的量之比为1∶1∶2
D.氧气的百分含量不再变化
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ·mol- 1
②洗涤含SO2的烟气。
写出焦炭与水蒸气反应的热化学方程式:________________________ 。
(3)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”之一。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质)。一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
①写出NO与活性炭反应的化学方程式________________ ;
②计算上述反应T1℃时的平衡常数K1=________ ;若T1<T2,则该反应的△H_______ 0(填“>”、“<”或“=”)。
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为________ 。
(1)汽车尾气中NOx和CO的生成:已知汽缸中生成NO的反应为:N2(g)+O2(g)
 2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是
2NO(g)△H>0。恒温,恒容密闭容器中,下列说法中能说明该反应达到化学平衡状态的是A.混合气体的密度不再变化
B.容器内的压强不再变化
C.N2、O2、NO的物质的量之比为1∶1∶2
D.氧气的百分含量不再变化
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ·mol- 1
②洗涤含SO2的烟气。
写出焦炭与水蒸气反应的热化学方程式:
(3)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”之一。活性炭可处理大气污染物NO。在5L密闭容器中加入NO和活性炭(假设无杂质)。一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
| 物质 温度/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
①写出NO与活性炭反应的化学方程式
②计算上述反应T1℃时的平衡常数K1=
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】化学在绿色发展、循环发展、低碳发展及推进生态文明建设中正发挥着积极作用。因此,研发 利用技术,降低空气中
利用技术,降低空气中 含量成为研究热点。以
含量成为研究热点。以 、
、 为原料同时发生反应I、II如下:
为原料同时发生反应I、II如下:
反应I.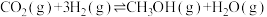
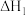

反应II.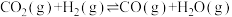
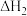

(1)如图1所示,则
_______ 0(填“>”、“<”或“=”)。

(2)在5MPa压强下,恒压反应器中通入3mol 、1mol
、1mol 气体,
气体, 的平衡转化率及
的平衡转化率及 的平衡产率随温度变化关系如图2。
的平衡产率随温度变化关系如图2。
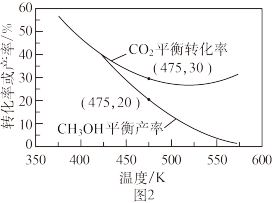
已知: 的产率=
的产率=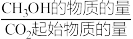 ×100%。
×100%。
①下列说法正确的是_______ 。
A.反应过程中,容器内压强不再变化,说明反应I达到平衡
B.反应过程中,气体密度维持不变,说明反应I达到平衡
C.改用高效催化剂,可增大反应的平衡常数
D.加入对反应I催化效果更佳的催化剂,可以提高 的产率
的产率
②475K时,反应II的压强平衡常数
_______ (压强平衡常数:用平衡分压代替平衡浓度,分压=总压×气体物质的量分数)。
③图2中525K以后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是_______ 。
(3)已知漂白粉需要密封保存,露置在空气中其有效成分易与 反应而变质。
反应而变质。
低温时:
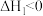
高温时:
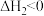
有研究表明,生成 的反应分两步进行:
的反应分两步进行:
i.

ii.

常温下,反应ii能快速进行,但氯气与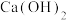 反应很难得到
反应很难得到 。请画出上述过程中
。请画出上述过程中 、
、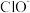 、
、 、
、 的四种物质在反应过程中的能量图
的四种物质在反应过程中的能量图___________ 。

 利用技术,降低空气中
利用技术,降低空气中 含量成为研究热点。以
含量成为研究热点。以 、
、 为原料同时发生反应I、II如下:
为原料同时发生反应I、II如下:反应I.
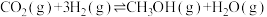
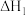

反应II.
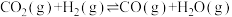
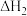

(1)如图1所示,则


(2)在5MPa压强下,恒压反应器中通入3mol
 、1mol
、1mol 气体,
气体, 的平衡转化率及
的平衡转化率及 的平衡产率随温度变化关系如图2。
的平衡产率随温度变化关系如图2。
已知:
 的产率=
的产率=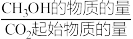 ×100%。
×100%。①下列说法正确的是
A.反应过程中,容器内压强不再变化,说明反应I达到平衡
B.反应过程中,气体密度维持不变,说明反应I达到平衡
C.改用高效催化剂,可增大反应的平衡常数
D.加入对反应I催化效果更佳的催化剂,可以提高
 的产率
的产率②475K时,反应II的压强平衡常数

③图2中525K以后,
 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是(3)已知漂白粉需要密封保存,露置在空气中其有效成分易与
 反应而变质。
反应而变质。低温时:

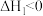
高温时:

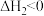
有研究表明,生成
 的反应分两步进行:
的反应分两步进行:i.


ii.


常温下,反应ii能快速进行,但氯气与
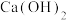 反应很难得到
反应很难得到 。请画出上述过程中
。请画出上述过程中 、
、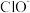 、
、 、
、 的四种物质在反应过程中的能量图
的四种物质在反应过程中的能量图
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】硫及其化合物在生产生活中有广泛的应用。请回答:
(1)室温下, 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示)。
(2)下列关于硫及其化合物的说法,正确的是___________ (填字母)。
A.硫元素在自然界中只能以化合态形式存在
B. 通入紫色石蕊试液,先变红后褪色
通入紫色石蕊试液,先变红后褪色
C.酸雨是 的降水,主要是由污染物
的降水,主要是由污染物 、
、 造成
造成
D.浓硫酸中加入少量胆矾晶体,搅拌,固体逐渐变成白色
(3)光谱研究表明, 的水溶液中存在下列平衡:
的水溶液中存在下列平衡:
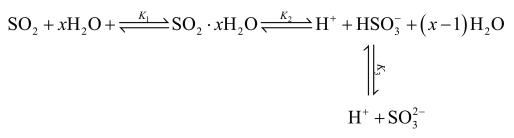
其中 、
、 、
、 为各步的平衡常数,且
为各步的平衡常数,且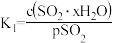 (
( 表示
表示 的平衡压强)。
的平衡压强)。
①当 的平衡压强为p时,测得
的平衡压强为p时,测得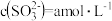 ,则溶液
,则溶液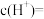
___________ 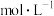 。
。
(用含p、a、 、
、 、
、 的式子表示)
的式子表示)
②滴加NaOH至 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中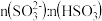
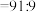 ,需加NaOH将溶液pH调整为约等于
,需加NaOH将溶液pH调整为约等于___________ 。
(4)“钙基固硫”是利用石灰石将燃煤烟气中的 转化为
转化为 。但高温时CO会与
。但高温时CO会与 反应而影响脱硫效率。相关反应如下:
反应而影响脱硫效率。相关反应如下:
Ⅰ.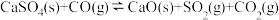
Ⅱ.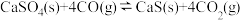
当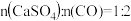 时,反应25min,体系中
时,反应25min,体系中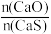 的比值随温度变化如表所示:
的比值随温度变化如表所示:
请结合题给反应过程能量图,说明:
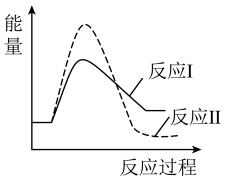
①750K→1250K时,比值随温度升高逐渐减小的原因是___________ 。
②1250K后,比值随温度升高逐渐增大的原因是___________ 。
(5)氨水也可吸收 :
: ,
,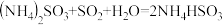 。能提高
。能提高 去除率的措施有
去除率的措施有___________ (填字母)。
A.增大氨水浓度 B.加热煮沸
C.降低烟气的流速 D.补充 ,将
,将 氧化为
氧化为
(1)室温下,
 溶液呈碱性的原因是
溶液呈碱性的原因是(2)下列关于硫及其化合物的说法,正确的是
A.硫元素在自然界中只能以化合态形式存在
B.
 通入紫色石蕊试液,先变红后褪色
通入紫色石蕊试液,先变红后褪色C.酸雨是
 的降水,主要是由污染物
的降水,主要是由污染物 、
、 造成
造成D.浓硫酸中加入少量胆矾晶体,搅拌,固体逐渐变成白色
(3)光谱研究表明,
 的水溶液中存在下列平衡:
的水溶液中存在下列平衡: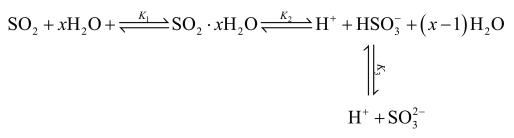
其中
 、
、 、
、 为各步的平衡常数,且
为各步的平衡常数,且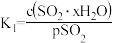 (
( 表示
表示 的平衡压强)。
的平衡压强)。①当
 的平衡压强为p时,测得
的平衡压强为p时,测得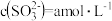 ,则溶液
,则溶液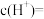
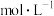 。
。(用含p、a、
 、
、 、
、 的式子表示)
的式子表示)②滴加NaOH至
 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中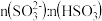
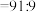 ,需加NaOH将溶液pH调整为约等于
,需加NaOH将溶液pH调整为约等于(4)“钙基固硫”是利用石灰石将燃煤烟气中的
 转化为
转化为 。但高温时CO会与
。但高温时CO会与 反应而影响脱硫效率。相关反应如下:
反应而影响脱硫效率。相关反应如下:Ⅰ.
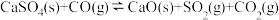
Ⅱ.
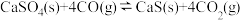
当
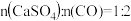 时,反应25min,体系中
时,反应25min,体系中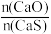 的比值随温度变化如表所示:
的比值随温度变化如表所示:| 温度 | 750K | 1250K | 1750K |
| 比值 | 3.57 | 1.08 | 3.42 |

①750K→1250K时,比值随温度升高逐渐减小的原因是
②1250K后,比值随温度升高逐渐增大的原因是
(5)氨水也可吸收
 :
: ,
,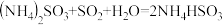 。能提高
。能提高 去除率的措施有
去除率的措施有A.增大氨水浓度 B.加热煮沸
C.降低烟气的流速 D.补充
 ,将
,将 氧化为
氧化为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。
主反应:
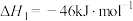
副反应:

回答下列问题:
(1)相关化学键的键能数据如下:
则x=___________ ,主反应在___________ (填“高温”“低温”或“任意温度”)条件下能自发进行。
(2)主反应在铜催化下的反应历程如下:
决定主反应速率的基元反应为___________ (填标号),原因是___________ 。
(3) 和
和 按物质的量之比
按物质的量之比 ,在压强为
,在压强为 ,
, 催化下进行反应,测得
催化下进行反应,测得 转化率和
转化率和 选择性[
选择性[ 选择性=
选择性=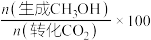 %]随温度的变化如图所示:
%]随温度的变化如图所示:
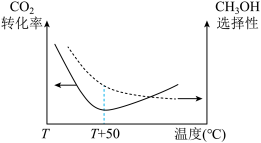
①温度高于 ℃,
℃, 转化率增大的原因可能是
转化率增大的原因可能是___________ 。
②某温度时,若测得 转化率为25%,
转化率为25%, 的选择性为20%,副反应的压力商
的选择性为20%,副反应的压力商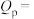
___________ (以分压代替浓度进行计算,分压=总压×物质的量分数,保留一位有效数字)。
③若想要提高 的产率,除改变温度外,还可采取的措施有
的产率,除改变温度外,还可采取的措施有___________ 。
主反应:

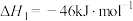
副反应:


回答下列问题:
(1)相关化学键的键能数据如下:
| 化学键 | C=O | H—H | C—H | C—O | O—H |
键能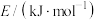 | 803 | 436 | 414 | X | 464 |
(2)主反应在铜催化下的反应历程如下:
| 序号 | 基元反应 |  (活化能/eV) (活化能/eV) |  (反应能/eV) (反应能/eV) |
| ① | 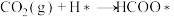 | 0.20 | 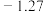 |
| ② | 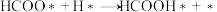 | 1.27 | 0.55 |
| ③ |  | 0.76 | 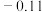 |
| ④ |  | 0.42 | 0.35 |
| ⑤ |  | 0.11 |  |
| ⑥ | 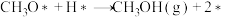 | 0.89 | 0.37 |
| ⑦ | 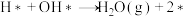 | 1.01 | 0.32 |
(3)
 和
和 按物质的量之比
按物质的量之比 ,在压强为
,在压强为 ,
, 催化下进行反应,测得
催化下进行反应,测得 转化率和
转化率和 选择性[
选择性[ 选择性=
选择性=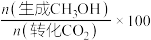 %]随温度的变化如图所示:
%]随温度的变化如图所示:
①温度高于
 ℃,
℃, 转化率增大的原因可能是
转化率增大的原因可能是②某温度时,若测得
 转化率为25%,
转化率为25%, 的选择性为20%,副反应的压力商
的选择性为20%,副反应的压力商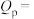
③若想要提高
 的产率,除改变温度外,还可采取的措施有
的产率,除改变温度外,还可采取的措施有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氮及其化合物的研究对于生态环境保护和工农业生产发展非常重要。
Ⅰ. 对合成氨的研究
(1)已知: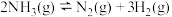
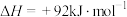 ,该反应的活化能
,该反应的活化能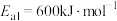 ,则合成氨反应:
,则合成氨反应: 的活化能
的活化能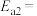
_______ 。
(2)在一定条件下,向某反应容器中投入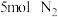 、
、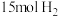 在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。
在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。
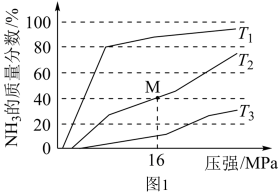
①温度 、
、 、
、 中,由低到高为
中,由低到高为_______ , 点
点 的转化率为
的转化率为_______ 。
②1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为: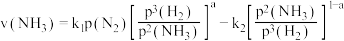 ,
, ,
, 分别为正反应和逆反应的速率常数;
分别为正反应和逆反应的速率常数;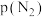 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁触媒为催化剂时,
代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁触媒为催化剂时,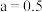 。温度为
。温度为 时,
时,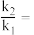
_______  (保留一位小数)。
(保留一位小数)。
Ⅱ. 对相关脱硝反应的研究
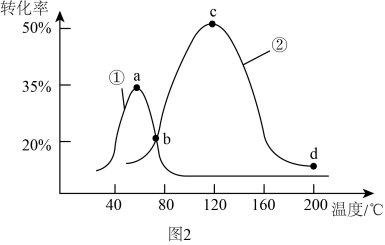
(3)将等物质的量的 和
和 分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
 ,经过相同时间测得
,经过相同时间测得 的转化率如图2所示。图中c点
的转化率如图2所示。图中c点_______ (填“一定”或“不一定”)是平衡状态,请说明理由_______ 。
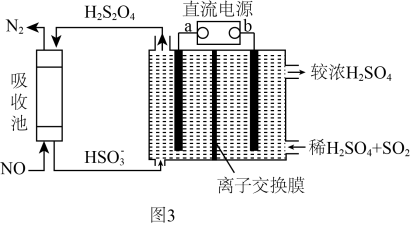
(4)氮的氧化物脱除可用电化学原理处理,如图3装置可同时吸收 和NO。已知:
和NO。已知: 是一种弱酸。该装置中阴极的电极反应式为
是一种弱酸。该装置中阴极的电极反应式为_______ ,应选择_______ (填“阳”或“阴”)离子交换膜。
Ⅰ. 对合成氨的研究
(1)已知:
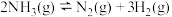
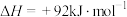 ,该反应的活化能
,该反应的活化能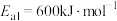 ,则合成氨反应:
,则合成氨反应: 的活化能
的活化能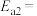
(2)在一定条件下,向某反应容器中投入
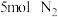 、
、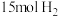 在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。
在不同温度下反应,平衡体系中氨的质量分数随压强变化曲线如图1所示。
①温度
 、
、 、
、 中,由低到高为
中,由低到高为 点
点 的转化率为
的转化率为②1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为:
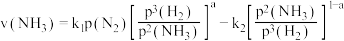 ,
, ,
, 分别为正反应和逆反应的速率常数;
分别为正反应和逆反应的速率常数;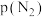 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁触媒为催化剂时,
代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁触媒为催化剂时,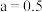 。温度为
。温度为 时,
时,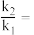
 (保留一位小数)。
(保留一位小数)。Ⅱ. 对相关脱硝反应的研究
(3)将等物质的量的
 和
和 分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
 ,经过相同时间测得
,经过相同时间测得 的转化率如图2所示。图中c点
的转化率如图2所示。图中c点
(4)氮的氧化物脱除可用电化学原理处理,如图3装置可同时吸收
 和NO。已知:
和NO。已知: 是一种弱酸。该装置中阴极的电极反应式为
是一种弱酸。该装置中阴极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】甲烷具有广泛的应用,对于甲烷相关性质的研究成为当前科学研究的重点课题。
(1)利用 和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应:
和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应: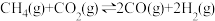 。在恒容密闭容器中
。在恒容密闭容器中 、
、 的分压分别为
的分压分别为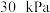 、
、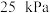 在一定条件下发生上述反应,已知
在一定条件下发生上述反应,已知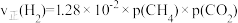
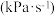 ,某时刻测得
,某时刻测得 ,则该时刻
,则该时刻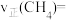
_______ 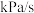 。
。
(2) 和
和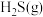 反应可以生成化工原料
反应可以生成化工原料 和
和 。控制体系压强为
。控制体系压强为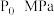 ,当原料初始组成
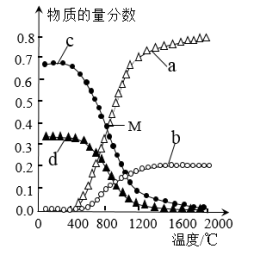
,当原料初始组成 ,当反应达平衡时四种组分的物质的量分数随温度的变化如图。图中表示
,当反应达平衡时四种组分的物质的量分数随温度的变化如图。图中表示 、
、 变化的曲线分别是
变化的曲线分别是_______ (填字母序号)。M点对应温度下, 的转化率是
的转化率是_______ ,反应的
_______ (以分压表示,分压=总压×物质的量分数)。
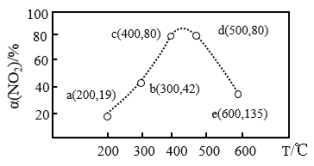
(3)在恒容密闭容器中,通入一定量 和
和 发生反应,相同时间内测得
发生反应,相同时间内测得 的转化率与温度的关系如图。下列叙述正确的是_______。
的转化率与温度的关系如图。下列叙述正确的是_______。
(1)利用
 和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应:
和CO2重整不仅可以获得合成气(主要成分为CO、H2),还可减少温室气体的排放。已知重整过程中涉及如下反应: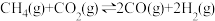 。在恒容密闭容器中
。在恒容密闭容器中 、
、 的分压分别为
的分压分别为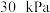 、
、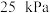 在一定条件下发生上述反应,已知
在一定条件下发生上述反应,已知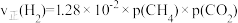
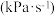 ,某时刻测得
,某时刻测得 ,则该时刻
,则该时刻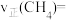
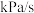 。
。(2)
 和
和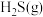 反应可以生成化工原料
反应可以生成化工原料 和
和 。控制体系压强为
。控制体系压强为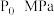 ,当原料初始组成
,当原料初始组成 ,当反应达平衡时四种组分的物质的量分数随温度的变化如图。图中表示
,当反应达平衡时四种组分的物质的量分数随温度的变化如图。图中表示 、
、 变化的曲线分别是
变化的曲线分别是 的转化率是
的转化率是

(3)在恒容密闭容器中,通入一定量
 和
和 发生反应,相同时间内测得
发生反应,相同时间内测得 的转化率与温度的关系如图。下列叙述正确的是_______。
的转化率与温度的关系如图。下列叙述正确的是_______。
A.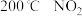 的平衡转化率大于 的平衡转化率大于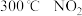 的平衡转化率 的平衡转化率 |
| B.b点的v(逆)大于e点的v(逆) |
| C.c点和d点均处于平衡状态 |
D.适当升温或增大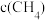 可提高C点时 可提高C点时 的转化率和反应速率 的转化率和反应速率 |
您最近一年使用:0次
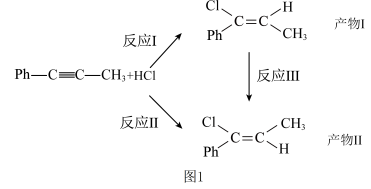
【推荐3】采用固体催化剂可使1-苯基-1-丙炔(Ph-C≡C-CH3,-Ph表示苯基)与HCl加成,体系中涉及反应如图1:
②因反应在高压HCl氛围下进行,故HCl压强近似等于总压。
回答下列问题:
(1)以0.005molPh-C≡C-CH3为初始原料,在473K,3.0×109kPa的高压HCl氛围下,进行上述反应。当产物I和产物Ⅱ的产率均为10%时,体系放热mkJ;当产物I产率为15%、产物Ⅱ产率为25%时,体系放热nkJ。若2m<n,则反应Ⅲ焓变ΔH3_______ 0(填“>”“<”或“=”),反应Ⅱ焓变ΔH2(473K,3.0×109kPa)=_______ kJ/mol(用含m、n的代数式表示)。
(2)初始条件同上,且设产物I为A,产物Ⅱ为B。δi表示某物种i的物质的量与除HCl外其他各物种总物质的量之比,δ₁随时间t变化关系如图2所示。反应的活化能I_______ Ⅱ(填“>”“<”或“=”),平衡后δA=x,δB=y,则Ph-C≡C-CH3转化率=_______ (用含x、y的代数式表示,下同);B产率=_______ ;反应Ⅱ平衡常数Kp=_______ kPa-1。________ 填标号),与改变催化剂状态之前时相比,A达浓度峰值时,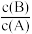 的值
的值_______ 填“增大”“减小”或“不变”,下同),Ph-C≡C-CH3浓度_______ 。
②因反应在高压HCl氛围下进行,故HCl压强近似等于总压。
回答下列问题:
(1)以0.005molPh-C≡C-CH3为初始原料,在473K,3.0×109kPa的高压HCl氛围下,进行上述反应。当产物I和产物Ⅱ的产率均为10%时,体系放热mkJ;当产物I产率为15%、产物Ⅱ产率为25%时,体系放热nkJ。若2m<n,则反应Ⅲ焓变ΔH3
(2)初始条件同上,且设产物I为A,产物Ⅱ为B。δi表示某物种i的物质的量与除HCl外其他各物种总物质的量之比,δ₁随时间t变化关系如图2所示。反应的活化能I

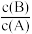 的值
的值
您最近一年使用:0次



