已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g) ΔH=-Q kJ·mol−1(Q>0)。在温度为T1时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,经过4 min反应达到平衡,平衡时H2O(g)的物质的量分数为2%,则下列说法不正确的是
COS(g)+H2O(g) ΔH=-Q kJ·mol−1(Q>0)。在温度为T1时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,经过4 min反应达到平衡,平衡时H2O(g)的物质的量分数为2%,则下列说法不正确的是
 COS(g)+H2O(g) ΔH=-Q kJ·mol−1(Q>0)。在温度为T1时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,经过4 min反应达到平衡,平衡时H2O(g)的物质的量分数为2%,则下列说法不正确的是
COS(g)+H2O(g) ΔH=-Q kJ·mol−1(Q>0)。在温度为T1时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,经过4 min反应达到平衡,平衡时H2O(g)的物质的量分数为2%,则下列说法不正确的是| A.CO2的平衡转化率α=2.5% |
| B.0~4 min内用H2S表示该反应的速率为0.001 mol·L−1·min−1 |
| C.上述条件下反应达到平衡时放出的热量为0.01Q kJ |
| D.其他条件不变,若该反应在温度为T2条件下进行,达到平衡所需时间小于4 min,则T1<T2 |
更新时间:2019-09-30 15:46:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 L浓度为0.100 mol/L的Na2CO3溶液中,阴离子数为0.100NA |
| B.常温下,pH=9的CH3COONa溶液中,水电离出的H+数为10-5NA |
| C.CH4和C2H4混合气体2.24 L(标准状况)完全燃烧,则消耗O2分子数目为0.25NA |
D.H2(g)+ O2(g)=H2O(l) △H=-286 kJ/mol,则每1 mol [H2(g)+ O2(g)=H2O(l) △H=-286 kJ/mol,则每1 mol [H2(g)+ O2(g)]生成1 mol[H2O(l)]放热286 kJ O2(g)]生成1 mol[H2O(l)]放热286 kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】相同质量的氢气、一氧化碳、乙醇、甲烷完全燃烧时,放出热量最多 的是(已知这些物质的燃烧热分别为285.8 kJ/mol、283.0 kJ/mol、1366.8 kJ/mol、890.3 kJ/mol) ( )
| A.C2H5OH(l) | B.CO(g) | C.H2(g) | D.CH4(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】取50 mL过氧化氢水溶液,在少量I- 存在下分解:2H2O2=2H2O+O2↑。在一定温度下,测得O2的放出量,转换成H2O2浓度(c)如下表:
下列说法不正确的是
| t/min | 0 | 20 | 40 | 60 | 80 |
| c/(mol·L-1) | 0.80 | 0.40 | 0.20 | 0.10 | 0.050 |
| A.反应20min时,测得O2体积为224mL(标准状况) |
| B.20~40min,消耗H2O2的平均速率为0.010mol·L-1·min-1 |
| C.第30min时的瞬时速率小于第50min时的瞬时速率 |
| D.H2O2分解酶或Fe2O3代替I-也可以催化H2O2分解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在其他条件不变的情况下,研究催化剂对化学反应速率的影响。在容积不变的密闭容器中,反应A(g)=2B(g)各物质浓度c随反应时间t的部分变化曲线如图所示,下列说法中正确的是
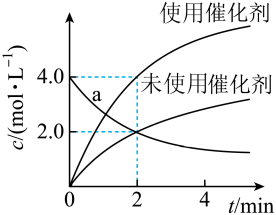

| A.与无催化剂相比,催化剂使反应活化能升高 |
| B.增大催化剂的比表面积,化学反应速率不变 |
| C.a曲线表示未使用催化剂时A的浓度随时间的变化 |
D.使用催化剂时,0~2min内 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案,不能达到相应实验目的的是
| A | B | C | D |
 |  |  |  |
| 探究温度对化学平衡的影响 | 用该装置测定中和热 | 定量测量化学反应速率 | 用于酸性高锰酸钾溶液滴定草酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,利用测压法在刚性反应器中研究固体催化剂作用下的A的分解反应: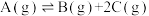 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:
下列说法正确的是
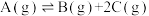 。体系的总压强p随时间t的变化如表所示:
。体系的总压强p随时间t的变化如表所示:| t/'min | 0 | 100 | 150 | 250 | 420 | 540 | 580 | 900 |
| p/kPa | 12.1 | 13.3 | 13.9 | 15.l | 17.14 | 18.58 | 19.06 | a |
A.100~250min,消耗A的平均速率为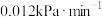 |
| B.推测a一定为22.9 |
| C.适当升高体系温度,改用表面积更大的催化剂可加快反应速率 |
| D.其他条件不变,改用容积更小的刚性反应器,反应速率增大 |
您最近一年使用:0次
【推荐1】 的密闭容器中,充入
的密闭容器中,充入 和
和 发生反应
发生反应 ,经
,经 后B的浓度减少
后B的浓度减少 。对此反应的正确表示是
。对此反应的正确表示是
 的密闭容器中,充入
的密闭容器中,充入 和
和 发生反应
发生反应 ,经
,经 后B的浓度减少
后B的浓度减少 。对此反应的正确表示是
。对此反应的正确表示是A.用A表示的反应速率是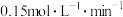 |
B.当C、D浓度之比为 时说明反应达平衡 时说明反应达平衡 |
C.反应 时密闭容器中气体的总物质的量是 时密闭容器中气体的总物质的量是 |
D.在 末B的转化率: 末B的转化率: |
您最近一年使用:0次
【推荐2】已知反应:
A(g)+B(g) C(g)+D(g)的平衡常数与温度的关系如下表。830 ℃时,向一个2 L的密闭容器中充入0.2 mol A和0.8 mol B,反应至4 s时c(C)=0.02 mol·L-1。下列说法正确的是
C(g)+D(g)的平衡常数与温度的关系如下表。830 ℃时,向一个2 L的密闭容器中充入0.2 mol A和0.8 mol B,反应至4 s时c(C)=0.02 mol·L-1。下列说法正确的是
A(g)+B(g)
 C(g)+D(g)的平衡常数与温度的关系如下表。830 ℃时,向一个2 L的密闭容器中充入0.2 mol A和0.8 mol B,反应至4 s时c(C)=0.02 mol·L-1。下列说法正确的是
C(g)+D(g)的平衡常数与温度的关系如下表。830 ℃时,向一个2 L的密闭容器中充入0.2 mol A和0.8 mol B,反应至4 s时c(C)=0.02 mol·L-1。下列说法正确的是| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A.1 200 ℃时反应C(g)+D(g) A(g)+B(g)的平衡常数K=0.4 A(g)+B(g)的平衡常数K=0.4 |
| B.反应达平衡后,升高温度,平衡正向移动 |
| C.830 ℃下反应达平衡时,B的转化率为20% |
| D.4 s内,用A表示的该反应的平均反应速率v(A)=0.01 mol·L-1·s-1 |
您最近一年使用:0次

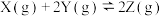 ,X的转化率
,X的转化率 随温度
随温度 的变化如图所示(图中不同温度下的转化率是第5min数据)。下列说法正确的
的变化如图所示(图中不同温度下的转化率是第5min数据)。下列说法正确的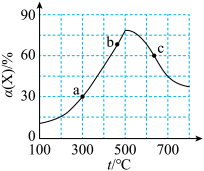

 (Y)大小关系:
(Y)大小关系:
 molX(
molX(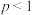 ),同时消耗
),同时消耗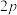 molZ
molZ
 ,其正反应速率方程为
,其正反应速率方程为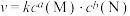 ,T℃时,实验得到了起始反应速率的一组数据如下表所示:
,T℃时,实验得到了起始反应速率的一组数据如下表所示: )
) )
)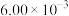
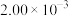
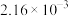
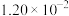
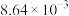
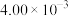
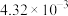
 ,
,
 通入3 L的密闭容器中发生分解反应(此时容器内总压为200 kPa),部分物质的分压随时间的变化曲线如图所示。下列说法错误的是
通入3 L的密闭容器中发生分解反应(此时容器内总压为200 kPa),部分物质的分压随时间的变化曲线如图所示。下列说法错误的是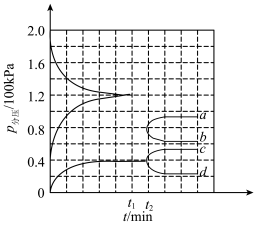
 时已达平衡,混合气体的平均相对分子质量不再变化
时已达平衡,混合气体的平均相对分子质量不再变化 的分压为120 kPa
的分压为120 kPa 时将容器体积迅速缩小至原来的一半并保持不变,图中能表示压缩后
时将容器体积迅速缩小至原来的一半并保持不变,图中能表示压缩后 分压变化趋势的曲线是a
分压变化趋势的曲线是a

