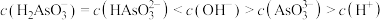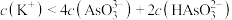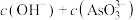已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是
| 弱酸化学 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0 -11 |
| A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| B.a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合后,所得溶液中 c(CN-)>c(Na+),则a一定大于b |
| C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小 |
| D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-) |
11-12高二上·广东汕头·阶段练习 查看更多[1]
(已下线)2011-2012学年广东省汕头市金山中学高二12月月考化学试卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】25℃,加水稀释10 mL pH=11的氨水,下列判断正确的是
| A.原氨水的浓度=10-3 mol·L-1 | B.NH3·H2O的电离程度增大 |
C.溶液中 的增大 的增大 | D.再加入10 mL pH=3的盐酸,混合液pH=7 |
您最近一年使用:0次
多选题
|
适中
(0.65)
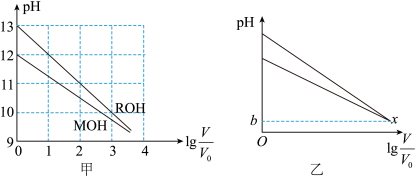
【推荐2】常温下,浓度均为 、体积均为
、体积均为 的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随
的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随 的变化如图甲所示。图乙中,
的变化如图甲所示。图乙中, 时,两曲线出现交叉点x。下列叙述正确的是
时,两曲线出现交叉点x。下列叙述正确的是
 、体积均为
、体积均为 的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随
的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随 的变化如图甲所示。图乙中,
的变化如图甲所示。图乙中, 时,两曲线出现交叉点x。下列叙述正确的是
时,两曲线出现交叉点x。下列叙述正确的是
A. 、 、 均不能确定其数值大小 均不能确定其数值大小 |
| B.x点时,将两种碱溶液等体积混合,混合溶液的pH不变(假设两溶液混合后的体积为二者体积之和) |
| C.x点时,两种溶液中水的电离程度相等 |
D. 相同时,将两种溶液同时升高相同的温度,则 相同时,将两种溶液同时升高相同的温度,则 减小 减小 |
您最近一年使用:0次
【推荐3】由下列操作与现象推出的相应结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 光束通过蛋白质溶液 | 产生光亮通路 | 蛋白质溶液属于胶体 |
| B | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| C | 向某溶液中加入盐酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中不一定含有SO42﹣ |
| D | 测定0.1mol•L﹣1和0.01mol•L﹣1的醋酸溶液导电性 | 前者导电性更强 | 浓度越大,醋酸电离程度越大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,用含0.2molNaOH的溶液恰好吸收0.2molNO2后得1L溶液,反应的化学方程式为:2NO2+2NaOH→NaNO3+NaNO2+H2O。对反应后的溶液,下列说法正确的是(已知:Ka(HNO2)=7.1×10-4、Ka(CH3COOH)=1.7×10-5)( )
| A.n(NO2-)+n(OH-)-n(H+)=0.1mol |
| B.若通入0.01molHCl气体,溶液pH大于2(忽略溶液体积的变化) |
| C.若加入少量CH3COONa固体,溶液的碱性会减弱 |
| D.此时溶液的pH大于0.1mol/L的CH3COONa溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】298K时,向100mL0.1mol•L-1HA溶液中滴入等浓度的KOH溶液,混合溶液的pH与P[ ]的关系如图所示。下列叙述错误的是
]的关系如图所示。下列叙述错误的是
已知:P[ ]=-lg[
]=-lg[ ]
]

 ]的关系如图所示。下列叙述错误的是
]的关系如图所示。下列叙述错误的是已知:P[
 ]=-lg[
]=-lg[ ]
]
| A.25℃时,A-的水解平衡常数Kh的数量级为10-11 |
| B.B点时,2c(K+)>2c(A-)+c(HA) |
| C.未加KOH时,酸和水电离出的H+浓度之比约为1010 |
| D.A点到B点过程中,水的电离程度逐渐减小 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列实验操作和现象及所得结论正确的是
| 实验操作和现象 | 实验结论 | |
| A | 用pH计分别测0.1 mol/L的NaClO与CH3COONa溶液的pH,前者pH大 | Ka(HClO)>Ka(CH3COOH) |
| B | 将铁锈溶于浓盐酸,滴加酸性KMnO4溶液,紫色褪去 | 铁锈中含有二价铁 |
| C | 用pH计测量室温下0.1mol/L氨水pH,pH=11.1 | NH3·H2O是弱碱 |
| D | 向含酚酞的Na2CO3溶液中加入少量BaCl2固体,有白色沉淀生成,溶液颜色变浅 | 溶液中存在水解平衡: +H2O +H2O  +OH- +OH- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
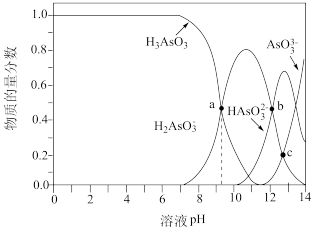
【推荐1】室温下,向一定浓度的 溶液中滴加盐酸,溶液中lg
溶液中滴加盐酸,溶液中lg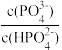 、lg
、lg 、lg
、lg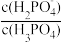 随溶液酸度
随溶液酸度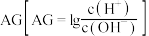 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
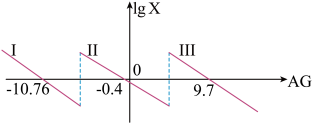
 溶液中滴加盐酸,溶液中lg
溶液中滴加盐酸,溶液中lg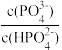 、lg
、lg 、lg
、lg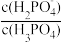 随溶液酸度
随溶液酸度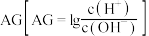 的变化如图所示。下列说法错误的是
的变化如图所示。下列说法错误的是
A. 的 的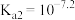 |
B.室温下, 溶液显碱性 溶液显碱性 |
C.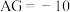 时, c(Cl-)+c(OH-)+5c(PO 时, c(Cl-)+c(OH-)+5c(PO )+c(H2PO )+c(H2PO )> c(Na+)+c(H+) )> c(Na+)+c(H+) |
D.随着 的增大, 的增大, 不断增大 不断增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】向一定体积的 的草酸溶液中滴加
的草酸溶液中滴加 的NaOH溶液,溶液中
的NaOH溶液,溶液中 、
、 、
、 的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是
的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是

 的草酸溶液中滴加
的草酸溶液中滴加 的NaOH溶液,溶液中
的NaOH溶液,溶液中 、
、 、
、 的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是
的物质的量分数(δ)随pH变化的关系如图所示。下列说法错误的是
| A.水的电离程度:N>M>P |
B. 的水解平衡常数 的水解平衡常数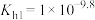 |
C.N点: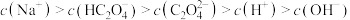 |
D.向 的溶液中持续滴加NaOH溶液,水的电离程度持续变大 的溶液中持续滴加NaOH溶液,水的电离程度持续变大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】室温时,下列溶液中微粒的物质的量浓度关系正确的是
A.0.1mol·L-1K2C2O4溶液与0.2mol·L−1KHC2O4溶液等体积混合:4c(K+)=3[c( )+c( )+c( )+c(H2C2O4)] )+c(H2C2O4)] |
| B.0.2mol·L-1NH3·H2O溶液与0.1mol·L−1HCl溶液等体积混合:c(Cl-)+c(H+)=c(NH3·H2O)+c(OH-) |
| C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合,溶液pH=4:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.0.1mol·L-1CH3COONa溶液与0.1mol·L-1HCl溶液混合到pH=7:c(Na+)>c(Cl-)=c(CH3COOH) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】草酸(H2C2O4)是一种二元弱酸。实验室配制了0.0100mol•L﹣1Na2C2O4标准溶液,现对25℃时该溶液的性质进行探究,下列所得结论正确的是
A.测得0.0100mol•L﹣1Na2C2O4溶液pH为8.6,此时溶液中存在:c(Na+)>c( )>c( )>c( )>c(H+) )>c(H+) |
B.向该溶液中滴加稀盐酸至溶液pH=7,此时溶液中存在:c(Na+)=c( )+2c( )+2c( ) ) |
C.向该溶液中加入足量稀硫酸酸化后,再滴加KMnO4溶液,发生反应的离子方程式为 +4 +4 +14H+=2CO2↑+4Mn2++7H2O +14H+=2CO2↑+4Mn2++7H2O |
D.已知CaC2O4难溶于水,存在溶解平衡,25℃时饱和CaC2O4溶液的浓度为5×10﹣5mol•L﹣1,向该溶液中加入等体积0.0200mol•L﹣1CaCl2溶液,所得上层清液中c( )<5.00×10﹣5mol•L﹣1 )<5.00×10﹣5mol•L﹣1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】常温下,向20mL0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液。滴加过程中微粒的物质的量变化绘制在如图中,根据图示分析判断,下列说法正确的是( )


| A.当V(NaOH)=0mL时,溶液中pH<4 |
| B.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.当V(NaOH)=30mL时,溶液中离子浓度大小关系:c(A2-)>c(HA-) |
| D.当V(NaOH)=40mL时,其溶液中水的电离程度比纯水小 |
您最近一年使用:0次