TiCl3是烯烃定向聚合的催化剂、TiCl4可用于制备金属Ti。
nCH3CH=CH2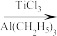
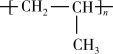
TiO2+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
TiCl4+2Mg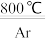 Ti+2MgCl2
Ti+2MgCl2
(1)Ti3+的基态核外电子排布式为__________ 。
(2)丙烯分子中,碳原子轨道杂化类型为______ 和____ 。
(3)Mg、Al、Cl第一电离能由大到小的顺序是___________ 。
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式________ 。
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为______ 。
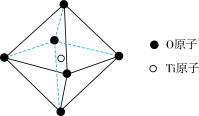
(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为_________ 。
nCH3CH=CH2
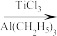
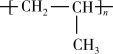
TiO2+2C+2Cl2
 TiCl4+2CO
TiCl4+2COTiCl4+2Mg
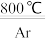 Ti+2MgCl2
Ti+2MgCl2(1)Ti3+的基态核外电子排布式为
(2)丙烯分子中,碳原子轨道杂化类型为
(3)Mg、Al、Cl第一电离能由大到小的顺序是
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为

(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为
更新时间:2019-12-17 14:46:24
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】N、P、As均为氮族元素,这些元素与人们的生活息息相关。回答下列问题:
(1)按电子排布N元素在周期表分区中属于_____ 区元素,基态N原子的未成对电子数目为____ 个。
(2)Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是____ ,第一电离能由大到小的顺序是_____ 。
(3)吡啶为含N有机物,这类物质是合成医药、农药的重要原料。下列吡啶类化合物A与Zn(CH3CH2)2(即ZnEt2)反应生成有机化合物B,B具有优异的催化性能。
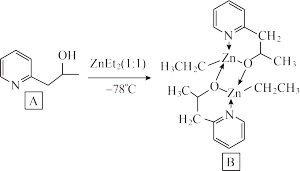
吡啶类化合物A中N原子的杂化类型是___ ,化合物A易溶于水,主要原因是_____ 。含Zn有机物B的分子结构中含_______ (填字母代号)。
A.离子键 B.配位键 C.π键 D.σ键 E.氢键
(4)N与金属可形成氮化物,如AlN的晶体结构如图1所示,某种氮化铁的结构如图2所示。
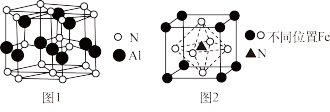
①AlN晶体结构单元中,含有的Al、N原子个数均是_______ ;
②若该氮化铁的晶胞边长为apm,阿伏加德罗常数的值为NA,则该氮化铁的晶体密度可表示为_______ g·cm−3。
(1)按电子排布N元素在周期表分区中属于
(2)Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是
(3)吡啶为含N有机物,这类物质是合成医药、农药的重要原料。下列吡啶类化合物A与Zn(CH3CH2)2(即ZnEt2)反应生成有机化合物B,B具有优异的催化性能。

吡啶类化合物A中N原子的杂化类型是
A.离子键 B.配位键 C.π键 D.σ键 E.氢键
(4)N与金属可形成氮化物,如AlN的晶体结构如图1所示,某种氮化铁的结构如图2所示。

①AlN晶体结构单元中,含有的Al、N原子个数均是
②若该氮化铁的晶胞边长为apm,阿伏加德罗常数的值为NA,则该氮化铁的晶体密度可表示为
您最近半年使用:0次
【推荐2】2017年5月海底天然气水合物(俗称可燃冰)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子的空间结构为___________ 。
(3)为开采海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为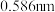 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(4)“可燃冰”中分子间存在的作用力是氢键和___________ ,上图中最小的环中连接的原子总数是___________ 。
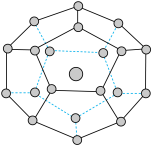
| 参数分子 | 分子直径/nm | 分子与H2O的结合能E(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为
(2)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为(3)为开采海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为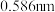 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是(4)“可燃冰”中分子间存在的作用力是氢键和
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布是 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①元素:C___________ 、F___________ 。
②A、B、C三种元素的电负性由大到小的顺序是:___________ 。
③B、C、D、E四种元素的第一电离能由大到小的顺序是:___________ 。
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是___________ (填元素符号)。
(3)F元素位于周期表的_______ 区,此区元素的价电子层结构特点是_______ 。
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E和D的最高能层数相同,其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。(1)请用元素符号完成下列空白:
①元素:C
②A、B、C三种元素的电负性由大到小的顺序是:
③B、C、D、E四种元素的第一电离能由大到小的顺序是:
(2)下表是A~F元素中某种元素的部分电离能,由此可判断该元素是
| 元素 | 电离能/( | ||||
 |  |  |  |  | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近半年使用:0次
【推荐1】研究发现,在CO2低压合成甲醇反应CO23H2CH3OHH2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为________ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(3)比较CO2和H2O沸点________ ,原因是________ 。
(4)MnNO3中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)比较CO2和H2O沸点
(4)MnNO3中的化学键除了σ键外,还存在
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】中国政府承诺:力争CO2的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”,CO2的捕集与利用成为当前研究的热点。回答下面问题:
(1)写出CO2的电子式______ ,CO2分子属于______ (填“极性”或“非极性”)分子,其晶体俗名干冰,属于______ 晶体,其晶体内存在的微粒间相互作用有______ 。
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为______ 。Co在周期表中属于______ 区元素。甲醇(CH3OH)能够与水任意比互溶,解释其原因是______ 。
(3)金属Zn属于金属晶体,其导电的原因是是______ 。已知金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为______ 。
(4)CaF2的晶胞结构如图所示,X代表的离子是______ ;若该立方晶胞参数为apm,CaF2的摩尔质量用Mg/mol,阿伏伽德罗常数用NA来表示,则CaF2晶体的密度=______ g/cm3(写出表达式),阴阳离子的核间距最小为______ pm。

(1)写出CO2的电子式
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为
(3)金属Zn属于金属晶体,其导电的原因是是
(4)CaF2的晶胞结构如图所示,X代表的离子是

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】我国将力争在2030年前实现碳达峰,2060年前实现碳中和的目标,因此二氧化碳的固定以及转化将成为重要的研究课题。
Ⅰ.在 催化下
催化下 和
和 反应生成甲醇:
反应生成甲醇: 。
。
Ⅱ.新型 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储氢物质HCOOH。
被转化为储氢物质HCOOH。
请回答下列问题:
(1)I中涉及的 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是___________ ,基态O原子核外有___________ 种不同空间运动状态的电子。
(2)HCOOH分子中 键和
键和 键数目之比为
键数目之比为___________ 。
(3)反应 中,碳原子的杂化方式由
中,碳原子的杂化方式由___________ 转变为___________ 。 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(4)一种铜的配合物为 ,其配体为
,其配体为___________ ,0.1mol该配合物与足量 溶液充分反应,生成的白色沉淀质量为
溶液充分反应,生成的白色沉淀质量为___________ g。
Ⅰ.在
 催化下
催化下 和
和 反应生成甲醇:
反应生成甲醇: 。
。Ⅱ.新型
 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储氢物质HCOOH。
被转化为储氢物质HCOOH。请回答下列问题:
(1)I中涉及的
 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是(2)HCOOH分子中
 键和
键和 键数目之比为
键数目之比为(3)反应
 中,碳原子的杂化方式由
中,碳原子的杂化方式由 的沸点高于
的沸点高于 ,原因是
,原因是(4)一种铜的配合物为
 ,其配体为
,其配体为 溶液充分反应,生成的白色沉淀质量为
溶液充分反应,生成的白色沉淀质量为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】蛇纹石是一类含水富镁硅酸盐矿物,主要成分为MgO和SiO2,含少量Fe、Ni的氧化物。可用于生产重要无机化工产品碱式碳酸镁[Mg2(OH)2CO3)。其制备流程如图所示:
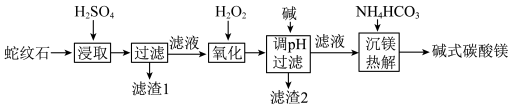
(1)①滤渣1的主要成分从性质上来分,属于___________ 氧化物,其用途很广泛,请写出一种:___________ 。
A.酸性 B.两性 C.碱性
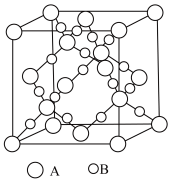
②如图表示该物质晶体的晶胞结构,1个该晶胞中含有___________ 个A-B键。
A.28 B.32 C.36
(2)a.滤渣2的主要成分是Fe(OH)3和Ni(OH)2,“氧化”过程中发现所用H2O2远高于理论用量,造成这一结果的主要原因有:①氧化产物Fe3+可以作H2O2分解的催化剂,加快H2O2的分解速率、②___________ 。
b.酸性KMnO4溶液是否可以检验“氧化”过程已完全___________ ?并说明理由___________ 。
A.是 B.否
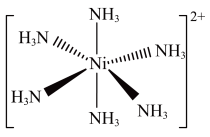
(3)Ni2+易形成[Ni(NH3)6]2+配合物,若[Ni(NH3)6]2+为正八面体构型(如图所示),则[Ni(CO)2(NH3)4]2+的结构有___________ 种。
A.1 B.2 C.4
(4)“沉镁热解”由连续的两步完成,第一步:沉镁生成正碳酸镤(MgCO3·3H2O)和CO2,第二步:将正碳酸镁热解生成碱式碳酸镁。写出第一步的化学方程式:___________ 。
(5)用x吨含3MgO·2SiO2·2H2O(摩尔质量为ag/mol)为80%蛇纹石为原料,按以上流程制取[Mg2(OH)2CO3](摩尔质量为bg/mol),制得产品y吨,制取过程中镁元素的损失率为___________ ×100%(用含x、y、a、b的式子表示)。

(1)①滤渣1的主要成分从性质上来分,属于
A.酸性 B.两性 C.碱性
②如图表示该物质晶体的晶胞结构,1个该晶胞中含有
A.28 B.32 C.36

(2)a.滤渣2的主要成分是Fe(OH)3和Ni(OH)2,“氧化”过程中发现所用H2O2远高于理论用量,造成这一结果的主要原因有:①氧化产物Fe3+可以作H2O2分解的催化剂,加快H2O2的分解速率、②
b.酸性KMnO4溶液是否可以检验“氧化”过程已完全
A.是 B.否
(3)Ni2+易形成[Ni(NH3)6]2+配合物,若[Ni(NH3)6]2+为正八面体构型(如图所示),则[Ni(CO)2(NH3)4]2+的结构有
A.1 B.2 C.4

(4)“沉镁热解”由连续的两步完成,第一步:沉镁生成正碳酸镤(MgCO3·3H2O)和CO2,第二步:将正碳酸镁热解生成碱式碳酸镁。写出第一步的化学方程式:
(5)用x吨含3MgO·2SiO2·2H2O(摩尔质量为ag/mol)为80%蛇纹石为原料,按以上流程制取[Mg2(OH)2CO3](摩尔质量为bg/mol),制得产品y吨,制取过程中镁元素的损失率为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
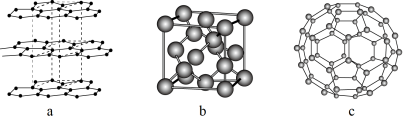
观察上述结构,判断a中碳原子的杂化方式为______ ,b对应的物质是_______ ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为__________ 。
(2)在C60单质中,微粒之间的作用力为_______________ ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于________ 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为_______ ;写出另一与CO互为等电子体的化学式______ 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为_____________________ ;写出基态Ni原子的电子排布式_________________ 。
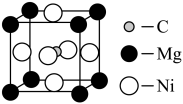
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为______ ; C、Ni、Mg三种元素中,电负性最大的是___________ 。
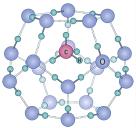
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能___ ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是____________________________________ 。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图

观察上述结构,判断a中碳原子的杂化方式为
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为
(2)在C60单质中,微粒之间的作用力为
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为

(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】宋代《开宝本草》记载“取钢煅作叶如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”“铁华”是醋酸亚铁,其熔点约为195°C。请回答下列问题:
(1)基态Fe3+的电子排布式为__________ 。
(2)醋酸亚铁中碳原子的杂化轨道类型有__________ ,其晶体类型最可能是__________ 。
(3)盐水若洒在煤火上会产生黄色火焰,此过程中相应原子中电子跃迁方式为__________ 。
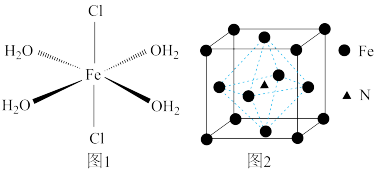
(4)FeCl2•4H2O是一种配合物,其结构如图l所示,则FeCl2•4H2O是__________ (填“极性”或“非极性”)分子。
(1)基态Fe3+的电子排布式为
(2)醋酸亚铁中碳原子的杂化轨道类型有
(3)盐水若洒在煤火上会产生黄色火焰,此过程中相应原子中电子跃迁方式为
(4)FeCl2•4H2O是一种配合物,其结构如图l所示,则FeCl2•4H2O是

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】Fe、Co、Ni是第四周期的重要的金属元素,回答下列问题:
(1)FeCoOx是一种新型光电催化剂,第四电离能大小关系是I4(Fe)_____ I4(Co)(填“>”“<”或“=”),原因是____________________ 。
(2)二茂铁是一种具有芳香族性质的有机过渡金属化合物。其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为____________
②1mol环戊二烯中有__________ molσ键。
(3)①FeS2晶体的晶胞如图甲所示。已知其晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,晶胞边长__________ nm。
②该晶胞中Fe2+位于S 所形成的正八面体的体心,则正八面体的边长为
所形成的正八面体的体心,则正八面体的边长为______ nm
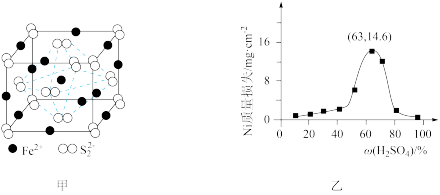
(4)基态Ni2+的价电子排布图为________ 。在一定温度下将Ni片与不同质量分数的硫酸反应,4h后的Ni的质量损失情况如图乙所示,发现当硫酸质量分数大于63%时Ni被腐蚀的速率逐渐降低,其可能原因为__________________ 。
(1)FeCoOx是一种新型光电催化剂,第四电离能大小关系是I4(Fe)
(2)二茂铁是一种具有芳香族性质的有机过渡金属化合物。其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为
②1mol环戊二烯中有
(3)①FeS2晶体的晶胞如图甲所示。已知其晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,晶胞边长
②该晶胞中Fe2+位于S
 所形成的正八面体的体心,则正八面体的边长为
所形成的正八面体的体心,则正八面体的边长为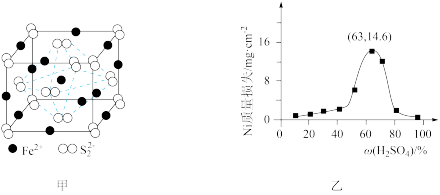
(4)基态Ni2+的价电子排布图为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】钛的化合物种类繁多。回答下列问题:
(1)下列价电子排布图表示基态 原子的是
原子的是_____ (填标号)。
A. B.
B. C.
C.
(2) 的熔点
的熔点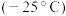 远低于
远低于 的熔点
的熔点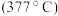 ,原因是
,原因是_____ 。
(3) 常温下呈固态。
常温下呈固态。
①区分 是晶体或非晶体最可靠的科学方法是
是晶体或非晶体最可靠的科学方法是_____ 。
② 水溶液可制备配合物
水溶液可制备配合物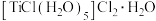 ,其配位原子是
,其配位原子是_____ (用化学符号表示),化学键类型有_____ (填标号)。
A.离子键 B.非极性键 C.配位键 D.金属键
(4)TiN晶胞结构如图所示。
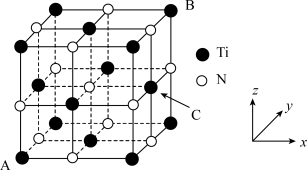
①如果 位于晶胞的棱心和体心,则
位于晶胞的棱心和体心,则 位于晶胞的
位于晶胞的_____ 。
②已知A、B原子的坐标参数分别为 、
、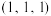 ,则
,则 处
处 原子的坐标为
原子的坐标为_____ 。
③若 立方晶胞参数为
立方晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是_____  (列出计算式)。
(列出计算式)。
(1)下列价电子排布图表示基态
 原子的是
原子的是A.
 B.
B. C.
C.
(2)
 的熔点
的熔点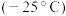 远低于
远低于 的熔点
的熔点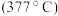 ,原因是
,原因是(3)
 常温下呈固态。
常温下呈固态。①区分
 是晶体或非晶体最可靠的科学方法是
是晶体或非晶体最可靠的科学方法是②
 水溶液可制备配合物
水溶液可制备配合物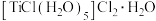 ,其配位原子是
,其配位原子是A.离子键 B.非极性键 C.配位键 D.金属键
(4)TiN晶胞结构如图所示。

①如果
 位于晶胞的棱心和体心,则
位于晶胞的棱心和体心,则 位于晶胞的
位于晶胞的②已知A、B原子的坐标参数分别为
 、
、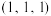 ,则
,则 处
处 原子的坐标为
原子的坐标为③若
 立方晶胞参数为
立方晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是 (列出计算式)。
(列出计算式)。
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)键角:
______ 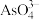 ,与
,与 互为等电子体的分子为
互为等电子体的分子为_______ (填化学式,任写一种即可)。
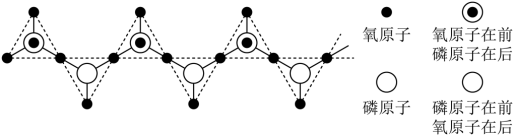
(2)浓磷酸在常温下呈粘稠状,原因_______ ,多聚磷酸由磷酸 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为_______ 。
(3) 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有_______ 个。
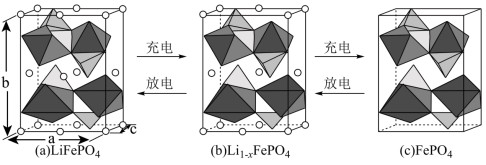
电池充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=_______ ,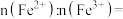
_______ 。
(1)键角:

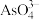 ,与
,与 互为等电子体的分子为
互为等电子体的分子为(2)浓磷酸在常温下呈粘稠状,原因
 加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
加热脱水缩合而成。链状多聚磷酸是多个磷酸通过脱水后共有部分氧原子连接起来的,多聚磷酸根离子的部分结构投影图如图所示(由于P、O原子的半径大小不同,投影图中P与O之间存在部分或全部遮掩关系),则其化学式为
(3)
 的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
的晶胞结构示意图如(a)所示。其中О围绕Fe和Р分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有
电池充电时,
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则x=
,结构示意图如(b)所示,则x=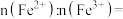
您最近半年使用:0次

 )
)

