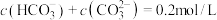下列有关水溶液的一些叙述正确的是( )
A.某水溶液中,c(H+)=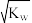 mol/L,该溶液呈中性 mol/L,该溶液呈中性 |
| B.已知电离常数H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11,HClO的Ka=2.95×10-8,相同温度相同浓度溶液的pH:Na2CO3<NaClO |
| C.常温下,向Na2S溶液中加入NaCl溶液,S2-的水解程度不受影响 |
| D.向含有Cl-、Br-、I-的混合溶液中滴加AgNO3溶液,先产生黄色沉淀,说明c(I-)最大 |
更新时间:2020-02-13 17:42:58
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知25℃时CH3COOH的电离常数K=1.6×10-5。该温度下向20ml 0.01mol·L-1 CH3COOH溶液中逐滴加入0.01mol·L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是

| A.a点溶液中c(H+)为4.0×10-5mol/L |
| B.c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO->c(H+)=c(OH-) |
| C.V=200 |
| D.a、b、c三点中水的电离程度最大的是c点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组离子在指定条件下,一定能大量共存的是( )
A.能使蓝色石蕊试纸变红色的溶液中:K+、Na+、CO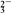 、NO 、NO |
B.水电离出的c(H+)=1×10-12 mol/L的溶液中:Na+、Mg2+、Cl-、SO |
C.能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH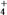 、S2-、Br- 、S2-、Br- |
D.c(H+)=1×10-1 mol/L的溶液中:Cu2+、Al3+、SO 、NO 、NO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,浓度均为 的下列溶液中,粒子的物质的量浓度关系正确的是
的下列溶液中,粒子的物质的量浓度关系正确的是
 的下列溶液中,粒子的物质的量浓度关系正确的是
的下列溶液中,粒子的物质的量浓度关系正确的是A. 溶液中, 溶液中,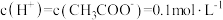 |
B. 溶液中, 溶液中,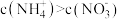 |
C. 溶液中, 溶液中,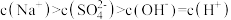 |
D. 溶液中, 溶液中, |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
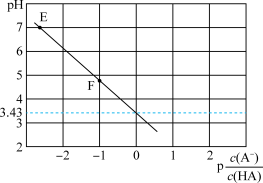
【推荐2】25℃时,向0.1mol/LNaA溶液中逐滴滴加盐酸,测得混合溶液的pH与 变化关系如图所示[p
变化关系如图所示[p =-lg
=-lg ]。下列叙述错误的是
]。下列叙述错误的是
 变化关系如图所示[p
变化关系如图所示[p =-lg
=-lg ]。下列叙述错误的是
]。下列叙述错误的是
| A.Ka (HA)的数量级为10-4 |
| B.E点溶液中c(Na+)=c(A—) |
C.滴加过程中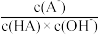 保持不变 保持不变 |
| D.F点溶液c(Na+)>c(A—)>c(HA) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下将分散系X加水稀释10倍后,所做判断正确的是
| 选项 | X | 稀释后 |
| A | 0. 1mol·L-1NaCl | c(Na+)和c(H+)都减小 |
| B | 0. 1mol·L-1Na2CO3 | c( HCO )/ c ( CO )/ c ( CO )减小 )减小 |
| C | 0. 1mol·L-1氨水 | n(H+)·n(OH-)增大 |
| D | 一定量的CuS悬浊液 | c( Cu2+ )和c(S2- )都增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 实验操作和现象 | 结论 | |
| A | 用pH计测得NaOH溶液的pH为11.0,NH4Cl溶液的pH为3.0 | 水的电离程度相同 |
| B | 用pH试纸测得CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH的强 |
| C | 将20℃0.5mol/LCH3COONa溶液加热到60℃,用pH传感器测定溶液的pH,pH逐渐减小 | 水解平衡逆向移动的结果 |
| D | 常温下,用pH计分别测定1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4的pH,pH都等于7 | 两溶液均发生了水解,水解后均显中性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】沉淀的转化在生产中具有重要的应用价值。为了除去水垢中的 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是
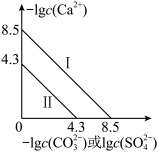
已知: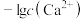 与
与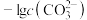 或
或 的关系如图所示,且
的关系如图所示,且 。
。
 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是已知:
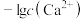 与
与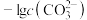 或
或 的关系如图所示,且
的关系如图所示,且 。
。
A. 中 中 的杂化轨道类型是 的杂化轨道类型是 |
B.反应 的平衡常数 的平衡常数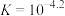 |
C. 中存在的化学键为 中存在的化学键为 键、 键、 键和范德华力 键和范德华力 |
D. 的 的 溶液中,一定存在 溶液中,一定存在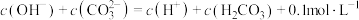 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列图示所得出的结论正确的是( )
A.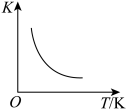 ,反应 ,反应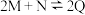 的平衡常数与温度的关系,说明该反应的 的平衡常数与温度的关系,说明该反应的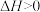 |
B.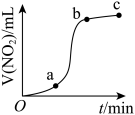 , , 与过量浓硝酸反应生成的 与过量浓硝酸反应生成的 气体体积随时间的变化关系,说明该反应在b→c时间段内反应速率最快 气体体积随时间的变化关系,说明该反应在b→c时间段内反应速率最快 |
C.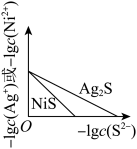 ,常温下 ,常温下 和 和 的沉淀溶解平衡曲线,若 的沉淀溶解平衡曲线,若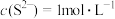 时,两者的 时,两者的 相等 相等 |
D.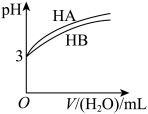 ,常温下 ,常温下 的 的 和 和 溶液分别加水稀释时 溶液分别加水稀释时 的变化曲线,说明两者的电离平衡常数 的变化曲线,说明两者的电离平衡常数 |
您最近一年使用:0次

 、Na+、
、Na+、
 、K+、
、K+、 、Br-
、Br- 溶液中:
溶液中: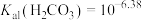 、
、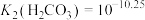 ,下列有关Na2CO3和NaHCO3混合溶液的说法正确的是
,下列有关Na2CO3和NaHCO3混合溶液的说法正确的是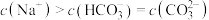
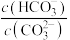 的值逐渐变小
的值逐渐变小 溶液,反应的离子方程式为
溶液,反应的离子方程式为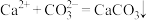
 时,
时,