沉淀的转化在生产中具有重要的应用价值。为了除去水垢中的 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是
已知: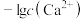 与
与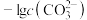 或
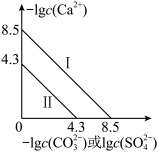
或 的关系如图所示,且
的关系如图所示,且 。
。
 ,可先用
,可先用 溶液处理,使
溶液处理,使 转化为疏松、易溶于酸的
转化为疏松、易溶于酸的 ,下列说法正确的是
,下列说法正确的是已知:
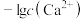 与
与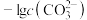 或
或 的关系如图所示,且
的关系如图所示,且 。
。
A. 中 中 的杂化轨道类型是 的杂化轨道类型是 |
B.反应 的平衡常数 的平衡常数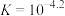 |
C. 中存在的化学键为 中存在的化学键为 键、 键、 键和范德华力 键和范德华力 |
D. 的 的 溶液中,一定存在 溶液中,一定存在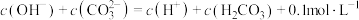 |
更新时间:2024-05-08 16:23:09
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.升高NaOH稀溶液的温度,溶液的pH值不变 |
B. 溶液中: 溶液中: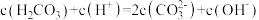 |
C.向 的 的 溶液中加入少量 溶液中加入少量 固体后, 固体后, 的值减小 的值减小 |
D. 溶液加水稀释后, 溶液加水稀释后,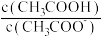 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用氨水吸收工厂烟气中的SO2时,溶液中H2SO3、 的物质的量分数
的物质的量分数 随pH的分布如图所示。下列叙述错误的是
随pH的分布如图所示。下列叙述错误的是

 的物质的量分数
的物质的量分数 随pH的分布如图所示。下列叙述错误的是
随pH的分布如图所示。下列叙述错误的是
A. |
| B.由图象可知,NaHSO3溶液显酸性 |
C.当溶液pH=6时,溶液中浓度最大的阴离子为 |
D.随着pH的变化,溶液中都有 |
您最近一年使用:0次
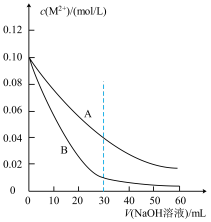
【推荐1】室温下,向20 mL含有0.10 mol/L 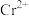 和0.10 mol/L
和0.10 mol/L  的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于
的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于 mol/L可视为沉淀完全;
mol/L可视为沉淀完全;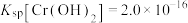 ,
,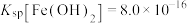 。则下列说法错误的是
。则下列说法错误的是
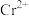 和0.10 mol/L
和0.10 mol/L  的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于
的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于 mol/L可视为沉淀完全;
mol/L可视为沉淀完全;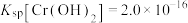 ,
,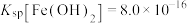 。则下列说法错误的是
。则下列说法错误的是
A.曲线A表示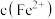 与V(NaOH溶液)的关系 与V(NaOH溶液)的关系 |
B.当pH=7时,溶液中 、 、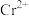 均沉淀完全 均沉淀完全 |
C.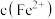 减小,并不能说明 减小,并不能说明 沉淀一定已开始生成 沉淀一定已开始生成 |
D.当两种离子均沉淀完全后,溶液中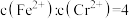 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】Ni2O3可用作制造人造卫星、宇宙飞船的高能电源。现以镍废料(主要含有Ni,还含有少量的Cu、Fe等)为原料制备Ni2O3,工艺流程如图所示。
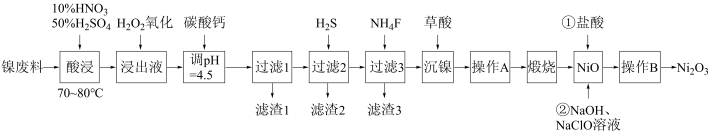
已知:常温下,0.01mol·L-1的金属离子形成氢氧化物沉淀时溶液的pH如表所示,当溶液中的离子浓度≤1.0×10-5mol·L-1时可认为沉淀完全。下列说法错误的是

已知:常温下,0.01mol·L-1的金属离子形成氢氧化物沉淀时溶液的pH如表所示,当溶液中的离子浓度≤1.0×10-5mol·L-1时可认为沉淀完全。下列说法错误的是
| Fe3+ | Cu2+ | Ni2+ | |
| 开始沉淀时的pH | 3.0 | 5.0 | 7.4 |
| 完全沉淀时的pH | 4.0 | 6.5 | 9.0 |
| A.由题中信息可知,常温下氢氧化镍的Ksp≈1.0×10-15 |
| B.生成Ni2O3的离子方程式为2Ni2++2H2O+ClO-=Ni2O3↓+Cl-+4H+ |
| C.滤渣1、滤渣2、滤渣3的主要成分分别为Fe(OH)3、CuS、CaF2 |
| D.操作A和操作B用到的主要玻璃仪器均为漏斗、烧杯、玻璃棒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是
| A.0.1molAgCl和0.1 molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
| B.常温下,向饱和CaCO3溶液中加入Na2CO3粉末,CaCO3的溶解度不变 |
| C.25 ℃时,Ksp[ Mg(OH)2 ]=5.61 × 10-12、Ksp(MgF2)=7.12 ×10-11,该温度下饱和 Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+) 大 |
| D.常温下Ksp(Ag2SO4)=1. 4× 10-5,向10mL 0.1mol/L的Na2SO4溶液中加入10 mL0.1 mol/L的AgNO3溶液,有白色沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关共价键和键参数的说法不正确的是
A.1个乙烯( )分子中含有5个 )分子中含有5个 键和1个 键和1个 键 键 |
B.C—H键比Si—H键的键长更短,故 比 比 更稳定 更稳定 |
C. 、 、 、 、 三种分子的键角依次增大 三种分子的键角依次增大 |
| D.碳碳双键比碳碳单键的键能更大,故碳碳双键更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】CO与H2S反应可以制得COS,其化学方程式为 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是
 。NA为阿伏加德罗常数的值,下列有关说法正确的是
。NA为阿伏加德罗常数的值,下列有关说法正确的是A.2.8g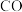 中含有的中子数为1.4NA 中含有的中子数为1.4NA |
B.pH=3的H2S溶液中 的数目为0.001NA 的数目为0.001NA |
C.0.1molCOS中 键数目为0.4NA 键数目为0.4NA |
| D.生成2.24LH2(标准状况),转移电子数目为0.4NA |
您最近一年使用:0次
【推荐1】醛生成亚胺的反应机理如图1,反应速率随pH的变化如图2。下列说法错误的是
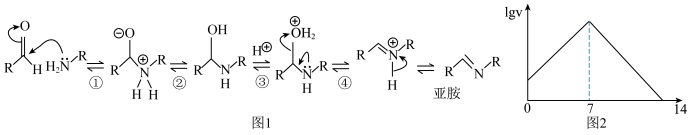
| A.酸性较强时,③为决速步;碱性较强时,①为决速步 |
| B.反应历程中,N原子的杂化方式有2种 |
| C.反应历程中,氧原子始终保持8电子稳定结构 |
| D.苯甲醛与羟胺(NH2—OH)反应的产物存在顺反异构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以 NA表示阿伏伽德罗常数的值,下列说法正确的是
A. 18g 冰中含 O﹣ H 键数目为 4NA 18g 冰中含 O﹣ H 键数目为 4NA |
B.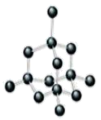 28g 晶体硅中含有σ键数目为 4NA 28g 晶体硅中含有σ键数目为 4NA |
C.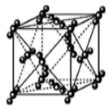 44g干冰中含有 0.25NA个晶胞结构单元 44g干冰中含有 0.25NA个晶胞结构单元 |
D.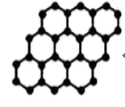 石墨烯是碳原子单层片状新材料,12g 石墨烯中含π键数目为 1.5NA 石墨烯是碳原子单层片状新材料,12g 石墨烯中含π键数目为 1.5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值,下列说法错误的是
| A.合成氨反应每生成标况下1.12 L氨气,转移的电子数为0.15NA |
| B.1L0.1mol/L的Na2CO3溶液中,阴、阳离子的总数大于0.3NA |
| C.NH5的结构类似于NH4Cl,则,1 mol NH5中所含σ键的数目为5NA |
| D.钢铁电化学腐蚀生成0.05 mol Fe2O3·nH2O,则负极反应失电子数为0.2NA |
您最近一年使用:0次

 溶液中逐滴加入
溶液中逐滴加入 氨水,所得溶液
氨水,所得溶液 及导电能力变化如图所示。下列分析正确的是
及导电能力变化如图所示。下列分析正确的是

 、
、 、
、 、
、 点对应溶液中阳离子浓度最大的是
点对应溶液中阳离子浓度最大的是 的水解常数的数量级为
的水解常数的数量级为




