常温下,向 溶液中逐滴加入
溶液中逐滴加入 氨水,所得溶液
氨水,所得溶液 及导电能力变化如图所示。下列分析正确的是
及导电能力变化如图所示。下列分析正确的是

 溶液中逐滴加入
溶液中逐滴加入 氨水,所得溶液
氨水,所得溶液 及导电能力变化如图所示。下列分析正确的是
及导电能力变化如图所示。下列分析正确的是

A. 、 、 、 、 、 、 点对应溶液中阳离子浓度最大的是 点对应溶液中阳离子浓度最大的是 点 点 |
B.常温下, 的水解常数的数量级为 的水解常数的数量级为 |
C. 点和 点和 点对应溶液中,水的电离程度相等 点对应溶液中,水的电离程度相等 |
D. 点对应溶液中微粒浓度关系:c(R-)+2c(HR)=c(NH3·H2O) 点对应溶液中微粒浓度关系:c(R-)+2c(HR)=c(NH3·H2O) |
更新时间:2022-10-26 09:36:02
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】利用pH传感器和温度传感器探究0.1mol/L Na2SO3溶液的pH随溶液温度的变化,实验装置如图甲所示,升温和降温过程中溶液pH的变化分别如图乙、丙所示,下列说法不正确的是
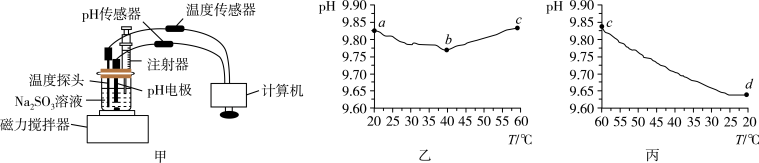
A.Na2SO3溶液中存在水解平衡:SO +H2O +H2O HSO HSO +OH- +OH- |
B.从a点到b点,pH下降的原因是SO 的水解和水的电离程度均增大,但前者更显著 的水解和水的电离程度均增大,但前者更显著 |
| C.d点pH低于a点的原因是部分Na2SO3被氧化成Na2SO4 |
| D.a点和d点的Kw值相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在25 ℃时,水中存在电离平衡:H2O⇌H++OH-,下列关于水的说法,正确的是
| A.水是极弱的电解质,水的电离是吸热过程,升温促进水的电离 |
| B.任何条件下水溶液中的c(H+)和c(OH-)的乘积均为1×10-14 |
| C.向水中加入盐类物质,水溶液一定是中性 |
| D.向水中加入少量稀硫酸,c(H+)增大,KW不变,促进水的电离 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知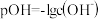 。向20mL
。向20mL 的氨水中滴加未知浓度的稀
的氨水中滴加未知浓度的稀 ,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如图所示,下列说法不正确的是
,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如图所示,下列说法不正确的是

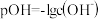 。向20mL
。向20mL 的氨水中滴加未知浓度的稀
的氨水中滴加未知浓度的稀 ,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如图所示,下列说法不正确的是
,测得混合溶液的温度、pOH随加入稀硫酸体积的变化如图所示,下列说法不正确的是
A.稀 的物质的量浓度为 的物质的量浓度为 |
B.a点时溶液中存在 |
C.c点对应的溶液 |
D.a、b、c三点对应 的水解平衡常数: 的水解平衡常数: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.01mol/L的NaOH溶液滴定某浓度的H2N2O2(二元弱酸)溶液,所得溶液中H2N2O2、HN2O 、N2O
、N2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。则下列说法中正确的是
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。则下列说法中正确的是

 、N2O
、N2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。则下列说法中正确的是
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。则下列说法中正确的是 
| A.该滴定过程应该选择甲基橙作为指示剂 |
| B.Ka1(H2N2O2)的数量级为10-4.2 |
| C.pH=1.2溶液中:c(Na+)+c(H+)=c(OH-)+c(H2N2O2) |
D.pH=4.2溶液中:c(Na+)>2c(N2O )+c(HN2O )+c(HN2O ) ) |
您最近一年使用:0次
【推荐3】25℃时,用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H3AO3溶液,溶液中所有含A微粒的分布分数δ(平衡时某含A微粒的浓度占各含A微粒浓度之和的分数)与pH的关系如图所示(已知100.2=1.58):
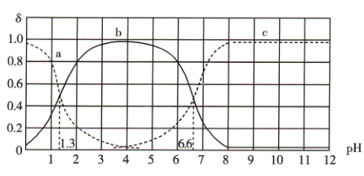
下列说法错误的是

下列说法错误的是
| A.H3AO3属于二元酸 |
| B.第一次滴定终点时可用甲基橙作指示剂 |
C.当溶液呈中性时,溶液中 约为6 约为6 |
D.当加入30mLNaOH溶液时,2c(Na+)=6c(HAO )+3c(H3AO3) )+3c(H3AO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关电解质溶液的说法正确的是
A.物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl、CH3COONH4溶液中c(NH ):(NH4)2SO4>CH3COONH4>NH4HSO4>NH4Cl ):(NH4)2SO4>CH3COONH4>NH4HSO4>NH4Cl |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
C.1.0mol·L-1Na2CO3溶液:c(OH-)=2c(HCO )+c(H+)+c(H2CO3) )+c(H+)+c(H2CO3) |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
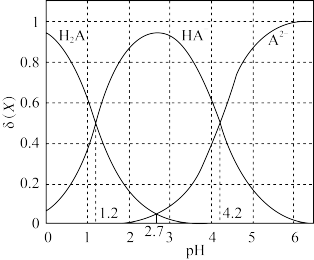
【推荐2】将0.1 mol/L二元弱酸H2A溶液与KOH溶液混合,H2A、HA-、A2-的物质的量分数 随体系pH的变化如图所示[已知
随体系pH的变化如图所示[已知 ]。下列叙述错误的是
]。下列叙述错误的是
 随体系pH的变化如图所示[已知
随体系pH的变化如图所示[已知 ]。下列叙述错误的是
]。下列叙述错误的是
| A.pH=1.2时,c(H2A)=c(HA-) |
| B.Ka2(H2A)=10-4.2 |
| C.KHA溶液中,c(HA-)>c(A2-)>c(H2A) |
| D.混合溶液始终存在c(K+)=c(HA-)+2c(A2-) |
您最近一年使用:0次

 )的
)的 ,
,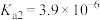 。该温度下,用
。该温度下,用 的
的 溶液滴定
溶液滴定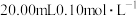 的邻苯二甲酸氢钾(
的邻苯二甲酸氢钾(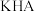 )溶液,溶液
)溶液,溶液
 点的混合溶液中:
点的混合溶液中:
 点的混合溶液中:
点的混合溶液中:

 点水的电离程度逐渐增大
点水的电离程度逐渐增大

