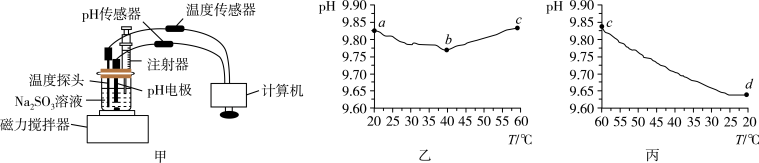
利用pH传感器和温度传感器探究0.1mol/L Na2SO3溶液的pH随溶液温度的变化,实验装置如图甲所示,升温和降温过程中溶液pH的变化分别如图乙、丙所示,下列说法不正确的是
A.Na2SO3溶液中存在水解平衡:SO +H2O +H2O HSO HSO +OH- +OH- |
B.从a点到b点,pH下降的原因是SO 的水解和水的电离程度均增大,但前者更显著 的水解和水的电离程度均增大,但前者更显著 |
| C.d点pH低于a点的原因是部分Na2SO3被氧化成Na2SO4 |
| D.a点和d点的Kw值相等 |
更新时间:2022-12-18 21:35:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关离子方程式或离子共存的叙述正确的是
| A.将磁性氧化铁溶于氢碘酸: Fe3O4+ 8H+= 2Fe3++ Fe2+ + 4H2O |
| B.用肥皂(主要成分C17H35COONa)检验含有较多钙离子的硬水:2C17H35COO-+Ca2+=(C17H35COO)2Ca↓ |
C.常温下,在 =0.1的溶液中:Na+、K+、AlO2-、HCO3-能大量共存 =0.1的溶液中:Na+、K+、AlO2-、HCO3-能大量共存 |
| D.在NaClO溶液中:SO32-、OH-、Cl-、K+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图示与对应的叙述相符的是


| A.由图甲可知,a点Kw的数值比b点Kw的数值大 |
| B.乙表示在相同的密闭容器中,不同温度下的反应,该反应的△H>0 |
| C.丙表示用0.100mol·L-1NaOH溶液滴定20.00mL0.10 mol·L-1醋酸溶液的滴定曲线 |
| D.根据图丁BaSO4在水中的沉淀溶解平衡曲线,d点无BaSO4沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关电解质溶液的说法正确的是( )
A.向K2S溶液中加水稀释, 会减小 会减小 |
| B.向醋酸溶液中滴加NaOH溶液至恰好完全反应,水的电离程度先增大后减小 |
| C.向含有MgCO3固体的溶液中加入少量盐酸,c(CO32-)会增大 |
D.向CuS和FeS的饱和溶液中加入少量Na2S, 保持不变 保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.加入酚酞为无色的溶液中: 、 、 、 、 、 、 |
B.澄清透明的溶液中: 、 、 、 、 、 、 |
C. 的 的 溶液中: 溶液中: 、 、 、 、 、 、 |
D.水电离的 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加 德罗常数的值,下列说法正确的是( )
| A.1L 0.1mol·L-1的Na2CO3溶液中所含氧原子数目为0.3NA |
| B.1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| C.将1L 0.1mol•L-1 FeCl3溶液滴入沸水中,制得的Fe(OH)3胶粒数目为0.1NA |
| D.常温下,NH4+数目:1L 0.5mol•L-1NH4Cl溶液等于2L 0.25mol•L-1NH4Cl溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,下列关于电解质溶液的说法中不正确的是
A.将 的氨水与 的氨水与 的硝酸等体积混合: 的硝酸等体积混合: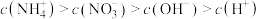 |
B.室温下,调节 溶液的 溶液的 时, 时,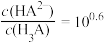 (已知:Ka1=10-2.2、Ka2=10-7.2、Ka3=10-12.4) (已知:Ka1=10-2.2、Ka2=10-7.2、Ka3=10-12.4) |
C. 时, 时, 的平衡常数 的平衡常数 [该温度下,Ksp(MS)=1.0×10-21、Ksp(RS)=4.0×10-18] [该温度下,Ksp(MS)=1.0×10-21、Ksp(RS)=4.0×10-18] |
D.加水稀释氯化铝溶液,铝离子水解程度增大, 物质的量增加,溶液酸性增强 物质的量增加,溶液酸性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物 ,Y 和Z最外层电子数之和与W的最外层电子数相同.
,Y 和Z最外层电子数之和与W的最外层电子数相同. 时
时 和W形成化合物的水溶液pH为
和W形成化合物的水溶液pH为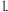 下列说法正确的是
下列说法正确的是
 ,Y 和Z最外层电子数之和与W的最外层电子数相同.
,Y 和Z最外层电子数之和与W的最外层电子数相同. 时
时 和W形成化合物的水溶液pH为
和W形成化合物的水溶液pH为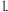 下列说法正确的是
下列说法正确的是A.Y和其它四种元素均可形成至少两种化合物 两种元素组成 两种元素组成 |
B.原子半径由大到小排列的顺序是: |
| C.在Z、Y形成的两种离子化合物中阴阳离子的个数比均为2:1 |
| D.Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某二元酸(H2A)按如下方式发生一级和二级电离:HA=H++HA-;HA-⇌H++A2-,测得25℃时,0.10mol/L的H2A溶液中c(H+)=0.11 mol/L,下列说法正确的是
| A.该条件下,HA-的电离度是9.1% |
| B.Na2A溶液显碱性,因为A2-+H2O⇌HA-+OH- |
| C.将NaHA固体溶于水中,可以促进水的电离 |
| D.0.1 mol/L的NaHA溶液中各离子的浓度大小顺序是:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究化学反应是否可逆 | 向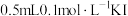 溶液中滴加1~2滴 溶液中滴加1~2滴 的 的 溶液,充分反应后,滴入1~2滴 溶液,充分反应后,滴入1~2滴 的 的 溶液,生成黄色沉淀 溶液,生成黄色沉淀 |
| B | 探究浓度对盐类水解平衡的影响 | 向滴有酚酞的碳酸钠溶液中滴加氯化钡溶液,观察现象 |
| C | 比较AgI和AgCl溶度积大小 | 向 的硝酸银溶液中先滴加2~3滴浓度为 的硝酸银溶液中先滴加2~3滴浓度为 的NaCl溶液,再滴加2~3滴相同浓度的NaI溶液,观察生成沉淀的颜色 的NaCl溶液,再滴加2~3滴相同浓度的NaI溶液,观察生成沉淀的颜色 |
| D | 比较HClO和 酸性强弱 酸性强弱 | 用pH试纸测定NaClO溶液和 溶液的pH 溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 =10﹣12mol•L﹣1的溶液中:Na+、K+、SiO
=10﹣12mol•L﹣1的溶液中:Na+、K+、SiO 、Cu2+、NO
、Cu2+、NO

 下,测定纯水和
下,测定纯水和 溶液的
溶液的
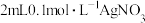 溶液中先滴加4滴
溶液中先滴加4滴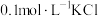 溶液,再滴加4滴
溶液,再滴加4滴 溶液
溶液 溶解度小于
溶解度小于 溶解度
溶解度 溶液中加入
溶液中加入 溶液
溶液 结合
结合 减小
减小 的番茄汁中
的番茄汁中 是
是 的牛奶中
的牛奶中
 升温至
升温至 ,溶液中
,溶液中 增大
增大

