氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。工业ZnO中含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ),纯化工业ZnO的流程如下:
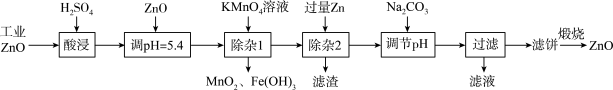
提示:在本实验条件下,Ni(Ⅱ)不能被氧化。
(1)“酸浸”时需不断通入高温水蒸气,其目的是________________ 。
(2)“除杂I”中生成Fe(OH)3反应的离子方程式为______________________________ 。
(3)“除杂2”中所得滤渣主要成分是____________ 。
(4)滤饼要用水洗,检验是否洗涤干净的方法是_________________ 。
(5)已知:Zn(OH)2的Ksp=l×10-17。室温下为使Zn2+完全沉淀(其浓度<1×10-5mol·L-1),需调节溶液pH范围为____________ 。

提示:在本实验条件下,Ni(Ⅱ)不能被氧化。
(1)“酸浸”时需不断通入高温水蒸气,其目的是
(2)“除杂I”中生成Fe(OH)3反应的离子方程式为
(3)“除杂2”中所得滤渣主要成分是
(4)滤饼要用水洗,检验是否洗涤干净的方法是
(5)已知:Zn(OH)2的Ksp=l×10-17。室温下为使Zn2+完全沉淀(其浓度<1×10-5mol·L-1),需调节溶液pH范围为
更新时间:2020-02-18 11:00:59
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】碱式氧化镍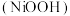 为镍氢电池的正极材料。黄钠铁矾的化学式为
为镍氢电池的正极材料。黄钠铁矾的化学式为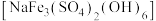 被用做净水剂。用含镍废渣(主要成分为
被用做净水剂。用含镍废渣(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
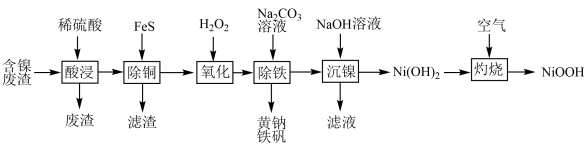
已知:部分金属硫化物的溶度积常数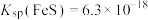 ;
;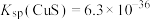 ;
;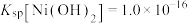 ,回答下列问题:
,回答下列问题:
(1)Fe元素在周期表的位置__________________________ 。
(2)“酸浸”后所得废渣的主要成分为__________ (填“化学式”);除铜步骤的离子方程式为_________________ 。
(3)“氧化”时,若用稀硝酸代替过氧化氢氧化 ,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是
,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是______________________ 。
(4)加入 溶液调节pH为3.7生成黄钠铁矾的离子方程式
溶液调节pH为3.7生成黄钠铁矾的离子方程式___________________ 。
(5)“沉镍”时,要使镍尽可能沉淀完全需调节溶液pH至少为___________ 。
(6)“灼烧”反应过程中氧化剂与还原剂的物质的量之比为_____________ 。
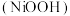 为镍氢电池的正极材料。黄钠铁矾的化学式为
为镍氢电池的正极材料。黄钠铁矾的化学式为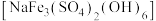 被用做净水剂。用含镍废渣(主要成分为
被用做净水剂。用含镍废渣(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
已知:部分金属硫化物的溶度积常数
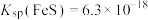 ;
; ;
;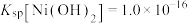 ,回答下列问题:
,回答下列问题:(1)Fe元素在周期表的位置
(2)“酸浸”后所得废渣的主要成分为
(3)“氧化”时,若用稀硝酸代替过氧化氢氧化
 ,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是
,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是(4)加入
 溶液调节pH为3.7生成黄钠铁矾的离子方程式
溶液调节pH为3.7生成黄钠铁矾的离子方程式(5)“沉镍”时,要使镍尽可能沉淀完全需调节溶液pH至少为
(6)“灼烧”反应过程中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】利用某钒废渣(主要成分为 、
、 、
、 、
、 、
、 等)制备
等)制备 的工艺流程如下:
的工艺流程如下: 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ. 。
。
回答下列问题:
(1)为加快“氧化1”速率,可以采取的措施有____________________ (写出一条即可),该过程发生反应的离子方程式为______________________________ 。
(2)滤渣2的主要成分为____________________ 。
(3)实验室进行萃取、分液操作时,需要的玻璃仪器有____________________ 。
(4)“氧化2”中发生反应的离子方程式为______________________________ 。
(5)“沉钒”前若滤液中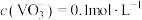 ,“沉钒”完成时,若上层清液中
,“沉钒”完成时,若上层清液中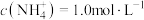 ,则钒元素的沉降率=
,则钒元素的沉降率=__________ %[ ,反应过程中溶液的体积不变]。
,反应过程中溶液的体积不变]。
(6)在Ar气氛中“煅烧” 生成
生成 ,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式______________________________ 。
 、
、 、
、 、
、 、
、 等)制备
等)制备 的工艺流程如下:
的工艺流程如下: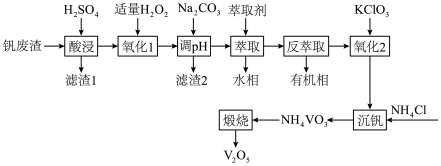
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
 。
。回答下列问题:
(1)为加快“氧化1”速率,可以采取的措施有
(2)滤渣2的主要成分为
(3)实验室进行萃取、分液操作时,需要的玻璃仪器有
(4)“氧化2”中发生反应的离子方程式为
(5)“沉钒”前若滤液中
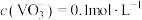 ,“沉钒”完成时,若上层清液中
,“沉钒”完成时,若上层清液中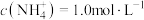 ,则钒元素的沉降率=
,则钒元素的沉降率= ,反应过程中溶液的体积不变]。
,反应过程中溶液的体积不变]。(6)在Ar气氛中“煅烧”
 生成
生成 ,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:
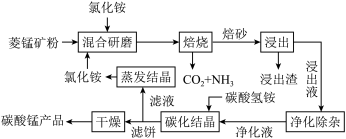
已知:①菱锰矿石主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素;
②常温下,CaF2、MgF2的溶度积分别为1.46×10-10、7.42×10-11
③相关金属离子c(Mn+)=0.1mol/L形成氯氧化物沉淀时的pH如下:
回答下列问题:
(1)“焙烧”时发生的主要化学反应方程式为______________________ 。
(2)分析下列图1、图2,氯化铵焙烧菱镁矿的最佳条件是:焙烧温度_________ ,氯化铵与菱镁矿粉的质量之比为_________ 。
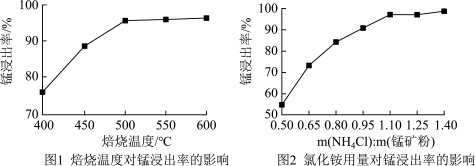
(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式______ ;然后调节溶液pH使Fe3+、Al3+沉淀完全,此时溶液的pH范围为_________ 。再加入NH4F沉淀Ca2+、Mg2+,当c(Ca2+)=1.0×10-5mol/L时,c(Mg2+)=______ mol/L
(4)碳化结晶时,发生反应的离子方程式为____________________________ 。
(5)流程中能循环利用的固态物质是____________ 。

已知:①菱锰矿石主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素;
②常温下,CaF2、MgF2的溶度积分别为1.46×10-10、7.42×10-11
③相关金属离子c(Mn+)=0.1mol/L形成氯氧化物沉淀时的pH如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
(1)“焙烧”时发生的主要化学反应方程式为
(2)分析下列图1、图2,氯化铵焙烧菱镁矿的最佳条件是:焙烧温度

(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式
(4)碳化结晶时,发生反应的离子方程式为
(5)流程中能循环利用的固态物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】由钛铁矿(主要成分是 ,含有少量
,含有少量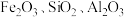 等杂质),制备
等杂质),制备 等产品的一种工艺流程如图:
等产品的一种工艺流程如图:
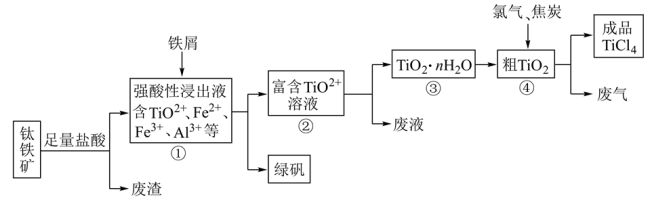
回答下列问题:
(1)用稀硫酸酸浸时,为使酸浸速率加快,可采取的措施是________________ (写1条即可).
(2)废渣的成分是__________________________ .(填化学式)
(3)②→③,加水稀释即可实现,其离子方程式为:____________________ .
(4)若将制得的固体 用酸清洗除去其中的
用酸清洗除去其中的 杂质,还可制得钛白粉.已知
杂质,还可制得钛白粉.已知 时,
时, ,
, ,则该温度下反应
,则该温度下反应 的平衡常数K的值为
的平衡常数K的值为____________________________ .
(5)废气主要为有毒气体,在高温下用 制备
制备 的化学方程式为
的化学方程式为___________________ .
 ,含有少量
,含有少量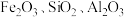 等杂质),制备
等杂质),制备 等产品的一种工艺流程如图:
等产品的一种工艺流程如图:
回答下列问题:
(1)用稀硫酸酸浸时,为使酸浸速率加快,可采取的措施是
(2)废渣的成分是
(3)②→③,加水稀释即可实现,其离子方程式为:
(4)若将制得的固体
 用酸清洗除去其中的
用酸清洗除去其中的 杂质,还可制得钛白粉.已知
杂质,还可制得钛白粉.已知 时,
时, ,
, ,则该温度下反应
,则该温度下反应 的平衡常数K的值为
的平衡常数K的值为(5)废气主要为有毒气体,在高温下用
 制备
制备 的化学方程式为
的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
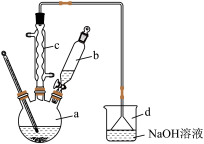
I.合成步骤:在a中加入15 mL无水苯和少量铁屑。在b中小心加入5.0 mL液溴。打开活塞,向a中滴入液溴,发生反应。请回答下列问题:
(1)仪器a的名称为_______ ,实验室制取溴苯的化学方程式为_______ 。
(2)反应过程中,仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为_______(填标号)。
(3)装置c的进水口在_______ (填”A”或”B”)。
(4)本实验中,仪器a的容积最适合的是_______(填标号)。
Ⅱ.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:
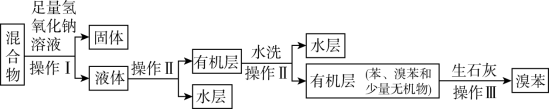
(5)流程中“固体”的化学式为_______ ,操作I所需主要玻璃仪器有_______ ,操作Ⅱ的名称是_______ 。
(6)设计实验检验水洗是否达到目的:_______ 。
(7)操作Ⅲ所需的玻璃仪器有_______ 。
A.分液漏斗 B.烧杯 C.蒸馏烧瓶 D.容量瓶 E.冷凝管 F.锥形瓶 G.胶头滴管 H.酒精灯 I.温度计 J.玻璃棒
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.20 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |

I.合成步骤:在a中加入15 mL无水苯和少量铁屑。在b中小心加入5.0 mL液溴。打开活塞,向a中滴入液溴,发生反应。请回答下列问题:
(1)仪器a的名称为
(2)反应过程中,仪器a外壁温度升高,为提高原料利用率可利用温度计控制温度,适宜的温度范围为_______(填标号)。
| A.>156°C | B.59°C - 80°C | C.<59°C | D.80°C- 156°C |
(4)本实验中,仪器a的容积最适合的是_______(填标号)。
| A.25 mL | B.50 mL | C.250 mL | D.500 mL |
Ⅱ.待反应完成后,取出a装置中的混合物,设计如下流程分离、提纯溴苯:

(5)流程中“固体”的化学式为
(6)设计实验检验水洗是否达到目的:
(7)操作Ⅲ所需的玻璃仪器有
A.分液漏斗 B.烧杯 C.蒸馏烧瓶 D.容量瓶 E.冷凝管 F.锥形瓶 G.胶头滴管 H.酒精灯 I.温度计 J.玻璃棒
您最近一年使用:0次
【推荐3】化工生产必须遵循科学原理。请根据下列工艺生产流程回答问题。
(1)某化学课外活动小组以海带为原料获得少量碘,其过程如下图所示:
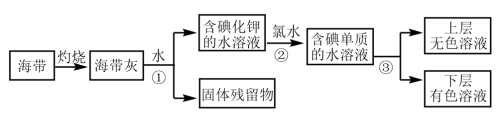
则:操作①的名称是_______ ,操作③使用的试剂(写化学式)_______ 。操作②中发生反应的离子方程式为_______ 。
(2)海水的综合利用可以制备金属钠和镁,其流程如下图所示:
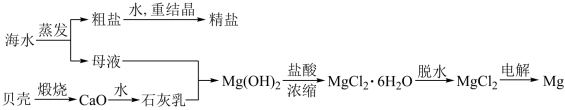
①上述流程中生成Mg(OH)2沉淀的离子方程式为_______ 。Mg(OH)2沉淀和盐酸反应的离子方程式为_______ 。
②实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:_______ ;过滤时:_______ ;蒸发时:_______ 。
③工业上把电解饱和食盐水称为“氯碱工业”。请你写出电解饱和食盐水的化学方程式_________ 。
(1)某化学课外活动小组以海带为原料获得少量碘,其过程如下图所示:

则:操作①的名称是
(2)海水的综合利用可以制备金属钠和镁,其流程如下图所示:

①上述流程中生成Mg(OH)2沉淀的离子方程式为
②实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:
③工业上把电解饱和食盐水称为“氯碱工业”。请你写出电解饱和食盐水的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯元素可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是________ ,a中的试剂为________ 。
(2)图中制备氯气的离子方程式为________________________________ 。
(3)b中发生的主要反应的化学方程式为________________________________ 。
(4)c采用冰水浴冷却的目的是________________________________ 。
(5)d用于处理尾气,可选用试剂________ (填标号)。
A.Na2S B.NaCl C.KOH D.Na2CO3

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)图中制备氯气的离子方程式为
(3)b中发生的主要反应的化学方程式为
(4)c采用冰水浴冷却的目的是
(5)d用于处理尾气,可选用试剂
A.Na2S B.NaCl C.KOH D.Na2CO3
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组在实验室制取Na2O2。查阅资料可知,钠与空气在453~473 K之间可生成Na2O,迅速提高温度到573~673 K之间可生成Na2O2,若温度提高到733~873 K之间Na2O2可分解。除Li外其他碱金属不与N2反应。
(1)甲组设计制取Na2O2装置如图。
①使用该装置制取的Na2O2中可能含有的杂质为________ 。
A.Na3N B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的Na2O2样品的纯度,设计装置如下:
烧瓶中发生的主要反应的化学方程式是______________________ 。分液漏斗和烧瓶用导管连接可使稀硫酸顺利流下,也可防止产生实验误差,若没有该导管将导致测定结果________ (填“偏大”“偏小”或“无影响”)。测定装置的接口从左至右正确的连接顺序是________ 。
(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果________ (填“偏大”或“偏小”)。为证明其分析的正确性,设计实验方案如下:
在上述实验中,能够证明乙组分析正确的最佳方案是____ (填实验序号)。根据上述实验可知,反应溶液中存在的中间产物与酚酞作用的条件是____________________ 。
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需要测定的有关数据_________________________________________________________________ 。
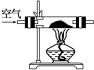
(1)甲组设计制取Na2O2装置如图。
①使用该装置制取的Na2O2中可能含有的杂质为
A.Na3N B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的Na2O2样品的纯度,设计装置如下:
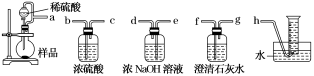
烧瓶中发生的主要反应的化学方程式是
(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果
| 实验方案 | 产生的现象 |
| Ⅰ.取烧瓶中的反应液加入少量MnO2粉末 | 有大量气泡逸出 |
| Ⅱ.向NaOH稀溶液中加入2~3滴酚酞溶液,然后加入少量的反应液 | 溶液先变红后褪色 |
| Ⅲ.向反应液中加入2~3滴酚酞溶液,充分振荡,然后逐滴加入过量的NaOH稀溶液 | 开始无明显现象,加NaOH溶液先变红后褪色 |
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需要测定的有关数据
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如图工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
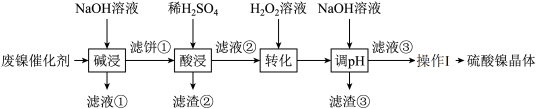
溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是_________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式________ 。
(2)“滤液②”中含有的金属离子是_______ 。
(3)“转化”中发生的离子方程式为_______ ,若工艺流程改为先“调pH”后“转化”,即:
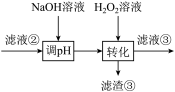
“滤液③”中可能含有的杂质离子为_________ 。
(4)“转化”后加NaOH溶液“调pH”应控制的pH范围是_____ ;操作Ⅰ的具体操作是_____ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式________ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH | 6.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是
(3)“转化”中发生的离子方程式为

“滤液③”中可能含有的杂质离子为
(4)“转化”后加NaOH溶液“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
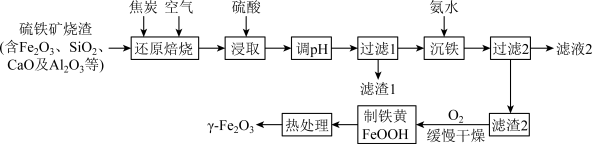
【推荐1】r—Fe2O3是一种具有磁性、催化、气敏的纳米材料。一种以硫铁矿烧渣等为原料制备r—Fe2O3的流程如下:
(1)下列有关“还原焙烧”工序的说法正确的是_____ (填字母)。
a.焦炭应少量,空气应过量
b. 焙烧过程均为吸热反应,需用电炉持续加热反应器
c.“还原焙烧”的主要反应为 3C+2O2 2CO+CO2、Fe2O3+CO
2CO+CO2、Fe2O3+CO 2FeO+CO2
2FeO+CO2
(2)“浸取”前需将焙烧生成的熔体粉碎,其目的是_____________________ 。
(3)已知三种金属离子开始沉淀和完全沉淀的pH如下表:
则“调pH”时,溶液的pH范围为_______________ 。
(4)滤渣1的主要成分为_________ (填化学式);“沉铁”时发生反应的离子方程式为___________ 。
(5)“过滤2”时需用蒸馏水洗涤,能证明沉淀已洗涤干净的方法是_________ ;沉淀缓慢氧化为铁黄的化学方程式为________________ 。
(1)下列有关“还原焙烧”工序的说法正确的是
a.焦炭应少量,空气应过量
b. 焙烧过程均为吸热反应,需用电炉持续加热反应器
c.“还原焙烧”的主要反应为 3C+2O2
 2CO+CO2、Fe2O3+CO
2CO+CO2、Fe2O3+CO 2FeO+CO2
2FeO+CO2(2)“浸取”前需将焙烧生成的熔体粉碎,其目的是
(3)已知三种金属离子开始沉淀和完全沉淀的pH如下表:
| Fe3+ | Fe2+ | Al3+ | |
| 开始沉淀的pH | 2.2 | 7.5 | 4.1 |
| 完全沉淀的pH | 3.5 | 9.5 | 5.4 |
(4)滤渣1的主要成分为
(5)“过滤2”时需用蒸馏水洗涤,能证明沉淀已洗涤干净的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,极易水解,遇潮湿空气会产生白雾。
(1)化合物SO2Cl2中S元素的化合价是__________ 。
(2)实验室中制备氯气时为得到干燥纯净的氯气,应将气体依次通过盛有_______ 和_______ 的洗气瓶。
(3)用如图所示装置制备SO2Cl2。
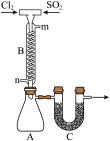
①B中冷凝水从__________ (填“m”或“n”)口进入。
②C中的药品是______ 。目的一是吸收外界空气中的水蒸气,目的二是:_______________ 。
③向A所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl-,写出SO2Cl2与H2O反应的化学方程式:_______________ 。
查阅资料:SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,极易水解,遇潮湿空气会产生白雾。
(1)化合物SO2Cl2中S元素的化合价是
(2)实验室中制备氯气时为得到干燥纯净的氯气,应将气体依次通过盛有
(3)用如图所示装置制备SO2Cl2。

①B中冷凝水从
②C中的药品是
③向A所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl-,写出SO2Cl2与H2O反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硒(Se)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取而得。
(1)硒在元素周期表中的位置如图所示:
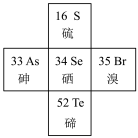
①Se在元素周期表中位置表示为___________ ;
②写出 的电子式:
的电子式:___________ 。
(2)阳极泥中的硒主要以 和
和 的形式存在,工业上提取硒的流程如下:
的形式存在,工业上提取硒的流程如下:
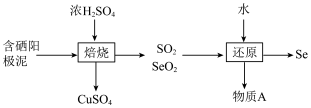
①请写出 与浓
与浓 反应的化学方程式:
反应的化学方程式:___________ 。
(2)物质A是___________ (填化学式)。
(3)下列说法正确的是___________。
(1)硒在元素周期表中的位置如图所示:

①Se在元素周期表中位置表示为
②写出
 的电子式:
的电子式:(2)阳极泥中的硒主要以
 和
和 的形式存在,工业上提取硒的流程如下:
的形式存在,工业上提取硒的流程如下:
①请写出
 与浓
与浓 反应的化学方程式:
反应的化学方程式:(2)物质A是
(3)下列说法正确的是___________。
A. 既有氧化性又有还原性 既有氧化性又有还原性 | B.原子半径由大到小顺序: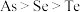 |
C.热稳定性: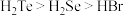 | D.酸性: |
您最近一年使用:0次



