现有a mol/L NaX和b mol/L NaY两种盐溶液。下列说法正确的是
| A.若a=b且c(X-)=c(Y-)+c(HY),则HX为强酸 |
| B.若a=b且pH(NaX)>pH(NaY),则c(X-)+c(OH-)>c(Y-)+c(OH-) |
| C.若a>b且c(X-)=c(Y-),则酸性HX>HY |
| D.若两溶液等体积混合,则c(Na+)=(a+b)mol/L |
15-16高三下·云南玉溪·阶段练习 查看更多[11]
山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题选择性必修1(SJ)专题3专题综合检测人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过综合 章末素养综合检测吉林省梅河口市第五中学2020-2021学年高二上学期第二次月考化学试题浙江省杭州市滨江区杭州第二中学2020年高中化学选修4专题3检测题(已下线)2018年11月11日——《每日一题》 人教 必修4-每周一测江西省金溪一中、余江一中等五市八校2018届高三上学期第一次联考化学试题2018届高三一轮复习化学:微考点62-攻克盐类水解平衡2015-2016学年河北省定州中学高二下期末化学试卷22015-2016学年河北省定州中学高二下期末化学试卷12016届云南省玉溪一中高三下第七次月考理综化学试卷
更新时间:2020-03-05 19:35:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述正确的是
| A.常温下,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.中和热测定实验中用到的玻璃仪器有烧杯、量筒、环形玻璃搅拌棒 |
| C.MgCl2·6H2O受热时发生水解,而 MgSO4·7H2O受热不易发生水解 |
| D.常温下,中和pH与体积均相同的硫酸和醋酸,消耗NaOH的物质的量相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,pH=2的盐酸和醋酸溶液各1mL分别加水稀释,pH随溶液体积变化的曲线如图所示。下列说法正确的是
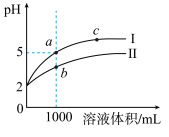

| A.曲线Ⅰ代表醋酸溶液的稀释过程 |
| B.a点溶液的导电性比c点溶液的导电能力差 |
C.与足量的锌反应,最终盐酸产生 的量较多 的量较多 |
| D.与相同浓度的NaOH溶液恰好中和时,醋酸消耗的NaOH溶液的体积大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】与水一样,甲醇也能微弱电离:2CH3OH(l) CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
 CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )| A.金属钠与甲醇反应比金属钠与水反应更剧烈 |
| B.结合H+的能力CH3O-<OH- |
| C.所得到溶液中K=c(CH3O-)×c(CH3OH2+) |
| D.所得到溶液中c(Na+)=c(CH3OH2+) + c(CH3O-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列叙述正确的是
| A.常温下,10 mL 0.02 mol•L-1 HCl溶液与10 mL 0.02 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
| B.常温下,向AgCl的饱和溶液中加入NaCl固体,有固体析出,且AgCl的Ksp变小 |
| C.在0.1 mol•L-1 CH3COONa溶液中,c(OH-)>c(CH3COOH)+c(H+) |
| D.常温下pH = 4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A. 中含有的中子数为 中含有的中子数为 |
| B.80gNaOH溶解在1L水中,所得溶液物质的量浓度为2mol/L |
C.1L0.1mol/L碳酸钠溶液中碳酸根离子数小于 |
D.标况下22.4L 中含有的分子数等于 中含有的分子数等于 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下, 溶液显酸性,溶液中部分离子浓度随
溶液显酸性,溶液中部分离子浓度随 浓度的变化如图所示。下列关系式一定正确的是
浓度的变化如图所示。下列关系式一定正确的是

 溶液显酸性,溶液中部分离子浓度随
溶液显酸性,溶液中部分离子浓度随 浓度的变化如图所示。下列关系式一定正确的是
浓度的变化如图所示。下列关系式一定正确的是
A. |
B.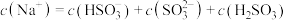 |
C. |
D. 时, 时, |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用一定浓度的 溶液分别滴定体积均为
溶液分别滴定体积均为 ,浓度均为
,浓度均为 的
的 、
、 和
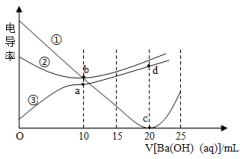
和 三种溶液。滴定过程中溶液的电导率如图所示(溶液电导率越大,导电能力越强;b点为曲线②上的点)。下列说法正确的是
三种溶液。滴定过程中溶液的电导率如图所示(溶液电导率越大,导电能力越强;b点为曲线②上的点)。下列说法正确的是
 溶液分别滴定体积均为
溶液分别滴定体积均为 ,浓度均为
,浓度均为 的
的 、
、 和
和 三种溶液。滴定过程中溶液的电导率如图所示(溶液电导率越大,导电能力越强;b点为曲线②上的点)。下列说法正确的是
三种溶液。滴定过程中溶液的电导率如图所示(溶液电导率越大,导电能力越强;b点为曲线②上的点)。下列说法正确的是
A.曲线①②③分别代表 滴定醋酸、盐酸和硫酸的曲线 滴定醋酸、盐酸和硫酸的曲线 |
B.d点对应的溶液中粒子浓度大小关系: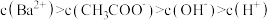 |
C. 浓度为 浓度为 ,且a、b、c、d点 ,且a、b、c、d点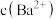 : :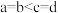 |
D.水的电离程度随 溶液的滴加,先增大后减小,且 溶液的滴加,先增大后减小,且 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,已知Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11,某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是


| A.H2R的一级电离常数Ka1的数量级为10-5 |
| B.在pH=4的溶液中:3c(R2-)<c(Na+)+c(H+)-c(OH-) |
| C.等体积、等浓度的NaOH与H2R溶液混合后,溶液中:c(R2-)<c(H2R) |
D.向Na2CO3溶液中加入过量H2R溶液,发生的反应是:CO + H2R=CO2↑+H2O+R2- + H2R=CO2↑+H2O+R2- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法不正确 的是
 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法A. 氯化铵水溶液中 氯化铵水溶液中 与 与 数目之和大于 数目之和大于 |
B.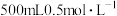 的 的 溶液中微粒数大于 溶液中微粒数大于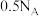 |
C. 与 与 混合物中含C原子数为 混合物中含C原子数为 |
D. 与 与 完全反应,反应中转移的电子数介于 完全反应,反应中转移的电子数介于 和 和 之间 之间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,向25 mL 0.100 0 mol • L-l的BOH溶液中逐滴滴入同浓度的一元弱酸HA的溶液,所得溶液PH与加入HA溶液的体积的关系曲线如图所示,则下列说法正确的是( )


| A.BOH的电离方程式为BOH =B++OH- |
| B.可选择酚酞作指示剂,滴定终点时,溶液恰好在B点从无色变为粉红色,且30秒内不恢复原色 |
| C.Ka(HA)<Kb(BOH) |
| D.加入HA溶液的体积为50 ml时,c(B+)+2c(BOH)+c(OH-)=c(HA)+c(H+) |
您最近一年使用:0次

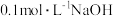 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的HA、HB两种酸的溶液,滴定过程中溶液的
的HA、HB两种酸的溶液,滴定过程中溶液的 随滴入的
随滴入的 溶液体积的变化如图所示(忽略溶液体积变化)。下列说法不正确的是
溶液体积的变化如图所示(忽略溶液体积变化)。下列说法不正确的是



 溶液中
溶液中 ,则往
,则往 溶液中滴入少量
溶液中滴入少量
 ) > c(
) > c( ) > c(
) > c( ) > c(
) > c(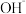 ) = c(
) = c( )
)
 )
)

