一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
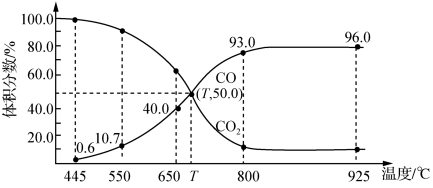
已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
已知:气体分压(p分)=气体总压(p总)×体积分数。下列说法正确的是
| A.650 ℃时,反应达平衡后 CO2的转化率为 25.0% |
| B.550 ℃时,若充入惰性气体,v(正)、v(逆)均减小,平衡不移动 |
| C.T ℃时,若充入等体积的 CO2 和 CO,平衡向正反应方向移动 |
| D.925 ℃时,用平衡分压代替平衡浓度表示的化学平衡常数 Kp=24.0p总 |
19-20高三下·天津河西·阶段练习 查看更多[2]
更新时间:2020/04/03 15:46:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在373K时,把0.5mol  气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时,
气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时, 的浓度为0.02mol/L。在60秒时,体系已达到平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
的浓度为0.02mol/L。在60秒时,体系已达到平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
 气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时,
气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时, 的浓度为0.02mol/L。在60秒时,体系已达到平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是
的浓度为0.02mol/L。在60秒时,体系已达到平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是A.前2秒,以 的浓度变化表示的平均反应速率为0.01mol/(L·s) 的浓度变化表示的平均反应速率为0.01mol/(L·s) |
| B.在2秒时体系内的压强为开始时的1.2倍 |
C.在平衡时体系内含 0.20mol 0.20mol |
D.平衡时,如果再充入一定量 ,则可提高 ,则可提高 的转化率 的转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知室温下, 的电离常数:
的电离常数: ,
, 。工业上,用饱和
。工业上,用饱和 溶液吸收水煤气中的
溶液吸收水煤气中的 ,回收和利用
,回收和利用 ,可以提纯
,可以提纯 和CO,有助于“双碳达标”。下列有关推理错误的是:
和CO,有助于“双碳达标”。下列有关推理错误的是:
 的电离常数:
的电离常数: ,
, 。工业上,用饱和
。工业上,用饱和 溶液吸收水煤气中的
溶液吸收水煤气中的 ,回收和利用
,回收和利用 ,可以提纯
,可以提纯 和CO,有助于“双碳达标”。下列有关推理错误的是:
和CO,有助于“双碳达标”。下列有关推理错误的是:A. 的平衡常数 的平衡常数 |
B.一定条件下,加热吸收 后溶液可使“吸收液”再生并回收 后溶液可使“吸收液”再生并回收 |
C.若吸收 后溶液中 后溶液中 ,则溶液pH=10 ,则溶液pH=10 |
D.饱和 溶液吸收 溶液吸收 后可能析出晶体 后可能析出晶体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐3】已知:N2(g)+3H2(g) 2NH3(g) △H=-92kJ/mol。起始反应物为
2NH3(g) △H=-92kJ/mol。起始反应物为 和
和 ,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中
,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中 的物质的量分数如下表:
的物质的量分数如下表:
下列说法正确的是
 2NH3(g) △H=-92kJ/mol。起始反应物为
2NH3(g) △H=-92kJ/mol。起始反应物为 和
和 ,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中
,物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中 的物质的量分数如下表:
的物质的量分数如下表:| 温度 压强 | 400℃ | 450℃ | 500℃ | 600℃ |
| 20MPa | 0.387 | 0.274 | 0.189 | 0.088 |
| 30MPa | 0.478 | 0.359 | 0.260 | 0.129 |
A.体系中 的物质的量分数越大,则正反应速率越大 的物质的量分数越大,则正反应速率越大 |
B.反应达到平衡时, 和 和 的转化率之比为1∶1 的转化率之比为1∶1 |
| C.反应达到平衡时,放出的热量均为92.4kJ |
D.600℃,30MPa下反应达到平衡时,生成 的物质的量最多 的物质的量最多 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】300℃时,将2molX和2molY两种气体混合于2L密闭容器中,发生如下反应: ,2min末达到平衡,生成0.8molW。下列说法错误的是
,2min末达到平衡,生成0.8molW。下列说法错误的是
 ,2min末达到平衡,生成0.8molW。下列说法错误的是
,2min末达到平衡,生成0.8molW。下列说法错误的是| A.300℃时,该反应的平衡常数K=0.5 |
B.在2min末时,Y的平衡浓度为0.8 |
C.0~2min,W的平均反应速率为0.2 |
| D.若温度不变,缩小容器容积,则X的转化率减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】COCl2(g) CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施能提高COCl2转化率的是( )
 CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施能提高COCl2转化率的是( )| A.降温 | B.增加CO的浓度 | C.恒容通入惰性气体 | D.恒压通入惰性气体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据下列实验操作和现象所得到的结论正确的是
 | 将 NO2 球浸泡在冷水和热水中2NO2(g)  N2O4(g) △H<0 N2O4(g) △H<0 | A.气体在热水中比在冷水中颜色浅 |
 | H2(g)+I2(g)  2HI(g) 2HI(g) | B.平衡体系加压后颜色先变深后变浅 |
 | 推动注射器活塞 | C.加压后气体颜色变深后不再变化 |
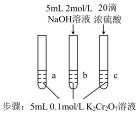 |  (aq)(橙色) + H2O(l) (aq)(橙色) + H2O(l)  2 2 (aq)(黄色)+ 2H+(aq) △H=+13.8 kJ/mol (aq)(黄色)+ 2H+(aq) △H=+13.8 kJ/mol | D.与a 颜色相比,b 溶液颜色变浅不能证明减小生成物浓度使平衡正向移动;c 溶液颜色变深能证明增加生成物浓度平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



