1 . 常温下,向 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: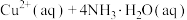

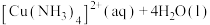 ,溶液中
,溶液中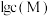 与
与 的关系如图所示,其中
的关系如图所示,其中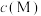 表示
表示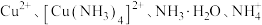 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是
 饱和溶液[有足量
饱和溶液[有足量 固体]中滴加氨水,发生反应:
固体]中滴加氨水,发生反应: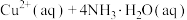

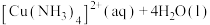 ,溶液中
,溶液中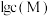 与
与 的关系如图所示,其中
的关系如图所示,其中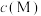 表示
表示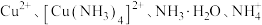 的浓度,单位为
的浓度,单位为 。下列说法正确的是
。下列说法正确的是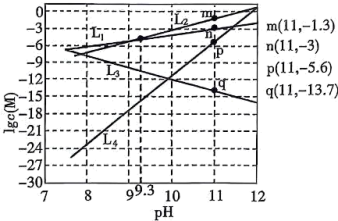
A. 表示溶液中 表示溶液中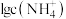 与 与 的关系 的关系 |
B. 的溶度积常数 的溶度积常数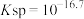 |
C. 时,溶液中: 时,溶液中: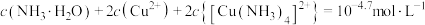 |
D.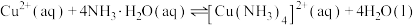 的平衡常数 的平衡常数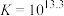 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
2 . 一种湿法炼铜法为用稀硫酸溶解孔雀石[主要成分为Cu2(OH)2CO3],再向其中加入铁屑可得铜。下列有关说法正确的是
| A.Cu2(OH)2CO3属于碱 |
B.CuSO4溶液中c(Cu2+)<c(SO ) ) |
| C.用Cu2(OH)2CO3炼铜的两个反应都是氧化还原反应 |
| D.常温下,CuSO4溶液能使蛋白质发生盐析 |
您最近半年使用:0次
名校
解题方法
3 . 类比是一种重要的学习方法,下列“类比”中错误的是
A.电解熔融 可制 可制 ,则电解熔融 ,则电解熔融 可制 可制 |
B.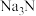 与盐酸反应生成 与盐酸反应生成 和 和 ,则 ,则 与盐酸反应生成 与盐酸反应生成 和 和 |
C. 溶液与少量 溶液与少量 溶液反应生成 溶液反应生成 和 和 ,则氨水与少量 ,则氨水与少量 溶液反应生成 溶液反应生成 和 和 |
D. 与 与 在溶液中可发生相互促进的水解反应生成沉淀和气体, 在溶液中可发生相互促进的水解反应生成沉淀和气体, 与 与 也如此 也如此 |
您最近半年使用:0次
昨日更新
|
31次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期二模化学试题
4 . 用0.1 NaOH标准溶液滴定20mL等浓度的三元酸
NaOH标准溶液滴定20mL等浓度的三元酸 ,得到pH与
,得到pH与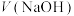 、
、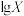 [
[ 或
或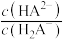 或
或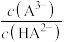 ]的关系分别如图1、图2所示。
]的关系分别如图1、图2所示。
 NaOH标准溶液滴定20mL等浓度的三元酸
NaOH标准溶液滴定20mL等浓度的三元酸 ,得到pH与
,得到pH与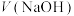 、
、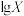 [
[ 或
或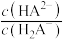 或
或 ]的关系分别如图1、图2所示。
]的关系分别如图1、图2所示。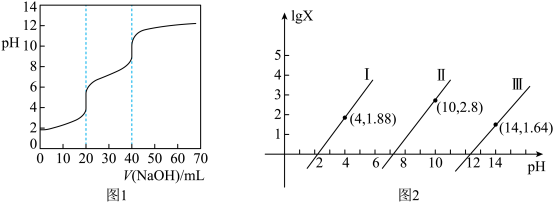
A.当加入20mL NaOH溶液时,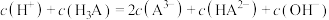 |
B.当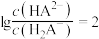 时,水电离出的 时,水电离出的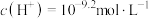 |
C.当加入40mL NaOH溶液时, |
D.当pH=11时,溶液中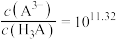 |
您最近半年使用:0次
5 . 常温下,向 溶液中逐滴加入
溶液中逐滴加入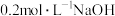 溶液,所得溶液的
溶液,所得溶液的 变化曲线如图所示。下列说法错误的是
变化曲线如图所示。下列说法错误的是
 溶液中逐滴加入
溶液中逐滴加入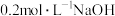 溶液,所得溶液的
溶液,所得溶液的 变化曲线如图所示。下列说法错误的是
变化曲线如图所示。下列说法错误的是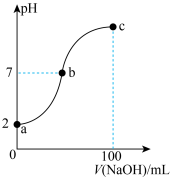
A.a点溶液中,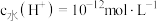 |
B.b点溶液中, |
C.常温下, |
| D.a、b、c三点溶液中,c点溶液中水的电离程度最小 |
您最近半年使用:0次
解题方法
6 . 研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1)25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入少量硫酸铵固体,则溶液中 将
将__________ (填“增大”“减小”或“不变”)。
②若向氨水中加入稀盐酸,使氨水恰好被中 和,则此时溶液显___________ (填“酸性”“碱性”或“中性”),用离子方程式表示其原因_________________ ,此溶液中离子的浓度大小顺序为___________
③在浓度为 的氨水中加入等体积
的氨水中加入等体积 的
的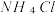 溶液,已知
溶液,已知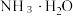 的电离常数为
的电离常数为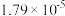 ,此时混合溶液显
,此时混合溶液显___________ (填“酸性”“碱性”或“中性”),此溶液中离子的浓度大小顺序为 ______
(2)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
①上述四种酸酸性由强到弱的顺序为___________ ;
②将少量的CO2通入NaClO溶液中,反应的离子方程式:___________ 。
(1)25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入少量硫酸铵固体,则溶液中
 将
将②若向氨水中加入稀盐酸,使氨水恰好被
③在浓度为
 的氨水中加入等体积
的氨水中加入等体积 的
的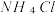 溶液,已知
溶液,已知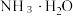 的电离常数为
的电离常数为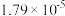 ,此时混合溶液显
,此时混合溶液显(2)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
| 化学式 | HCOOH | H2CO₃ | HCN | HClO |
| 电离平衡常数 | K=1.8×10⁻⁴ | K₁=4.3×10⁻⁷;K2=5.6×10⁻¹¹ | K=4.9×10⁻¹⁰ | K=4.7×10⁻⁸ |
②将少量的CO2通入NaClO溶液中,反应的离子方程式:
您最近半年使用:0次
2024·黑龙江·模拟预测
7 . 数字化实验是研究化学变化的重要手段,为验证次氯酸光照分解的产物,某同学采用三种传感器分别测得氯水光照过程中pH、Cl-浓度、 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是
 体积分数的变化,实验数据如图所示,下列叙述错误的是
体积分数的变化,实验数据如图所示,下列叙述错误的是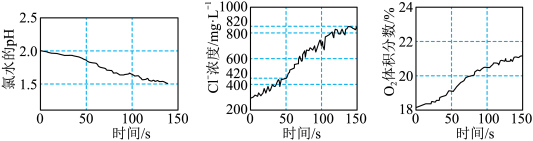
A.从0s到150s,溶液pH降低的原因是 右移 右移 |
B.氯水在光照过程中可能出现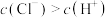 |
C.从50 s到150 s, 的平均生成速率约为 的平均生成速率约为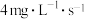 |
D.从0 s到150 s,溶液中 增加到起始浓度的 增加到起始浓度的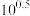 倍 倍 |
您最近半年使用:0次
名校
解题方法
8 . 室温下,通过下列实验探究0.0100mol/L Na2C2O4溶液的性质。
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
【实验1】用pH计测得该溶液pH=8.60。
【实验2】取5mL该溶液,滴加等体积等浓度稀盐酸。
【实验3】另取5mL该溶液,滴加等体积0.02mol/L CaCl2溶液,出现白色沉淀。已知室温下Ksp(CaC2O4)=2.5×10-9。
下列说法错误的是
A.该Na2C2O4溶液中满足: >2 >2 |
B.实验2滴加盐酸过程中可能存在;c(Na+ )= c( )+2c( )+2c( )+c(Cl-) )+c(Cl-) |
C.实验3所得上层清液中:c( )=5×10-7mol⋅L-1 )=5×10-7mol⋅L-1 |
D.实验3所得上层清液中:2c(Ca2+)+c(H+ )=c( )+2c( )+2c( )+0.02+c(OH-) )+0.02+c(OH-) |
您最近半年使用:0次
名校
解题方法
9 . 室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质。
已知: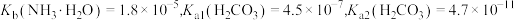 。
。
下列有关说法正确的是
已知:
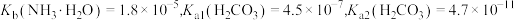 。
。| 实验 | 实验操作和现象 |
| 1 | 测量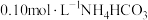 溶液的 溶液的 ,测得 ,测得 为 为 |
| 2 | 测量某浓度的 溶液的 溶液的 ,测得 ,测得 约为9.4 约为9.4 |
| 3 | 将两种浓度均为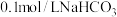 和 和 溶液等体积混合,测量其 溶液等体积混合,测量其 |
A.实验1溶液中: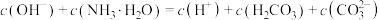 |
B.实验1测得的 值 值 |
C.实验2溶液中: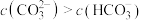 |
D.实验3所得溶液中: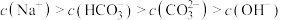 |
您最近半年使用:0次
名校
解题方法
10 . 在不同温度下,水溶液中 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是
 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是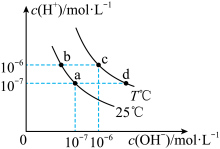
A.c点对应的溶液 ,溶液呈弱酸性 ,溶液呈弱酸性 |
B.b点对应的溶液中可以大量共存: 、 、 、 、 、 、 |
C.若a点表示 和 和 的混合溶液,则该溶液中的离子浓度大小为: 的混合溶液,则该溶液中的离子浓度大小为: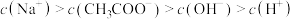 |
D.若d点表示某等浓度、等体积的 和 和 混合溶液,则溶液中的离子浓度存在如下关系: 混合溶液,则溶液中的离子浓度存在如下关系: |
您最近半年使用:0次



