名校
1 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,该
是硅的一种同位素,该 原子的中子数为
原子的中子数为_______ 。
(2)硅元素在自然界中通常以石英石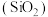 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式_______ 。
(3)关于硅及其相关化合物的叙述正确的是_______(填字母)。
(4)高纯硅单质可由石英砂(主要成分是 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:_______ ;
ⅱ.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,该
是硅的一种同位素,该 原子的中子数为
原子的中子数为(2)硅元素在自然界中通常以石英石
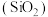 和硅酸盐的形式存在。已知
和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的离子方程式(3)关于硅及其相关化合物的叙述正确的是_______(填字母)。
| A.自然界中存在天然游离的硅单质 |
B.已知C与 的最高正价都是正四价,由于 的最高正价都是正四价,由于 ,用类比法得知, ,用类比法得知,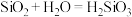 |
C.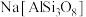 用氧化物形式表示为 用氧化物形式表示为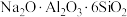 |
D. 既能和 既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物 溶液反应,又能和氢氟酸反应,所以是两性氧化物 |
 )制得,制备高纯硅的主要工艺流程如图所示:
)制得,制备高纯硅的主要工艺流程如图所示:
ⅱ.流程④的化学反应为置换反应,写出其化学方程式:
您最近半年使用:0次
名校
解题方法
2 . 地球上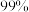 的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如图所示:
的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如图所示:
(2)如图流程中热空气吹出已经得到了粗溴,为什么还要添加“ 吸收、氧化、水蒸气吹出”三个步骤,其目的是
吸收、氧化、水蒸气吹出”三个步骤,其目的是___________ 。
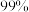 的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如图所示:
的溴元素分布在海洋中。空气吹出法工艺是目前“海水提溴”的主要方法之一,工艺流程如图所示:
| A.溴离子的还原性 | B.溴单质的还原性 | C.溴的沸点低 | D. 极易溶于水 极易溶于水 |
(2)如图流程中热空气吹出已经得到了粗溴,为什么还要添加“
 吸收、氧化、水蒸气吹出”三个步骤,其目的是
吸收、氧化、水蒸气吹出”三个步骤,其目的是
您最近半年使用:0次
名校
解题方法
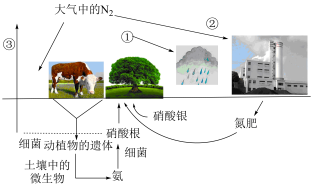
3 . 下图就是氮循环的简单示意图:
1.过程①是___________ 固氮, 性质之所以稳定是因为分子中含有
性质之所以稳定是因为分子中含有___________ 。过程②是人工固氮,化学方程式为:___________ 。
2.生产、生活中,与 的大量排放有关的环境问题是___________。
的大量排放有关的环境问题是___________。
3.下表是关于氮循环和硫循环的几种评价,其中正确的是___________。
1.过程①是
 性质之所以稳定是因为分子中含有
性质之所以稳定是因为分子中含有2.生产、生活中,与
 的大量排放有关的环境问题是___________。
的大量排放有关的环境问题是___________。| A.酸雨 | B. | C.温室效应 | D.白色污染 |
| 编号 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫循环不会进入大气 |
| B | 氮元素可以有机化合物形式参与循环 | 硫元素都以无机化合物形式参与循环 | |
| C | 同 | 人类活动对氮循环和硫循环都造成了巨大影响 | |
| D | 氮循环和硫循环对环境影响都导致温室效应 | ||
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 若将 和
和 等体积混合后再缓缓通入品红溶液,发现品红溶液
等体积混合后再缓缓通入品红溶液,发现品红溶液___________ ,其原因是___________ (用化学方程式解释原因)。
 和
和 等体积混合后再缓缓通入品红溶液,发现品红溶液
等体积混合后再缓缓通入品红溶液,发现品红溶液
您最近半年使用:0次
名校
5 . 大气固氮是在放电或高温下,空气中的 转化为
转化为 的过程。固氮过程中也会产生含氮化合物。
的过程。固氮过程中也会产生含氮化合物。___________ (填写化学式)。
2.上述转化关系中四种含氮物质中,含共价键的有___________ 种,属于共价化合物的有___________ 种。
3.写出过程②的反应方程式___________ 。
 转化为
转化为 的过程。固氮过程中也会产生含氮化合物。
的过程。固氮过程中也会产生含氮化合物。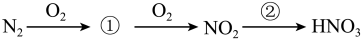
2.上述转化关系中四种含氮物质中,含共价键的有
3.写出过程②的反应方程式
您最近半年使用:0次
名校
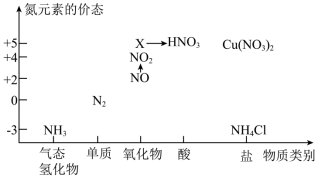
6 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。____________ 。
(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为______ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是____________ 。
(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即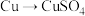
方案乙:由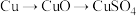
①方案甲中铜和浓硫酸反应的化学方程式是____________ 。该反应体现了浓硫酸的____________ 。
②这两种方案,你认为哪一种方案更合理?______ ,理由是____________ 。

(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
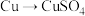
方案乙:由
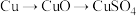
①方案甲中铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近半年使用:0次
名校
7 . 依据如图中氮元素及其化合物的转化关系,回答问题:_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:_______ 。
②用氨可将氮氧化物转化为无毒气体。如 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
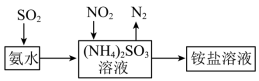
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:
②用氨可将氮氧化物转化为无毒气体。如
 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
您最近半年使用:0次
解题方法
8 . I.回答下列问题。
(1)下列变化中属于吸热反应的是___________ 。
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤ 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO
(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)___________ (填“吸收"或“放出”)的能量为___________ kJ。
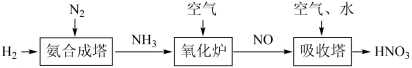
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:___________ (填“氧化剂”或“还原剂”)。
(5)写出氧化炉中反应的化学方程式___________ 。
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤
 固体溶于水;⑥C与CO2反应生成CO
固体溶于水;⑥C与CO2反应生成CO(2)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________。
A.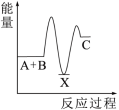 | B.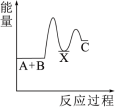 | C.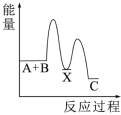 | D.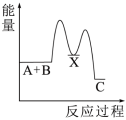 |
(3)过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),断裂1mol H2O2(l)中的O-O键和1mol O2(g)中的O=O键所需的能量依次为142kJ、497.3kJ,断裂H2O2(l)和H2O(l)中1molH-O键所需能量依次为367 kJ、467 kJ,则2 mol H2O2(l)反应生成2 mol H2O(l)和1mol O2(g)
Ⅱ.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
(5)写出氧化炉中反应的化学方程式
(6)用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。在酸性NaClO溶液中,HClO氧化NO生成
 和
和 ,其离子方程式为
,其离子方程式为
您最近半年使用:0次
名校
解题方法
9 . 运用化学反应原理研究化学反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3: ,混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
,混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。 ___________ (填“向左”“向右”或“不”)移动。
②若反应进行到状态D时,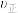
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)课本里介绍的合成氨技术叫哈伯法: ,应用此法反应达到平衡时反应物的转化率不高。
,应用此法反应达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是___________ (填编号)。
A.使用更高效的催化剂 B.升高温度
C.减小体积 D.充入氮气,增大氮气的浓度(保持容器体积不变)
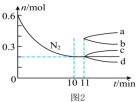
②若在某温度下,2 L的密闭容器中发生合成氨的反应,图2表示N2 的物质的量随时间的变化曲线。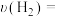
___________ 。从第11min起,扩大容器的体积为4 L,则n(N2) 的变化曲线为___________ (填编号)。
(3)实验室模拟用浓硫酸脱除氮氧化物,装置如图所示,实验开始后装置C中发生反应:NO+NO2+2H2SO4(浓)=2NOHSO4+H2O。___________ ,装置B的作用是___________ 。
②理论上应控制相同时间内a、b处通入气体的物质的量之比为___________ 。
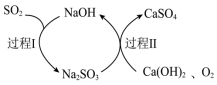
(4)可用双碱法(氢氧化钙为悬浊液)脱硫处理工业废气中的SO2,原理如图所示,双碱法脱硫的总反应方程式为___________ 。
(1)硫酸生产中,SO2催化氧化生成SO3:
 ,混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
,混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。 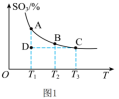
②若反应进行到状态D时,
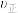
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)课本里介绍的合成氨技术叫哈伯法:
 ,应用此法反应达到平衡时反应物的转化率不高。
,应用此法反应达到平衡时反应物的转化率不高。①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是
A.使用更高效的催化剂 B.升高温度
C.减小体积 D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2 L的密闭容器中发生合成氨的反应,图2表示N2 的物质的量随时间的变化曲线。
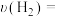
(3)实验室模拟用浓硫酸脱除氮氧化物,装置如图所示,实验开始后装置C中发生反应:NO+NO2+2H2SO4(浓)=2NOHSO4+H2O。
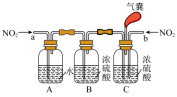
②理论上应控制相同时间内a、b处通入气体的物质的量之比为
(4)可用双碱法(氢氧化钙为悬浊液)脱硫处理工业废气中的SO2,原理如图所示,双碱法脱硫的总反应方程式为
您最近半年使用:0次
名校
10 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的 。
。
(1)水晶和玛瑙的主要成分均为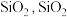 为
为___________ (填“酸性”、“碱性”或“两性”)氧化物,写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:___________ 。
(2)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。
(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;
③ 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。
Ⅰ.第②步制备 反应的化学方程式为:
反应的化学方程式为:___________ ,步骤①②③中属于氧化还原反应的是___________ (填序号)。
Ⅱ.整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:___________ 。
 。
。(1)水晶和玛瑙的主要成分均为
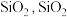 为
为 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:(2)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作(3)工业上制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥
 气体在300℃反应制得
气体在300℃反应制得 和
和 ;
;③
 与过量
与过量 在1000~1100℃反应制得纯硅。
在1000~1100℃反应制得纯硅。Ⅰ.第②步制备
 反应的化学方程式为:
反应的化学方程式为:Ⅱ.整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 和另一种物质,写出该反应的化学方程式:
和另一种物质,写出该反应的化学方程式:
您最近半年使用:0次



