名校
1 . 探究是培养创新精神和实践能力的手段。用如下装置探究氯气的性质,图中三支试管口均放置浸有NaOH溶液的棉花。下列对实验现象的分析错误的是
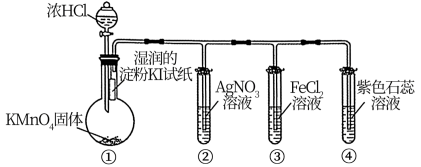

| A.①中淀粉KI试纸变蓝,说明氯气的氧化性强于碘 |
| B.②中产生白色沉淀,说明氯气与水反应生成Cl— |
| C.③中的溶液变为棕黄色,说明氯气有氧化性 |
| D.④溶液先变红后褪色,说明氯水有酸性和漂白性 |
您最近一年使用:0次
2021-03-18更新
|
5172次组卷
|
27卷引用:重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题
重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题重庆市育才中学校2022-2023学年高一上学期期中考试化学试题广东省广州市2021届高三3月第一次模拟考试化学试题广东省广州市2021届高三下学期毕业班综合测试(一)化学试题(已下线)第四章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)第9周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练广东省广州市三校2021-202学年高一上学期期末联考化学试题福建省厦门市同安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)第二节 氯及其化合物 第2课时 氯气的实验室制法及氯离子的检验江西省赣州市赣县第三中学2023届高三上学期月考强化训练(B8)化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题广东省广州市海珠外国语实验中学2022-2023学年高一上学期第二次月考化学试题河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题山东省临沂第一中学文峰校区2022-2023学年高一上学期期末考试化学试题四川省成都市树德中学2022-2023学年高一上学期期末复习化学试题福建省尤溪县第七中学2022-2023学年高一下学期第一次阶段检测化学试题湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题 河南大学附属中学2022-2023学年高一下学期第一次月考化学试题湖南师范大学附属中学2023-2024学年高一上学期期中考试化学试题天津市双菱中学2023-2024学年高一上学期期中考试化学试卷陕西省西安市长安区第一中学2023-2024学年高一上学期期中考试化学试题河北省邯郸市涉县第一中学2023-2024学年高一上学期12月月考 化学试卷四川省成都市成华区某校2023-2024学年高一上学期12月月考化学试题湖南省长沙市雅礼中学2023-2024学年高三上学期一模化学试题黑龙江省哈尔滨市宾县第二中学2023-2024学年高一上学期第三次月考化学试题
13-14高三上·安徽马鞍山·期中
名校
解题方法
2 . 下列实验过程中产生沉淀的物质的量(Y)与加入试剂的物质的量(X)之间的关系正确的是


| A.甲向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡 |
| B.乙向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡 |
| C.丙向NH4Al(SO4)2溶液中逐滴加入NaOH溶液直至过量 |
| D.丁向NaOH、Ba(OH)2、NaAlO2的混合溶液中逐渐通入CO2至过量 |
您最近一年使用:0次
2020-12-25更新
|
4090次组卷
|
51卷引用:重庆市巴蜀中学2019-2020学年高一下学期期中考试化学试题
重庆市巴蜀中学2019-2020学年高一下学期期中考试化学试题(已下线)2014届安徽省马鞍山二中高三上学期期中考试化学试卷(已下线)2015届湖北省四校高三上学期期中联考化学试卷2016届河南省周口中英文学校高三上学期期中测试化学试卷2015-2016学年河北省正定中学高一上第三次月考化学试卷12015-2016学年河北省正定中学高一上第三次月考化学试卷22017届陕西省黄陵中学高新部高三上学期一轮复习第一次测试化学试卷2017届河北省石家庄二中高三上学期9月月考化学试卷2017届河北省定兴第三中学高三上学期第一次月考化学试卷2016-2017学年广西钦州市钦州港区高一12月月考化学卷江西省新余市第一中学2018届高三毕业班第四次模拟考试化学试题广西南宁市第三中学2017-2018学年高一上学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【押题专练】【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高一上学期第二次月考化学试题【校级联考】湖南省岳阳县第一中学、汨罗市一中2018-2019学年高一上学期期末考试化学试题百所名校联考-金属及其化合物(已下线)2019年11月10日《每日一题》必修1—— 每周一测甘肃省兰州市第一中学2020届高三9月月考化学试题安徽省怀宁中学2019-2020学年高一上学期第二次月考化学试题江西省南昌市八一中学、洪都中学等六校2019-2020学年高一上学期期末联考化学试题广东省珠海市珠海一中 2019-2020学年度高一下学期期中考试化学试题(已下线)【南昌新东方】2019-2020 莲塘一中 高一(上)期末 004(已下线)【南昌新东方】2019-2020 八一洪都 高一(上)期末联考 003福建省南平市高级中学2019-2020学年高一下学期期中考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(2)内蒙古呼和浩特市和林格尔县第一中学2019-2020学年高一下学期开学测验卷化学试题(已下线)小题必刷14 铝及其化合物——2021年高考化学一轮复习小题必刷(通用版)吉林省白城市洮南市第一中学2021届高三上学期第一次月考化学试题(已下线)第3章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP429】【化学】江西省会昌中学2020-2021学年高一上学期第二次月考化学试题江西省上高二中2020-2021学年高一上学期第三次月考化学试题(已下线)【浙江新东方】绍兴qw135(已下线)练习12 从铝土矿到铝合金-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)江西省高安中学2020-2021学年高一上学期期末考试化学试题河南省信阳市2021届高三上学期第二次教学质量检测化学试题青海省湟川中学2020-2021学年高一下学期开学考试化学试题四川省眉山市彭山区第一中学2020-2021学年高一4月月考化学试题(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)易错专题24 铝及其化合物的两性特点-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)宁夏银川一中2021-2022学年高一上学期期末考试化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题(已下线)微专题12 数形结合思想突破“铝三角”的图象与计算-备战2023年高考化学一轮复习考点微专题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题河南省部分重点中学环际大联考圆梦计划2022-2023学年高三上学期期中考试化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题四川省达州市宣汉县土黄中学2021-2022学年高一上学期第三次月考化学试题陕西省西安市高新第一中学2021-2022学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元01讲核心宁夏平罗中学2022-2023学年高二下学期期末考试化学试题陕西省西安市铁一中学2023-2024学年高三上学期9月月考化学试题
3 . 类推是一种经常采用的科研和学习方法,下列类推结论合理的是
A.由单质铜和 反应生成 反应生成 ,推出单质铜和硫磺反应生成CuS ,推出单质铜和硫磺反应生成CuS |
| B.由卤素单质熔点从上到下逐渐升高,推出碱金属元素单质熔点从上到下逐渐升高 |
| C.由氮元素的最高价含氧酸的酸性强于磷元素,推出氟元素的最高价含氧酸的酸性强于氯元素 |
| D.由金属Na在常温下与水剧烈反应,推出金属Cs在常温下也能与水剧烈反应 |
您最近一年使用:0次
2022-04-19更新
|
922次组卷
|
3卷引用:重庆市缙云教育联盟2022届高三第三次诊断性检测化学试题
重庆市缙云教育联盟2022届高三第三次诊断性检测化学试题河南省郑州市十校2021-2022学年高一下学期期中联考化学试题(已下线)第五章 物质结构 元素周期律(测)-2023年高考化学一轮复习讲练测(全国通用)
4 . 三种气体 X、Y、Z 的相对分子质量关系为 Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
| A.原子数相等的三种气体,质量最大是 Z |
| B.若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1 mol |
| C.同温同压下,同质量的三种气体,气体密度最小的是X |
| D.同温下,体积相同的两容器分别充agY气体和2agZ气体,则压强之比为1:2 |
您最近一年使用:0次
2022-12-25更新
|
1613次组卷
|
52卷引用:重庆市万州纯阳中学2022-2023学年高三上学期8月月考化学试题
重庆市万州纯阳中学2022-2023学年高三上学期8月月考化学试题2016届湖北省武汉市高三下学期2月调研理综化学试卷2016-2017学年江西省南昌二中高一上月考一化学试卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷2016届辽宁省葫芦岛市第一高级中学高三上学期第二次周考理综化学试卷河北省“名校联盟”(五校联考)2018届高三上学期教学质量监测(一)化学试题湖北省武汉市部分重点中学2017-2018学年高一上学期期中考试化学试题山东省沂水县第一中学2018届高三下学期第2次模拟化学试题【全国百强校】河北省邢台市第一中学2017-2018学年高二下学期第三次月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点02 物质的量【市级联考】山东省泰安市2019届高三上学期期中考试化学试题【校级联考】安徽省滁州市定远县西片区2018-2019学年高一上学期期中考试化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题云南省元江县一中2018-2019学年高一下学期2月份考试化学试题(已下线)2019年7月2日 《每日一题》2020年高考一轮复习-阿伏加德罗定律及其推论的应用河北省秦皇岛一中2019-2020学年高一上学期第一次月考化学试题四川省广安市邻水县邻水实验学校2019-2020学年高一上学期第一次月考化学试题河北省邯郸市2019-2020学年高一上学期期中考试化学试题内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高一10月月考化学试题广西南宁市第三中学2019-2020学年高一上学期期中考试化学试题安徽省合肥十中2019-2020学年高一上学期期中考试化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题1内蒙古包钢第一中学2019-2020学年高一上学期10月月考化学试题广东省江门市第一中学2019-2020学年高一上学期10月月考化学试题山西省忻州市第一中学2019-2020学年高一上学期第二次月考化学试题安徽省合肥市肥东县第二中学2020-2021学年高一上学期期末考试化学试题内蒙古呼和浩特市第十六中学2020-2021学年高一上学期第一次质量检测化学试题专题1 第2课时气体摩尔体积-高中化学苏教2019版必修第一册(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时11 物质的量、气体摩尔体积-2022年高考化学一轮复习小题多维练(全国通用)福建省厦门一中2019-2020学年高一上学期第一次月考(10月)化学试题(已下线)考点02 化学用语和常用化学计量-备战2022年高考化学学霸纠错(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)化学-2022年高考押题预测卷02(山东卷)(已下线)必刷卷04-2022年高考化学考前信息必刷卷(山东专用)(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第04讲 物质的量 气体摩尔体积 (练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省龙西北八校联合体2022-2023学年高三上学期开学考试化学试题河南省南阳市第一中学校2023届高三上学期第二次阶段考试化学试题(已下线)专题五 化学常用计量与化学计算-实战高考·二轮复习核心突破山东莒县第一中学2022-2023学年高一上学期12月月考化学试题山东省烟台第一中学2022-2023学年高一上学期月考化学试题山东省烟台第一中学2022-2023学年高一上学期期末调研化学试题安徽省安庆市桐城中学2022-2023学年高一上学期第二次教学质量检测化学试题第二章 物质的量化学实验基本技能 第6讲 物质的量山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题河北省石家庄二中教育集团2022-2023学年度高一年级上学期期末考试化学试题广西浦北中学2023-2024学年高一上学期10月月考化学试题福建省泉州市安溪一中、养正中学、惠安一中、实验中学2023-2024学年高一上学期期中考化学试题
名校
5 . 化合物甲是一种常见无机物,其结构如下图所示(图中的“—”为单键或双键),其中W、X、Y、Z为元素周期表中的短周期主族元素,且原子序数依次增大,W和Y、X和Z分别为同主族元素,其四种元素原子的最外层电子数之和为14.下列叙述正确的是( )
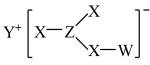
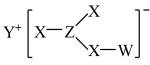
| A.W分别与X、Z形成的简单分子均为10电子微粒 |
| B.X、Y形成的离子化合物只含离子键 |
| C.X、Y、Z三种元素的简单离子半径大小顺序为Z>X>Y |
| D.等物质的量Y和Z的最高价氧化物对应的水化物反应生成甲 |
您最近一年使用:0次
2020-09-14更新
|
2896次组卷
|
12卷引用:重庆市第七中学2021届高三上学期期中化学试题
重庆市第七中学2021届高三上学期期中化学试题天一大联考“顶尖计划”2021届高三第一次考试化学试题黑龙江省大庆实验中学2021届高三上学期第一次月考化学试题黑龙江省哈尔滨师范大学附属中学2021届高三10月月考化学试题(已下线)【南昌新东方】6 2020年10月江西南昌-江科附中-高三-上学期-月考化学卷四川省绵阳市涪城区绵阳南山中学2021届高三上学期11月月考理综化学试题(已下线)小题必刷22 元素周期表(律)及其应用——2021年高考化学一轮复习小题必刷(通用版)(已下线)练习13 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)湖南省长沙市长郡中学2021-2022学年高三下学期月考考试(第六次)化学试题河南省商丘市第一高级中学2021-2022学年高一下学期开学测试化学试题山东省临沂第一中学文峰校区2022-2023学年高一上学期期末考试化学试题江苏省沛县中学2022-2023学年高三上学期12月月考化学试题
名校
解题方法
6 . 大多数离子液体含有体积很大的阴、阳离子(如图所示)。其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。下列说法正确的是
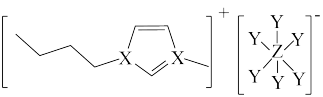

| A.原子半径:Z>X>Y | B.气态氢化物的稳定性:Z>X>Y |
| C.Z的氯化物的分子式一定为ZCl3 | D.此阴离子中Y、Z均满足8电子稳定结构 |
您最近一年使用:0次
2022-07-10更新
|
1346次组卷
|
7卷引用:重庆市第一中学2022-2023学年高二上学期期末考试化学试题
7 . 从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
| A.Cu2S既是氧化产物又是还原产物 |
| B.5mol FeS2发生反应,有10mol电子转移 |
C.产物中的SO 离子有一部分是氧化产物 离子有一部分是氧化产物 |
| D.FeS2只作还原剂 |
您最近一年使用:0次
2021-01-12更新
|
1912次组卷
|
41卷引用:2016届重庆市巫山中学高三第一次质量检测化学试卷
2016届重庆市巫山中学高三第一次质量检测化学试卷(已下线)2010年云南省玉溪一中高二下学期期末考试化学试题(已下线)2010年安徽省合肥八中高三上学期第二次月考化学试题(已下线)2012届浙江省杭州市高复高三上学期11月份月考化学试卷(已下线)2013-2014学年辽宁省抚顺市六校联合体高二下学期期末考试化学试卷2016届辽宁省葫芦岛市高三上学期期末调研化学试卷2015-2016学年吉林松原油田高中高一下期初考试化学试卷2015-2016学年湖南省长沙长郡中学高一上期末化学试卷2016-2017学年安徽省合肥一中高一上开学测化学试卷2017届陕西省西安市第七十中学高三上学期10月月考化学试卷2017届河北辛集中学高三上理综测试三化学试卷2017届河北省定州中学高三上期中化学试卷12016-2017学年安徽省铜陵一中高一12月月考化学试卷广东省化州市2018届高三上学期第一次高考模拟考试理综化学试题辽宁省大连育明高级中学、本溪市高级中学2018届高三10月月考化学(理)试题江苏省无锡市普通高中2017-2018学年高一上学期期末考试化学试题陕西省西安市第一中学2017-2018学年高一上学期期末考试化学试题云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题福建省华安一中、长泰一中等四校2017-2018学年高一下学期第一次(4月)联考化学试题(已下线)2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 讲【全国百强校】陕西省西安市第一中学2019届高三上学期第一次月考化学试题【全国百强校】西藏自治区拉萨北京实验中学2019届高三上学期第二次月考化学试题【全国百强校】河北省武邑中学2019届高三上学期第四次调研考试化学试题【全国百强校】山东省临沂市蒙阴县实验中学2019届高三上学期第二次月考(12月)化学试题吉林省白城市第一中学2018-2019学年高一上学期12月月考化学试题福建省福州市八县一中2020届高三年上学期期中联考化学试题广东省深圳市实验中学2019-2020学年高一上学期期中考试化学试题安徽省滁州市定远县育才学校2019-2020学年高一(普通班)上学期第三次月考化学试题甘肃省武威第十八中学2021届高三上学期第四次诊断检测(期末)化学试题专题3 第一单元 第3课时 氧化还原反应-高中化学苏教2019版必修第一册(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)江西省丰城市第九中学2021-2022学年高三上学期9月月考化学试题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)押新高考卷10题 氧化还原反应-备战2022年高考化学临考题号押题(新高考通版)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)福建省福州市格致中学2022-2023学年高三上学期期中模拟测试化学试题山西省山西大学附属中学2022-2023学年高一上学期期中考试化学试题 新疆乌鲁木齐八一中学2023-2024学年高一上学期期中考试化学试卷
名校
解题方法
8 . 固体粉末可能由 中的几种等物质的量混合而成,进行如下实验:
中的几种等物质的量混合而成,进行如下实验:
①取 固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
②在第一份溶液中滴加足量稀盐酸无明显现象,再滴加足量 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。
固体。
③在第二份溶液中滴加 溶液无明显现象,继续滴加双氧水,溶液显血红色。
溶液无明显现象,继续滴加双氧水,溶液显血红色。
④在第三份溶液中滴加足量 溶液,过滤、洗涤、灼烧,得到固体
溶液,过滤、洗涤、灼烧,得到固体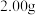 。
。
下列说法正确的是
 中的几种等物质的量混合而成,进行如下实验:
中的几种等物质的量混合而成,进行如下实验:①取
 固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。
固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份。②在第一份溶液中滴加足量稀盐酸无明显现象,再滴加足量
 溶液,过滤、洗涤、干燥,得到
溶液,过滤、洗涤、干燥,得到 固体。
固体。③在第二份溶液中滴加
 溶液无明显现象,继续滴加双氧水,溶液显血红色。
溶液无明显现象,继续滴加双氧水,溶液显血红色。④在第三份溶液中滴加足量
 溶液,过滤、洗涤、灼烧,得到固体
溶液,过滤、洗涤、灼烧,得到固体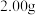 。
。下列说法正确的是
A.固体粉末中肯定没有 |
B.根据④中的沉淀颜色能判断固体粉末中是否含有 |
C.固体粉末中肯定含有 |
D.上述实验无法确定固体粉末是否含有 ,需进一步通过焰色试验确定 ,需进一步通过焰色试验确定 |
您最近一年使用:0次
2022-01-22更新
|
1114次组卷
|
5卷引用: 重庆市第一中学校2022-2023学年高一上学期期末考试化学试题
名校
9 .  (易潮解)是一种潜在的锂电池的电解质材料。某小组用粗锌(含少量
(易潮解)是一种潜在的锂电池的电解质材料。某小组用粗锌(含少量 和
和 )和稀硫酸反应制备
)和稀硫酸反应制备 ,利用纯化后的氢气还原硫酸锂制备硫化锂并对产品纯度进行分析。
,利用纯化后的氢气还原硫酸锂制备硫化锂并对产品纯度进行分析。
请回答下列问题:
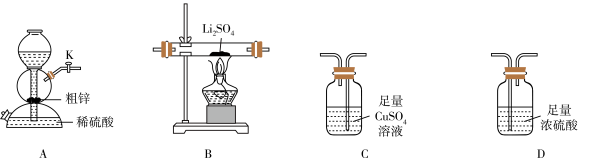
(1)利用上述装置制备 ,按气流从左至右,装置的连接顺序是A→
,按气流从左至右,装置的连接顺序是A→_______ (填字母,装置可重复使用)。
(2)其他条件相同,粗锌与稀硫酸反应比纯锌_______ (填“快”或“慢”),B中反应的化学方程式为_______ ,C中现象是_______ 。
(3)探究 产品的成分
产品的成分
由上述实验Ⅱ中滴加试剂为_______ ,产品中含有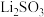 、
、 杂质的原因可能是
杂质的原因可能是_______ 。
(4)定量测定 的含量
的含量
①取 g
g 样品加入
样品加入


 稀硫酸(过量)
稀硫酸(过量)
②充分反应后,煮沸溶液以除去残留的酸性气体
③滴加酚酞溶液作指示剂,用
 标准
标准 溶液滴定过量的硫酸,消耗
溶液滴定过量的硫酸,消耗 溶液
溶液
 ,产品含
,产品含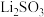 杂质,但不影响上述实验方案的科学性,理由是
杂质,但不影响上述实验方案的科学性,理由是_______ ,若产品中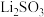 杂质含量为10%(质量分数),则
杂质含量为10%(质量分数),则 样品的纯度为
样品的纯度为_______ (用含 、
、 、
、 、
、 、m的代数式表示)。
、m的代数式表示)。
 (易潮解)是一种潜在的锂电池的电解质材料。某小组用粗锌(含少量
(易潮解)是一种潜在的锂电池的电解质材料。某小组用粗锌(含少量 和
和 )和稀硫酸反应制备
)和稀硫酸反应制备 ,利用纯化后的氢气还原硫酸锂制备硫化锂并对产品纯度进行分析。
,利用纯化后的氢气还原硫酸锂制备硫化锂并对产品纯度进行分析。请回答下列问题:

(1)利用上述装置制备
 ,按气流从左至右,装置的连接顺序是A→
,按气流从左至右,装置的连接顺序是A→(2)其他条件相同,粗锌与稀硫酸反应比纯锌
(3)探究
 产品的成分
产品的成分| 实验 | 操作与现象 | 结论 |
| Ⅰ | 取少量 样品,滴加足量稀盐酸,将气体通入品红溶液中,溶液褪色 样品,滴加足量稀盐酸,将气体通入品红溶液中,溶液褪色 | 样品含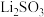 杂质 杂质 |
| Ⅱ | 在实验Ⅰ的溶液中滴加_______,产生白色沉淀 | 样品含 杂质 杂质 |
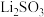 、
、 杂质的原因可能是
杂质的原因可能是(4)定量测定
 的含量
的含量①取
 g
g 样品加入
样品加入


 稀硫酸(过量)
稀硫酸(过量)②充分反应后,煮沸溶液以除去残留的酸性气体
③滴加酚酞溶液作指示剂,用

 标准
标准 溶液滴定过量的硫酸,消耗
溶液滴定过量的硫酸,消耗 溶液
溶液
 ,产品含
,产品含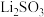 杂质,但不影响上述实验方案的科学性,理由是
杂质,但不影响上述实验方案的科学性,理由是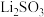 杂质含量为10%(质量分数),则
杂质含量为10%(质量分数),则 样品的纯度为
样品的纯度为 、
、 、
、 、
、 、m的代数式表示)。
、m的代数式表示)。
您最近一年使用:0次
10-11高二上·甘肃武威·阶段练习
名校
解题方法
10 . 在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量之比为3:2:1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变为1:2:4,则参加反应的铁粉和原溶液中Fe3+的物质的量之比为
| A.2:1 | B.1:2 | C.1:3 | D.1:4 |
您最近一年使用:0次
2021-09-09更新
|
1685次组卷
|
28卷引用:重庆市三峡名校联盟2020-2021学年高一上学期12月联考化学试题
重庆市三峡名校联盟2020-2021学年高一上学期12月联考化学试题(已下线)2010年甘肃省武威五中高二11月月考化学试卷2015届河北省邯郸市高三上学期1月教学质量检测化学试卷2014-2015江西省新余市高一上学期期末考试化学试卷2014-2015学年辽宁师大附中高二下学期期末考试化学试卷2015-2016学年陕西省长安区一中高一上期末化学试卷(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【押题专练】【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期12月月考化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题河北省大名县第一中学2020届高三9月月考化学试题河北省武安市第一中学2020届高三9月月考化学试题甘肃省兰州市第一中学2020届高三9月月考化学试题宁夏石嘴山市第三中学2019-2020学年高一上学期第二次(12月)月考化学试题安徽省安庆一中2018-2019学年高一上学期期末考试化学试题安徽省太和第一中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷2专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)3.1.2 铁的氢氧化物 铁盐和亚铁盐练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)第03章 铁 金属材料(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)人教版(2019)高一必修第一册第三章 铁 金属材料 素养拓展区人教版(2019)高一必修第一册 第三章素养检测江西省鹰潭市第一中学2021届高三上学期期中考试化学试题四川省仁寿第一中学校南校区2020-2021学年高一下学期开学考试化学试题(已下线)8.1 铁及其化合物-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)黑龙江省七台河市勃利县高级中学2021-2022学年高三上学期期中考试化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题陕西省延安子长市中学2021-2022学年高三上学期期中考试化学试题



