1 . 氟化钾是一种重要的无机化合物,应用广泛。其一种制备工艺流程如下:

回答下列问题:
(1)“滤渣”中的主要成分是_______ (填化学式),写出该成分的一种用途:_______ 。
(2)写出制备 的反应的化学方程式:
的反应的化学方程式:_______ ;配制 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸_______  。
。
(3)制备 的反应其基本反应类型为
的反应其基本反应类型为_______ 。
(4)写出“转化”时发生反应的化学方程式:_______ 。
(5)“系列操作”包括_______ 、过滤分离和干燥。

回答下列问题:
(1)“滤渣”中的主要成分是
(2)写出制备
 的反应的化学方程式:
的反应的化学方程式: 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸 。
。(3)制备
 的反应其基本反应类型为
的反应其基本反应类型为(4)写出“转化”时发生反应的化学方程式:
(5)“系列操作”包括
您最近一年使用:0次
2 . 病人输液用的葡萄糖注射液是葡萄糖(化学式 )的水溶液,其标签上的部分内容如图所示,则该注射液中葡萄糖的物质的量浓度约为
)的水溶液,其标签上的部分内容如图所示,则该注射液中葡萄糖的物质的量浓度约为

 )的水溶液,其标签上的部分内容如图所示,则该注射液中葡萄糖的物质的量浓度约为
)的水溶液,其标签上的部分内容如图所示,则该注射液中葡萄糖的物质的量浓度约为
A.0.18 | B.0.28 | C.0.014  | D.0.32 |
您最近一年使用:0次
22-23高一上·全国·课时练习
3 . “84消毒液”能有效杀灭甲型 病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
(1)该“84消毒液”的物质的量浓度约为_________________ 。
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=_________________ mol·L-1。
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8 g·cm-3)的浓硫酸配制100 mL物质的量浓度为0.8 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需要用量筒量取_________________ mL上述浓硫酸进行配制。
②稀释后的稀硫酸溶液中c(H+)为_________________ 。
 病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:
病毒,某同学购买了一瓶“威露士”牌“84消毒液”,该消毒液通常稀释100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如下信息:| 84消毒液 有效成分NaClO 规格1 000 mL 质量分数25% 密度1.19 g·cm-3 |
(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.8 g·cm-3)的浓硫酸配制100 mL物质的量浓度为0.8 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需要用量筒量取
②稀释后的稀硫酸溶液中c(H+)为
您最近一年使用:0次
解题方法
4 . 如图所示装置的实验中,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 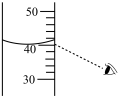 | 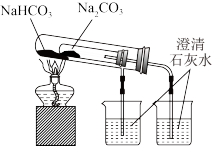 | 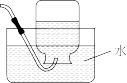 | 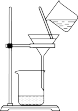 |
| 实验目的 | 配制氯化钠溶液时量取水的体积 | 比较 、 、 的稳定性 的稳定性 | 排水法收集NO | 分离氯化铁溶液和氢氧化铁胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 配制500mL0.1mol·L-1硫酸铜溶液,需胆矾
| A.8.00 g | B.16.0 g | C.25.0 g | D.12.5 g |
您最近一年使用:0次
解题方法
6 . 下列有关0.1mol·L-1NaOH溶液的叙述正确的是
| A.1L该溶液中含有NaOH40g |
| B.在1L水中溶解4gNaOH即可配制得0.1mol·L-1NaOH溶液 |
| C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01mol·L-1 |
| D.100ml该溶液中含有OH-0.01mol |
您最近一年使用:0次
7 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
解题方法
8 . 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是
| 硫酸 化学纯(CP)(500mL) 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
| A.该硫酸的物质的量浓度为9.2mol/L |
| B.用量筒量取10mL该样品,其中所含硫酸质量为18.4g |
| C.配制500mL4.6mol/L的稀硫酸需取该硫酸125mL |
| D.硫酸的摩尔质量为98 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
| A.Na2O2能与水反应生成碱,所以它是碱性氧化物 |
| B.足量MnO2与200 mL 12 mol/L的浓盐酸充分共热,生成氯气42.6g |
C.实验需要用到 溶液,配制该溶液时应称取2.5g胆矾晶体 溶液,配制该溶液时应称取2.5g胆矾晶体 |
| D.向饱和石灰水中加入一定量CaO固体,恢复原温度,溶液中Ca2+数目不变 |
您最近一年使用:0次
2022-11-30更新
|
189次组卷
|
2卷引用:湖南省湖南师范大学附属中学2021-2022学年高一上学期第一次大练习化学试题
名校
10 . 填空计算,不用写计算过程。
(1)一定量的液态化合物XY2在一定量的氧气(标准状况)中恰好完全燃烧,反应的化学方程式为XY2(l)+3O2(g)=XO2(g)+2YO2(g)。冷却后,在标准状况下测得生成物的体积为672mL,密度为2.56g·L-1,则:反应前O2的体积是_______ mL。化合物XY2的摩尔质量是_______ g/mol。
(2)用98%(密度为1.84g/cm3)的浓硫酸配制1mol/L的稀硫酸200mL需浓硫酸_______ mL。(保留小数点后一位)
(3)用1mol·L-1的Na2SO3溶液60mL恰好将一定物质的量的XO ,还原,已知氧化产物为
,还原,已知氧化产物为 ,而元素X在还原产物中的化合价为+4,则反应的XO
,而元素X在还原产物中的化合价为+4,则反应的XO 的物质的量是
的物质的量是_______ mol。
(1)一定量的液态化合物XY2在一定量的氧气(标准状况)中恰好完全燃烧,反应的化学方程式为XY2(l)+3O2(g)=XO2(g)+2YO2(g)。冷却后,在标准状况下测得生成物的体积为672mL,密度为2.56g·L-1,则:反应前O2的体积是
(2)用98%(密度为1.84g/cm3)的浓硫酸配制1mol/L的稀硫酸200mL需浓硫酸
(3)用1mol·L-1的Na2SO3溶液60mL恰好将一定物质的量的XO
 ,还原,已知氧化产物为
,还原,已知氧化产物为 ,而元素X在还原产物中的化合价为+4,则反应的XO
,而元素X在还原产物中的化合价为+4,则反应的XO 的物质的量是
的物质的量是
您最近一年使用:0次



