名校
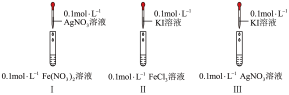
1 . 通过如下实验,比较 、
、 、
、 的氧化性。
的氧化性。
(1)实验室 溶液通常盛放在
溶液通常盛放在___________ 试剂瓶中。
(2)Ⅱ中反应的离子方程式为___________ 。
(3)I、Ⅱ中的现象说明___________。
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
(5)写出检验I中是否含有 的方法。
的方法。___________ 。
(6)检验Ⅱ中是否含有 不可选用:___________。(不定项)
不可选用:___________。(不定项)
(7)推测Ⅲ中未发生 氧化
氧化 的原因
的原因___________ 。
 、
、 、
、 的氧化性。
的氧化性。
| 实验现象 |
I中产生黑色沉淀,滴加 溶液,变红 溶液,变红 | |
| Ⅱ中溶液呈棕黄色,滴加淀粉溶液,变蓝 | |
| Ⅲ中产生黄色沉淀,滴加淀粉溶液,未变蓝 |
(1)实验室
 溶液通常盛放在
溶液通常盛放在(2)Ⅱ中反应的离子方程式为
(3)I、Ⅱ中的现象说明___________。
A.氧化性顺序: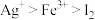 | B.氧化性顺序: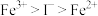 |
C.还原性顺序: | D.还原性顺序: |
(4)实验后,I试管壁上的黑色沉淀可用___________洗去。
| A.酒精 | B.二硫化碳 | C.浓硝酸 | D.热盐酸 |
(5)写出检验I中是否含有
 的方法。
的方法。(6)检验Ⅱ中是否含有
 不可选用:___________。(不定项)
不可选用:___________。(不定项)| A.氢氧化钠溶液 | B.酸性高辒酸钾溶液 | C.硫氰化钾溶液 | D.稀氨水 |
(7)推测Ⅲ中未发生
 氧化
氧化 的原因
的原因
您最近一年使用:0次
2 . 电子工业常用 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有___________ 。
(2) 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为___________ 。
(3)试剂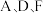 的化学式分别是
的化学式分别是___________ 、___________ 、___________ 。用 溶液制取
溶液制取 晶体的方法是
晶体的方法是___________ 。
A.蒸发结晶 B.降温结晶
 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: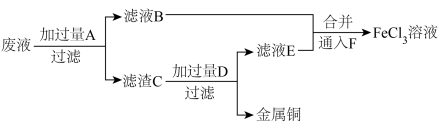
 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有(2)
 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为(3)试剂
 的化学式分别是
的化学式分别是 溶液制取
溶液制取 晶体的方法是
晶体的方法是A.蒸发结晶 B.降温结晶
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式书写正确的是
A.铁与稀盐酸反应: |
B.氯气与氯化亚铁溶液反应: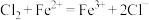 |
C.过量二氧化硫溶于氢氧化钠溶液: |
D.氯化铁溶液与硫化氢反应: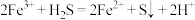 |
您最近一年使用:0次
4 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.在新制饱和氯水中: 、 、 、 、 、 、 |
B.使酚酞变红色的溶液: 、 、 、 、 、 、 |
C.使紫色石蕊试液变红色的溶液: 、 、 、 、 、 、 |
D.在 小于7的溶液: 小于7的溶液: 、 、 |
您最近一年使用:0次
名校
解题方法
5 . 利用赤铁矿(主要成分为 )、磁铁矿(主要成分为
)、磁铁矿(主要成分为 )、菱铁矿(主要成分为
)、菱铁矿(主要成分为 )都可以制备铁红。如图是
)都可以制备铁红。如图是 可以制备铁红的流程。
可以制备铁红的流程。
(2)检验滤液A中含有 的试剂是
的试剂是_____ 。(写名称)
(3)在空气中煅烧 的方程式为
的方程式为_____ 。
(4)铁红中的铁元素质量往往大于原磁铁矿中铁元素质量的原因是_____ 。
 )、磁铁矿(主要成分为
)、磁铁矿(主要成分为 )、菱铁矿(主要成分为
)、菱铁矿(主要成分为 )都可以制备铁红。如图是
)都可以制备铁红。如图是 可以制备铁红的流程。
可以制备铁红的流程。
| A.Fe | B.FeO | C. | D. |
(2)检验滤液A中含有
 的试剂是
的试剂是(3)在空气中煅烧
 的方程式为
的方程式为(4)铁红中的铁元素质量往往大于原磁铁矿中铁元素质量的原因是
您最近一年使用:0次
名校
6 . 某班同学用如下实验探究 、
、 的性质。回答下列问题:
的性质。回答下列问题:
(1)甲组同学通过研究 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为___________ 。

乙组同学为探究 与的反应,进行如图所示实验:
与的反应,进行如图所示实验:

(2) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与 相似;
相似;
iii.
实验方案如下:
(3) 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
(4) 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将 转化为
转化为 ”的结论?
”的结论?___________ (填“能”或“否”)请说明理由___________ 。
 、
、 的性质。回答下列问题:
的性质。回答下列问题:(1)甲组同学通过研究
 对
对 稳定性的影响,得到如图所示结果,增强
稳定性的影响,得到如图所示结果,增强 稳定性的措施为
稳定性的措施为
乙组同学为探究
 与的反应,进行如图所示实验:
与的反应,进行如图所示实验:
(2)
 与
与 反应的离子方程式为
反应的离子方程式为为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.的化学性质与
 相似;
相似;iii.

实验方案如下:
| 实验方案 | 实验现象 |
步骤1:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴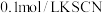 溶液 溶液 | 无明显现象 |
步骤2:取 溶液,向其中滴加3滴 溶液,向其中滴加3滴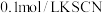 溶液 溶液 | 产生白色沉淀 |
 与
与 反应的离子方程式为
反应的离子方程式为(4)
 可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服。同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
 转化为
转化为 ”的结论?
”的结论?
您最近一年使用:0次
解题方法
7 . 打印机墨粉中Fe3O4的含量是衡量墨粉质量优劣的重要指标之一,为测定某墨粉Fe3O4的含量,同学们在化学实验室中进行了如下实验。

已知:①墨粉中除Fe3O4外,其余成分既不含铁元素,也不溶于水、不与酸反应
②酸性高锰酸钾溶液呈紫红色,Mn2+溶液无色
(1)列举两个生成磁性氧化铁反应的化学方程式:___________ 、___________ 。
(2)检验Fe2+:
i.[实验原理]____Fe2++___ +____H+=____Fe3++____Mn2++____H2O
+____H+=____Fe3++____Mn2++____H2O____________ ,配平离子方程式。
ii.[实验操作]取第一份溶液少许,向其中滴加酸性KMnO4溶液,振荡,观察到溶液紫色_______ 
iii.【实验结论】溶液中含Fe2+,同时证明Fe2+具有___________ 性。
(3)测定Fe3O4的含量:

i.加入足量氯水的目的是___________ ,有关反应的离子方程式是___________ 。
ii.加入足量NaOH溶液后观察到的现象是___________ 。
iii.沉淀加热时发生反应的化学方程式是___________ 。

已知:①墨粉中除Fe3O4外,其余成分既不含铁元素,也不溶于水、不与酸反应
②酸性高锰酸钾溶液呈紫红色,Mn2+溶液无色
(1)列举两个生成磁性氧化铁反应的化学方程式:
(2)检验Fe2+:
i.[实验原理]____Fe2++___
 +____H+=____Fe3++____Mn2++____H2O
+____H+=____Fe3++____Mn2++____H2Oii.[实验操作]取第一份溶液少许,向其中滴加酸性KMnO4溶液,振荡,观察到溶液紫色

iii.【实验结论】溶液中含Fe2+,同时证明Fe2+具有
(3)测定Fe3O4的含量:

i.加入足量氯水的目的是
ii.加入足量NaOH溶液后观察到的现象是
iii.沉淀加热时发生反应的化学方程式是
您最近一年使用:0次
名校
8 . 下列试剂不能将溶液中 转化为
转化为 的是
的是
 转化为
转化为 的是
的是| A.液溴 | B.氨水 | C.氯水 | D.浓硝酸 |
您最近一年使用:0次
名校
9 . 磁铁矿的主要成分是 。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。
。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。
(1)步骤一:取少量磁铁矿石,粉碎后加入过量的试剂A可选用_____。
(2)步骤二:验证: 。取溶解后的无色液体少许,加入少量
。取溶解后的无色液体少许,加入少量___________ ,若观察到溶液变为血红色,则证明有 。
。
(3)步骤三:验证: 。取溶解后的无色液体少许,加入少量
。取溶解后的无色液体少许,加入少量___________ ,若观察到___________ ,则证明有 。
。
 。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。
。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。(1)步骤一:取少量磁铁矿石,粉碎后加入过量的试剂A可选用_____。
| A.氨水 | B.氢氧化钠溶液 | C.盐酸 | D.硫酸 |
 。取溶解后的无色液体少许,加入少量
。取溶解后的无色液体少许,加入少量 。
。(3)步骤三:验证:
 。取溶解后的无色液体少许,加入少量
。取溶解后的无色液体少许,加入少量 。
。
您最近一年使用:0次
名校
10 . 铁的化合物有广泛用途,如碳酸亚铁( )可作补血剂,铁红(
)可作补血剂,铁红( )可作为颜料。利用某硫酸厂产生的烧渣(主要含
)可作为颜料。利用某硫酸厂产生的烧渣(主要含 、
、 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:

(1)“酸溶”时加入的硫酸不宜过是太多,其原因是:______ 。
(2)检验第1次过滤后的滤液中是否含有 需要的试剂是
需要的试剂是______ 。过滤操作需要用到的玻璃仪器有:烧杯、______ 和______ 。
(3)“还原”时,加入的 与
与 发生2种氧化还原反应:
发生2种氧化还原反应:
①
②______ 。(用离子方程式表示)
(4)“沉淀”时需控制pH值不宜过高,否则生成的 中可能混有
中可能混有______ 。杂质(写出一种即可)。写出“沉淀”时发生反应的离子方程式______ 。
(5) 浊液若未及时过滤,长时间暴露在空气中会有部分固体表面变为红褐色,同时释放
浊液若未及时过滤,长时间暴露在空气中会有部分固体表面变为红褐色,同时释放 ,则与
,则与 反应的物质是
反应的物质是______ (磌化学式)。
(6) 在空气中煅烧时生成
在空气中煅烧时生成 和
和 的混合物。充分煅烧
的混合物。充分煅烧 ,得到固体混合物
,得到固体混合物 ,则混合物中
,则混合物中 的质量为
的质量为______ 。
 )可作补血剂,铁红(
)可作补血剂,铁红( )可作为颜料。利用某硫酸厂产生的烧渣(主要含
)可作为颜料。利用某硫酸厂产生的烧渣(主要含 、
、 ,还有一定量的
,还有一定量的 )制备碳酸亚铁的流程如图所示:
)制备碳酸亚铁的流程如图所示:
(1)“酸溶”时加入的硫酸不宜过是太多,其原因是:
(2)检验第1次过滤后的滤液中是否含有
 需要的试剂是
需要的试剂是(3)“还原”时,加入的
 与
与 发生2种氧化还原反应:
发生2种氧化还原反应:①

②
(4)“沉淀”时需控制pH值不宜过高,否则生成的
 中可能混有
中可能混有(5)
 浊液若未及时过滤,长时间暴露在空气中会有部分固体表面变为红褐色,同时释放
浊液若未及时过滤,长时间暴露在空气中会有部分固体表面变为红褐色,同时释放 ,则与
,则与 反应的物质是
反应的物质是(6)
 在空气中煅烧时生成
在空气中煅烧时生成 和
和 的混合物。充分煅烧
的混合物。充分煅烧 ,得到固体混合物
,得到固体混合物 ,则混合物中
,则混合物中 的质量为
的质量为
您最近一年使用:0次