名校
解题方法
1 . 一种利用磁铁矿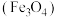 制备铁红的流程如下:
制备铁红的流程如下:
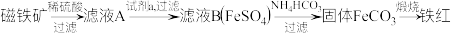
下列说法正确的是
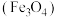 制备铁红的流程如下:
制备铁红的流程如下: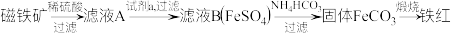
下列说法正确的是
| A.往滤液A中滴加少量酸性KMnO4溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C.FeCO3在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
解题方法
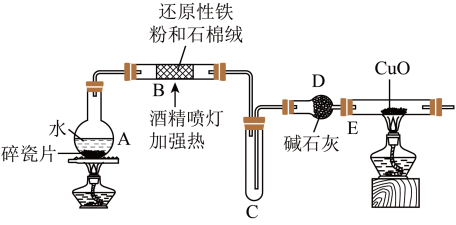
2 .  是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备
是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备 。回答下列问题:
。回答下列问题:
Ⅰ.制备
 的名称是
的名称是___________ ;装置 作用是
作用是___________ 。
(2)装置 中反应的化学方程式为
中反应的化学方程式为___________ 。
(3)实验过程中可观察到 中的现象是黑色固体变红,说明产生的气体是
中的现象是黑色固体变红,说明产生的气体是___________ 。
Ⅱ.探究 中铁粉是否完全反应
中铁粉是否完全反应
待硬质玻璃管 冷却后,取少许其中的固体物质进行如下实验(已知酸性
冷却后,取少许其中的固体物质进行如下实验(已知酸性 溶液能与盐酸发生反应):
溶液能与盐酸发生反应): 可以是
可以是___________ (填标号)。
A.盐酸 B.硫酸 C.次氯酸
(5)①现象1为___________ 。
②有同学认为现象2中溶液未变红色,说明 固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:
固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:___________ 。
(6)已知温度高于 时,铁与水蒸气反应的氧化产物只有
时,铁与水蒸气反应的氧化产物只有 ,甲同学称取
,甲同学称取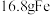 粉于装置
粉于装置 中,在
中,在 反应一段时间后停止加热,冷却后称得固体质量为
反应一段时间后停止加热,冷却后称得固体质量为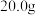 ,则未反应的
,则未反应的 粉的物质的量为
粉的物质的量为___________  。
。
 是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备
是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备 。回答下列问题:
。回答下列问题:Ⅰ.制备

 的名称是
的名称是 作用是
作用是(2)装置
 中反应的化学方程式为
中反应的化学方程式为(3)实验过程中可观察到
 中的现象是黑色固体变红,说明产生的气体是
中的现象是黑色固体变红,说明产生的气体是Ⅱ.探究
 中铁粉是否完全反应
中铁粉是否完全反应待硬质玻璃管
 冷却后,取少许其中的固体物质进行如下实验(已知酸性
冷却后,取少许其中的固体物质进行如下实验(已知酸性 溶液能与盐酸发生反应):
溶液能与盐酸发生反应):
 可以是
可以是A.盐酸 B.硫酸 C.次氯酸
(5)①现象1为
②有同学认为现象2中溶液未变红色,说明
 固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:
固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:(6)已知温度高于
 时,铁与水蒸气反应的氧化产物只有
时,铁与水蒸气反应的氧化产物只有 ,甲同学称取
,甲同学称取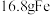 粉于装置
粉于装置 中,在
中,在 反应一段时间后停止加热,冷却后称得固体质量为
反应一段时间后停止加热,冷却后称得固体质量为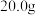 ,则未反应的
,则未反应的 粉的物质的量为
粉的物质的量为 。
。
您最近一年使用:0次
解题方法
3 . 根据下列实验操作和现象,所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 检验铁锈中是否含有二价铁,将铁锈溶于浓盐酸,滴入 溶液,紫色褪去 溶液,紫色褪去 | 铁锈中含有二价铁 |
| B | 用醋酸浸泡水壶中的水垢,可将其清除 | 醋酸的酸性强于碳酸的酸性 |
| C | 将水蒸气通过灼热的铁粉,粉末变黑色 | 铁与水在高温下发生反应 |
| D | 取久置的氯水于试管中,加入几滴紫色石蕊溶液,溶液变为红色,且较长时间内不褪色 | 氯水已经完全变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
524次组卷
|
5卷引用:湖南省娄底市涟源市2023-2024学年高一下学期3月月考化学试题
5 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题: 与浓盐酸反应制取氯气,写出反应的化学方程式并用双线桥法来表示出电子转移的方向和数目
与浓盐酸反应制取氯气,写出反应的化学方程式并用双线桥法来表示出电子转移的方向和数目___________ ,当生成 氯气,做还原剂的
氯气,做还原剂的 的物质的量为
的物质的量为___________ mol。
(2)仪器D的名称是___________ ,D中装的药品可以是___________ (填序号)。
A. B.碱石灰 C.
B.碱石灰 C. D.
D.
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有 ,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取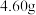 产品溶于过量的稀盐酸中;②加入足量
产品溶于过量的稀盐酸中;②加入足量 溶液;③再加入足量
溶液;③再加入足量 溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为
溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为 。写出加入足量
。写出加入足量 溶液中发生反应的离子方程式
溶液中发生反应的离子方程式___________ 计算该样品中铁元素的质量分数为___________ %(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施。
①对比氯化铁中铁元素的质量分数为34.46%,说明含有 杂质。
杂质。
②若要得到较纯净的无水氯化铁,实验装置可进行的改进措施是___________ 。
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
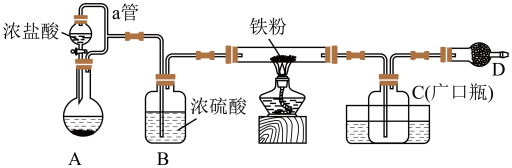
 与浓盐酸反应制取氯气,写出反应的化学方程式并用双线桥法来表示出电子转移的方向和数目
与浓盐酸反应制取氯气,写出反应的化学方程式并用双线桥法来表示出电子转移的方向和数目 氯气,做还原剂的
氯气,做还原剂的 的物质的量为
的物质的量为(2)仪器D的名称是
A.
 B.碱石灰 C.
B.碱石灰 C. D.
D.
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有
 ,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)
,可用下列试剂中的___________进行检测。(填序号,试剂不组合使用)| A.KSCN溶液 | B.酸性 溶液 溶液 |
C. 溶液 溶液 | D.KI-淀粉溶液 |
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取
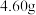 产品溶于过量的稀盐酸中;②加入足量
产品溶于过量的稀盐酸中;②加入足量 溶液;③再加入足量
溶液;③再加入足量 溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为
溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为 。写出加入足量
。写出加入足量 溶液中发生反应的离子方程式
溶液中发生反应的离子方程式(5)由(4)定量分析数据得出结论,并提出改进措施。
①对比氯化铁中铁元素的质量分数为34.46%,说明含有
 杂质。
杂质。②若要得到较纯净的无水氯化铁,实验装置可进行的改进措施是
您最近一年使用:0次
名校
6 . 下列物质的应用中,利用了氧化还原反应原理的是
A. 补血剂与维生素C配合使用效果 补血剂与维生素C配合使用效果 |
| B.二氧化碳灭火 |
| C.小苏打中和胃酸 |
| D.稀硫酸除铁锈更佳 |
您最近一年使用:0次
7 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用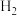 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
您最近一年使用:0次
名校
8 . 下列离子方程式书写正确的是
A.向溴化亚铁溶液中通入少量Cl2: |
B.向氯化钡溶液中通SO2: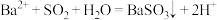 |
C.硫酸铝溶液与过量氨水反应: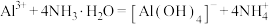 |
D.稀硝酸与过量铁粉反应: |
您最近一年使用:0次
名校
解题方法
9 . 实验室以锈蚀程度很大的废铁屑为原料制备无水 的流程可简要表示如图:
的流程可简要表示如图: ;
;
② ;
;
③在水溶液中 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。
试回答下列问题:
(1)“酸溶”过程中发生主要反应有:① ;②
;② ;③
;③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4) 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(5)“氧化”过程可在如图所示装置中进行。 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为___________
②装置C的作用是___________ 。
③证明装置B溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 的流程可简要表示如图:
的流程可简要表示如图:
 ;
;②
 ;
;③在水溶液中
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。试回答下列问题:
(1)“酸溶”过程中发生主要反应有:①
 ;②
;② ;③
;③(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是
(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)
 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(5)“氧化”过程可在如图所示装置中进行。

 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为②装置C的作用是
③证明装置B溶液中
 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
2024-04-01更新
|
211次组卷
|
2卷引用:湖南省长沙市实验中学2023-2024学年高一下学期期中考试化学试题
10 . 下列离子方程式正确的是
A.氢氧化钡溶液与稀硫酸反应: |
B.足量的氯气和 溶液反应: 溶液反应: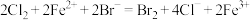 |
C. 溶液中加入过量的 溶液中加入过量的 溶液: 溶液: |
D.将 通入 通入 溶液中: 溶液中: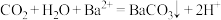 |
您最近一年使用:0次



