名校
解题方法
1 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀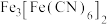 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀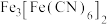 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
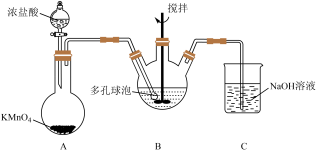
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
2 . 下列各组离子在指定溶液中能大量共存的是
A. 溶液中: 溶液中: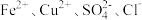 |
B.氨水中: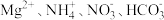 |
C. 溶液中: 溶液中: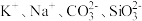 |
D. 溶液中: 溶液中: |
您最近一年使用:0次
2024-04-27更新
|
54次组卷
|
2卷引用:江西省赣州市十八县(市)二十四校2023-2024学年高一下学期期中考试化学试卷
解题方法
3 . 下列反应的离子方程式正确的是
A.氯气尾气处理的原理: |
B.少量 通入 通入 溶液中: 溶液中: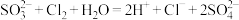 |
C.向红色 溶液中加入过量铁粉至溶液红色褪去: 溶液中加入过量铁粉至溶液红色褪去: |
| D.向含氯化亚铁的氯化铁溶液中通入适量氯气除杂质Fe2+:2Fe2++Cl2=2Fe3++2Clˉ |
您最近一年使用:0次
名校
解题方法
4 . 实验室用 和
和 溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
 和
和 溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
溶液制备碳酸亚铁的装置如图所示(夹持装置已省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是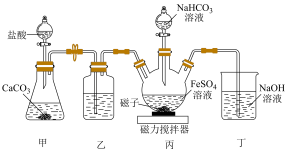
A.装置甲产生 可排除装置中的空气 可排除装置中的空气 |
B.装置乙中盛装的试剂为饱和 溶液 溶液 |
C.装置丙中发生反应的离子方程式: |
| D.反应结束后,将丙中反应液静置、过滤、洗涤、干燥,可得到碳酸亚铁 |
您最近一年使用:0次
2024-03-15更新
|
731次组卷
|
4卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题
江西省宜春市宜丰中学2023-2024学年高一下学期4月期中考试化学试题广东省江门市2023-2024学年高三一模考试化学卷(已下线)压轴题03?物质的制备、检验、分离与提纯(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)选择题1-5
5 . 下列离子方程式正确的是
A. 通入 通入 溶液中反应,若有四分之一的溴元素被氧化: 溶液中反应,若有四分之一的溴元素被氧化: |
| B.NH4HSO4溶液与少量NaOH溶液混合加热:H++OH-=H2O |
C. 溶液中加过量的澄清石灰水: 溶液中加过量的澄清石灰水: |
D.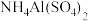 与 与 可能发生的反应: 可能发生的反应: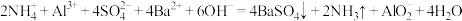 |
您最近一年使用:0次
6 . 铁及其化合物在生产、生活中有重要作用。回答下列问题:
I.硫酸亚铁晶体 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
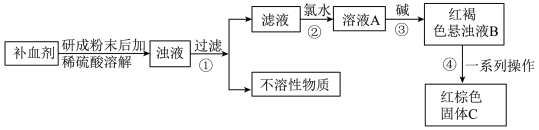
(1)检验经步骤①得到的滤液中是否含有 的方法为
的方法为______ 。
(2)步骤②加入氯水发生反应的离子方程式是______ 。
(3)步骤③产生的红褐色物质成分是______ (写化学式)。
(4)步骤④中一系列操作为______ 、洗涤、干燥、灼烧。
(5)若所取补血剂质量为 ,最终得到红棕色固体
,最终得到红棕色固体 的质量为
的质量为 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为______ (用含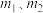 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。
II.高铁酸钾 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

(6)过程①制取 ,理论上需要
,理论上需要 的物质的量为
的物质的量为______ 。步骤②中反应能够发生的原因是______ 。实验室用 饱和溶液制备
饱和溶液制备 胶体的方法是:取
胶体的方法是:取 小烧杯,加入
小烧杯,加入 蒸馏水,将蒸馏水加热至沸腾
蒸馏水,将蒸馏水加热至沸腾______ (将操作补充完整)。
I.硫酸亚铁晶体
 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
(1)检验经步骤①得到的滤液中是否含有
 的方法为
的方法为(2)步骤②加入氯水发生反应的离子方程式是
(3)步骤③产生的红褐色物质成分是
(4)步骤④中一系列操作为
(5)若所取补血剂质量为
 ,最终得到红棕色固体
,最终得到红棕色固体 的质量为
的质量为 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为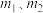 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。II.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
(6)过程①制取
 ,理论上需要
,理论上需要 的物质的量为
的物质的量为 饱和溶液制备
饱和溶液制备 胶体的方法是:取
胶体的方法是:取 小烧杯,加入
小烧杯,加入 蒸馏水,将蒸馏水加热至沸腾
蒸馏水,将蒸馏水加热至沸腾
您最近一年使用:0次
名校
解题方法
7 . 某工厂的工业废水中含有大量的Fe2(SO4)3和较多的CuSO4。为了减少污染并变废为宝,工厂计划从该废水中回收绿矾和金属铜。请根据以下流程图,回答下列问题:
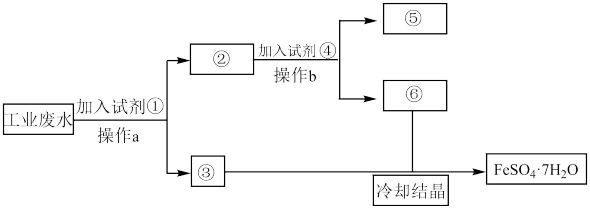
(1)操作a的名称为___________ 。
(2)②中物质为___________ ,试剂④为___________ 。鉴别溶液⑥中的金属阳离子时,应滴加的试剂依次是___________ 。请写出该鉴别过程中属于氧化还原反应的离子方程式___________ 。
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ 。

(1)操作a的名称为
(2)②中物质为
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
名校
8 . Ca(ClO)2、NaClO、FeCl3、Al2O3、Fe2O3、Mn2O7等都是重要的化合物。回答下列问题:
(1)属于酸性氧化物的是______ (填化学式),其相应的钾盐具有_____ (填“强氧化性”或“强还原性”),FeSO4溶液能使该钾盐的酸性溶液褪色,其原因为________ (用离子方程式解释)。
(2)属于“84"消毒液成分的是______ (填化学式),其在空气中易变质,产物之一为碳酸氢钠,写出发生该反应的离子方程式:_______ 。
(3)用覆铜板制作印刷电路板的原理是_______ (用离子方程式表示),检验“腐蚀液”中有无Fe3+的试剂为______ (填化学式)。
(4)将氯气通入冷的_____ (填物质名称)中可制得以Ca(ClO)2为有效成分的漂白粉,该过程中转移2mol电子时,消耗氧化剂与还原剂的质量之比为________ 。
(1)属于酸性氧化物的是
(2)属于“84"消毒液成分的是
(3)用覆铜板制作印刷电路板的原理是
(4)将氯气通入冷的
您最近一年使用:0次
名校
9 . 为除去下列括号内的杂质,所选用的试剂或方法不正确的是
A. 溶液( 溶液( ):加入适量氯水 ):加入适量氯水 |
B. 溶液( 溶液( ):加入适量的 ):加入适量的 溶液 溶液 |
C. 固体( 固体( ):加入过量的 ):加入过量的 溶液,过滤 溶液,过滤 |
D. 溶液( 溶液( ):通入过量的 ):通入过量的 气体 气体 |
您最近一年使用:0次
名校
10 . 关于物质的相关用途,下列说法错误的是
| A.氧化铝可用于耐火材料 | B.通常状况下液氯可以用钢瓶储存运输 |
| C.金属钠着火时,可用泡沫灭火器灭火 | D.配制 溶液时加入少量的铁粉 溶液时加入少量的铁粉 |
您最近一年使用:0次



