1 . 某实验小组探究Fe2+与H2O2反应中滴加KSCN溶液变红色后又褪色的原因,提出如下假设:
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
a.Fe3+被H2O2还原 b.SCN-被O2氧化 c.SCN-被H2O2氧化。
设计如下实验,下列说法错误的是
| 实验 | 滴加试剂 | 现象 |
| I | i.向2mLFeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液 ii.再滴加5滴5%H2O2溶液(物质的量浓度约为1.5mol·L-1、pH约为5) | i.无明显现象 ii.溶液变红,大约10秒左右红色褪去,并测得生成了两种可直接排放到空气中的气体 |
| II | iii.取褪色后溶液两份,一份滴加FeC13溶液;另一份滴加KSCN溶液 iV.取褪色后溶液,滴加盐酸和BaCl2溶液 | iii.一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色 iV.产生白色沉淀 |
| III | V.向2mL0.1mol·L-1FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,观察现象;后通入O2,观察现象 | V.先变红,通入氧气后无明显变化 |
| A.实验I褪色后的溶液中n(H+)变小 | B.通过实验II、III可验证假设c正确 |
C.实验II证明SCN-被氧化成SO | D.实验III的目的是排除假设b |
您最近一年使用:0次
名校
解题方法
2 . 长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验FeSO4溶液的变质程度
①将方案补充完整
②若要使部分变质的FeSO4复原,方法是___________ 。(用离子反应方程式表示)
(2)利用部分变质 的FeSO4溶液制备Fe2O3。
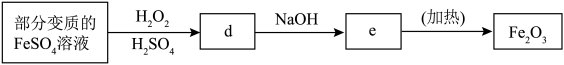
①填写下列各空:
d.___________ ;e.___________ 。
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为___________ 。
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
(1)设计实验检验FeSO4溶液的变质程度
①将方案补充完整
| 实验方案 | 实验现象 | 实验结论 | |
| 步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | ii | FeSO4溶液部分变质 |
| 步骤2 | i | iii | |
(2)利用

①填写下列各空:
d.
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量 Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
您最近一年使用:0次
名校
解题方法
3 . 在含有大量Fe2+、 、
、 的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
 、
、 的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是A.通入过量Cl2: 、 、 、 、 、 、 、 、 |
B.加入少量NaClO溶液: 、 、 、 、 、 、 、 、 |
C.加入过量NaClO和NaOH的混合溶液: 、 、 、 、 、 、 、 、 |
D.加入过量NaOH溶液: 、 、 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-01更新
|
198次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
名校
4 . 已知氧化性: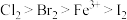 ,还原性:
,还原性: ,下列反应的化学方程式或离子方程式不成立的是
,下列反应的化学方程式或离子方程式不成立的是
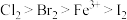 ,还原性:
,还原性: ,下列反应的化学方程式或离子方程式不成立的是
,下列反应的化学方程式或离子方程式不成立的是A. |
B.向 溶液中通入少量氯气; 溶液中通入少量氯气; |
C.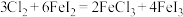 |
D.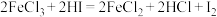 |
您最近一年使用:0次
2024-03-07更新
|
49次组卷
|
2卷引用:湖北省武汉西藏中学2023-2024学年高一下学期5月期中考试化学试题
解题方法
5 . 下列关于铁及其化合物的说法正确的是
| A.检验 FeCl2溶液中的Fe2+,可将酸性KMnO4溶液滴加到该溶液中,若酸性KMnO4溶液褪色,证明含有Fe2+ |
| B.Fe3O4中铁的化合价有+2和+3价,是一种混合物 |
| C.为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,应取少量样品溶于盐酸,滴加KSCN溶液,若溶液未变红,说明铁粉未变质 |
| D. FeCl3溶液腐蚀铜板的离子方程式为2Fe3++Cu=2Fe2++Cu2+ |
您最近一年使用:0次
名校
解题方法
6 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研学小组为测定黑木耳中的含铁量,进行了如下实验。
【铁元素的分离】
(1)高温灼烧黑木耳,使之完全灰化。用足量的硫酸充分溶解,过滤,得滤液。用铁氰化钾溶液检验发现滤液中也存在 ,请用离子方程式说明检验原理
,请用离子方程式说明检验原理_______ 。
【铁元素含量测定】
研学小组提出以下两种测定方案。
Ⅰ.沉淀法:
(2)向(1)中的滤液中加入足量NaOH溶液,过滤、洗涤沉淀、充分加热至恒重、称量。充分加热至恒重前发生的氧化还原反应方程式为_______ 。
Ⅱ.比色法:
方法:
步骤1:取10 mL a mol/L标准 溶液,再加0.1 mL b mol/L KSCN溶液,混合均匀;
溶液,再加0.1 mL b mol/L KSCN溶液,混合均匀;
步骤2:将混合液定容至100 mL得到溶液X,再用色度传感器测定其对光的吸收率;
步骤3:改变标准 溶液的浓度,重复步骤1和步骤2,得到标准色阶(吸光率与标准
溶液的浓度,重复步骤1和步骤2,得到标准色阶(吸光率与标准 溶液浓度的关系)如下图所示:
溶液浓度的关系)如下图所示:
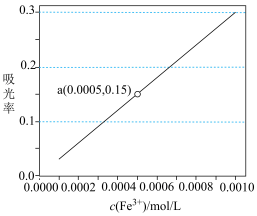
(3)用比色法估测(1)中的滤液中铁元素含量的操作如下:取10 mL(1)中的滤液,再加_______ ,混合均匀,再定容至100 mL,所得溶液颜色与标准色阶比对,即可测得10 mL滤液中铁元素含量。
(4)若(1)中取9 g黑木耳处理后得到15 mL滤液,按照比色法测得吸光率为上图中a点,则9g黑木耳中含铁元素的质量为_______ 。
(5)若将步骤1中的标准 溶液与(3)中的滤液用量均减少为原来的
溶液与(3)中的滤液用量均减少为原来的 ,其他操作相同,对比色阶,则测得的黑木耳中铁元素的含量
,其他操作相同,对比色阶,则测得的黑木耳中铁元素的含量_______ 。(填“偏高”、“偏低”或“不变”)
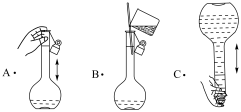
(6)用容量瓶配制a mol/L标准 溶液的部分操作如下,其中正确的是
溶液的部分操作如下,其中正确的是_______ ,若定容时仰视读数,则测得的黑木耳中铁元素的含量_______ 。(填“偏高”、“偏低”或“不变”)
【铁元素的分离】
(1)高温灼烧黑木耳,使之完全灰化。用足量的硫酸充分溶解,过滤,得滤液。用铁氰化钾溶液检验发现滤液中也存在
 ,请用离子方程式说明检验原理
,请用离子方程式说明检验原理【铁元素含量测定】
研学小组提出以下两种测定方案。
Ⅰ.沉淀法:
(2)向(1)中的滤液中加入足量NaOH溶液,过滤、洗涤沉淀、充分加热至恒重、称量。充分加热至恒重前发生的氧化还原反应方程式为
Ⅱ.比色法:
方法:
步骤1:取10 mL a mol/L标准
 溶液,再加0.1 mL b mol/L KSCN溶液,混合均匀;
溶液,再加0.1 mL b mol/L KSCN溶液,混合均匀;步骤2:将混合液定容至100 mL得到溶液X,再用色度传感器测定其对光的吸收率;
步骤3:改变标准
 溶液的浓度,重复步骤1和步骤2,得到标准色阶(吸光率与标准
溶液的浓度,重复步骤1和步骤2,得到标准色阶(吸光率与标准 溶液浓度的关系)如下图所示:
溶液浓度的关系)如下图所示:
(3)用比色法估测(1)中的滤液中铁元素含量的操作如下:取10 mL(1)中的滤液,再加
(4)若(1)中取9 g黑木耳处理后得到15 mL滤液,按照比色法测得吸光率为上图中a点,则9g黑木耳中含铁元素的质量为
(5)若将步骤1中的标准
 溶液与(3)中的滤液用量均减少为原来的
溶液与(3)中的滤液用量均减少为原来的 ,其他操作相同,对比色阶,则测得的黑木耳中铁元素的含量
,其他操作相同,对比色阶,则测得的黑木耳中铁元素的含量(6)用容量瓶配制a mol/L标准
 溶液的部分操作如下,其中正确的是
溶液的部分操作如下,其中正确的是
您最近一年使用:0次
名校
7 . 向500 含
含 、
、 、
、 的溶液中缓慢通入
的溶液中缓慢通入 L
L (标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
(标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是

 含
含 、
、 、
、 的溶液中缓慢通入
的溶液中缓慢通入 L
L (标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
(标准状况),测得溶液中部分离子的物质的量与V的关系如图所示。下列叙述正确的是
A.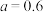 |
B. 时反应为 时反应为 |
C.原溶液中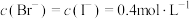 |
D.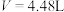 时总反应为 时总反应为 |
您最近一年使用:0次
2024-02-23更新
|
250次组卷
|
2卷引用:湖北省荆州八县市2023-2024学年高一上学期期末联考化学试题
解题方法
8 . 下列实验操作能达到目的是
| 选项 | 操作 | 目的 |
| A | 将 和 和 混合气体通过足量的 混合气体通过足量的 粉末 粉末 | 提纯 |
| B | 向含 的 的 溶液中通入适量氯气 溶液中通入适量氯气 | 除去 |
| C | 分别向 溶液、 溶液、 溶液中滴加澄清石灰水 溶液中滴加澄清石灰水 | 区分 溶液和 溶液和 溶液 溶液 |
| D | 在饱和 溶液中滴加 溶液中滴加 溶液 溶液 | 制备 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 化学与生活息息相关,下列做法不正确的是
| A.实验室金属钠着火时使用沙子扑灭 |
| B.使用漂白粉时滴入几滴醋酸,可提高漂白效率 |
| C.保存硫酸亚铁溶液时,要向其中加入少量铁粉 |
| D.浓硫酸溅到皮肤上时立即用稀碳酸钠溶液冲洗 |
您最近一年使用:0次
10 . 下列实验现象和结论不相符的是
| 操作及现象 | 结论 | |
| A | 向某溶液中加入 溶液,产生红褐色沉淀 溶液,产生红褐色沉淀 | 溶液中没有 |
| B | 向盛 固体的试管中滴入少量水并用温度计检测,温度计读数降低 固体的试管中滴入少量水并用温度计检测,温度计读数降低 |  溶于水伴有吸热现象 溶于水伴有吸热现象 |
| C | 氢气可在氯气中安静燃烧,发出苍白色火焰 | 燃烧不一定需要氧气 |
| D | 向某溶液中加入 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 溶液中可能含有 或 或 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



