1 . 下列物质之间有如下反应关系:
(1)写出下列物质的化学式:
A___________ B___________ D___________ 甲___________ 乙___________ 丙___________ ;
(2)写出E→C反应的化学方程式:___________ ;
(3)写出B+丙反应的离子方程式:___________ 。
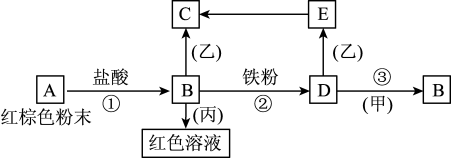
(1)写出下列物质的化学式:
A
(2)写出E→C反应的化学方程式:
(3)写出B+丙反应的离子方程式:
您最近一年使用:0次
解题方法
2 . 下列说法中不正确的是
| A.赤铁矿的主要成分与铁锈的主要成分相同 |
| B.Fe3O4可由单质直接化合而得到 |
| C.FeCl2、FeCl3、Fe(OH)3都可通过化合反应生成 |
| D.某溶液中滴加氯水,然后滴加KSCN溶液,溶液显红色,该溶液中一定含有Fe2+ |
您最近一年使用:0次
3 . 下列有关物质检验方法不合理的是
| A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ |
| B.用酸性KMnO4溶液检验Fe2(SO4)3溶液中是否含有FeSO4 |
| C.检验绿矾晶体是否已氧化变质,可将绿矾晶体溶于稀H2SO4后滴加KSCN溶液,再观察溶液是否变红 |
D.向某溶液中加入适量BaCl2溶液,产生白色沉淀,说明溶液中含有 |
您最近一年使用:0次
名校
解题方法
4 . 实验室以锈蚀程度很大的废铁屑为原料制备无水 的流程可简要表示如图:
的流程可简要表示如图: ;
;
② ;
;
③在水溶液中 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。
试回答下列问题:
(1)“酸溶”过程中发生主要反应有:① ;②
;② ;③
;③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4) 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(5)“氧化”过程可在如图所示装置中进行。 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为___________
②装置C的作用是___________ 。
③证明装置B溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 的流程可简要表示如图:
的流程可简要表示如图:
 ;
;②
 ;
;③在水溶液中
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。试回答下列问题:
(1)“酸溶”过程中发生主要反应有:①
 ;②
;② ;③
;③(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是
(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)
 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(5)“氧化”过程可在如图所示装置中进行。

 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为②装置C的作用是
③证明装置B溶液中
 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
2024-04-01更新
|
210次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一下学期教学测评月考卷(五)化学试题
5 . 某同学利用如图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
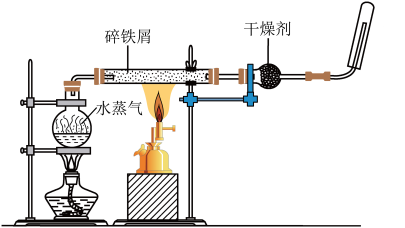
(1)试管中发生反应的化学方程式为___________ 。
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是___________ (只有一个选项符合题意),若溶液未变红,则试管中固体是___________ (只有一个选项符合题意)。
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式___________ 。
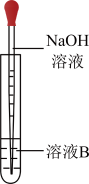
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是___________ ,并且配制时应加入少量___________ 。

(1)试管中发生反应的化学方程式为
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式

(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是
您最近一年使用:0次
6 . 下列离子的检验,所用试剂(或方法)及实验现象均正确的是
| 选项 | 离子 | 试剂(或方法) | 实验现象 |
| A | Fe2+ | 先加KSCN溶液,再加氯水 | 开始无现象,加氯水溶液变红 |
| B |  | 焰色试验 | 火焰呈紫色 |
| C | CO |  溶液 溶液 | 产生气泡 |
| D |  |  溶液、稀盐酸 溶液、稀盐酸 | 产生白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 铁是人类较早使用的金属之一,根据铁及其化合物之间的相互转化,回答下列问题:
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是______ 。
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:______ 。
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为______ 。
②能检验溶液A中含有Fe2+的试剂是______ (填字母)。
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为______ 。
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为______ 。
(1)Fe2+易被人体吸收,医生建议在服用补铁剂时,同时服用维生素C.维生素C的作用是
(2)印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的离子方程式:
(3)某废料铁泥的主要成分为Fe2O3、FeO、Fe和杂质(杂质不与硫酸反应)。现取wg废料铁泥提取Fe2O3,设计实验流程如下:

①分离溶液A和沉淀C的实验操作为
②能检验溶液A中含有Fe2+的试剂是
A.铁粉 B.酸性KMnO4溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为
④若最终获得ngFe2O3,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次
8 . 部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
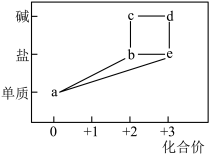

| A.a分别在纯氧中点燃和在高温下与水蒸气反应所生成的化合物相同 |
| B.b与e的相互转化可通过化合反应来实现 |
| C.加入a可除去b的硫酸盐溶液中混有的硫酸铜杂质 |
| D.c在空气中由灰绿色最终变为红褐色的d |
您最近一年使用:0次
名校
解题方法
9 . 铁是人体必需的微量元素,下面是一种常见补铁药品说明书中的部分内容:该药品含 33%~36%,不溶于水但能溶于人体中的胃酸:与维生素C(Vc)同服可增加本品吸收。某同学设计了以下实验检测该补铁药品中是否含有
33%~36%,不溶于水但能溶于人体中的胃酸:与维生素C(Vc)同服可增加本品吸收。某同学设计了以下实验检测该补铁药品中是否含有 并探究Vc的作用:
并探究Vc的作用:不正确 的是
 33%~36%,不溶于水但能溶于人体中的胃酸:与维生素C(Vc)同服可增加本品吸收。某同学设计了以下实验检测该补铁药品中是否含有
33%~36%,不溶于水但能溶于人体中的胃酸:与维生素C(Vc)同服可增加本品吸收。某同学设计了以下实验检测该补铁药品中是否含有 并探究Vc的作用:
并探究Vc的作用:
A.试剂1为 溶液,目的是溶解药片 溶液,目的是溶解药片 |
B.加入 溶液后溶液变为淡红色,说明溶液中有少量 溶液后溶液变为淡红色,说明溶液中有少量 |
| C.加入Vc后红色溶液颜色褪去,说明Vc具有一定的氧化性 |
| D.新制氯水可替换为双氧水进行实验 |
您最近一年使用:0次
2024-02-16更新
|
106次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
10 . 对下列图像的解释正确的是
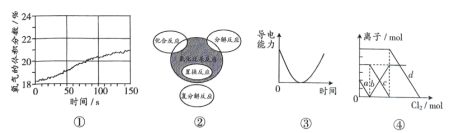

| A.图①表示强光照射氯水,氧气体积分数与时间的关系,说明在光照下,水分解生成了氧气 |
| B.过氧化钠与H2O的反应类型属于图②的阴影部分 |
| C.图③可表示向硫酸铜溶液中逐滴加入氢氧化钠溶液时,混合溶液导电能力随时间的变化 |
D.将Cl2通入FeI2和FeBr2的混合溶液中,图④中a曲线表示 随氯气加入量的变化曲线 随氯气加入量的变化曲线 |
您最近一年使用:0次
2024-02-03更新
|
80次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一下学期第一次月考化学试题



