名校
解题方法
1 . 某小组同学对 与
与 在不同的
在不同的 下反应进行探究。
下反应进行探究。
(1)测得 溶液
溶液 为10,
为10, 溶液
溶液 为5,用离子方程式表示
为5,用离子方程式表示 溶液显碱性的原因
溶液显碱性的原因___________ 。
(2)调节 与
与 混合后的初始
混合后的初始 ,实验记录如下:
,实验记录如下:
资料:ⅰ. :白色,不溶于水,可溶于过量
:白色,不溶于水,可溶于过量 溶液。
溶液。
ⅱ. :棕黑色,不溶于水,能和酸反应。
:棕黑色,不溶于水,能和酸反应。
针对实验 中白色沉淀提出两种推测:
中白色沉淀提出两种推测:
推测1:白色沉淀为 。
。
推测2:白色沉淀为 。
。
①推测1产生该沉淀的反应用离子方程式表示___________ 。
②推测2的理论依据是___________ 。
③取 、
、 中白色沉淀,分别置于过量
中白色沉淀,分别置于过量 溶液中,沉淀均溶解经实验证明白色沉淀不是
溶液中,沉淀均溶解经实验证明白色沉淀不是 ,实验过程:另取
,实验过程:另取 固体置于
固体置于___________ 溶液中,未溶解。
(3)为确认 组成,将
组成,将 中
中 过滤、洗涤,继续实验:
过滤、洗涤,继续实验:
Ⅰ.向 中滴加稀盐酸,无明显变化;
中滴加稀盐酸,无明显变化;
Ⅱ.向 中加入过量浓
中加入过量浓 ,产生红棕色气体;
,产生红棕色气体;
Ⅲ.用 、
、 检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
①Ⅰ的目的是___________ 。
②根据Ⅲ的现象,可判断 的元素组成
的元素组成___________ 。
③Ⅱ中反应的化学方程式是___________ 。
(4)综合以上实验,分析 产生的可能原因:
产生的可能原因:
①甲同学认为随着溶液酸性增强, 中的
中的 氧化性增强。
氧化性增强。
②乙同学认为___________ 。
 与
与 在不同的
在不同的 下反应进行探究。
下反应进行探究。(1)测得
 溶液
溶液 为10,
为10, 溶液
溶液 为5,用离子方程式表示
为5,用离子方程式表示 溶液显碱性的原因
溶液显碱性的原因(2)调节
 与
与 混合后的初始
混合后的初始 ,实验记录如下:
,实验记录如下:| 实验 |  | 现象 |
 | 10 | 产生白色沉淀,稍后沉淀溶解 |
 | 6 | 产生白色沉淀,一段时间后,沉淀未溶解 |
 | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质 |
 :白色,不溶于水,可溶于过量
:白色,不溶于水,可溶于过量 溶液。
溶液。ⅱ.
 :棕黑色,不溶于水,能和酸反应。
:棕黑色,不溶于水,能和酸反应。针对实验
 中白色沉淀提出两种推测:
中白色沉淀提出两种推测:推测1:白色沉淀为
 。
。推测2:白色沉淀为
 。
。①推测1产生该沉淀的反应用离子方程式表示
②推测2的理论依据是
③取
 、
、 中白色沉淀,分别置于过量
中白色沉淀,分别置于过量 溶液中,沉淀均溶解经实验证明白色沉淀不是
溶液中,沉淀均溶解经实验证明白色沉淀不是 ,实验过程:另取
,实验过程:另取 固体置于
固体置于(3)为确认
 组成,将
组成,将 中
中 过滤、洗涤,继续实验:
过滤、洗涤,继续实验:Ⅰ.向
 中滴加稀盐酸,无明显变化;
中滴加稀盐酸,无明显变化;Ⅱ.向
 中加入过量浓
中加入过量浓 ,产生红棕色气体;
,产生红棕色气体;Ⅲ.用
 、
、 检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。
检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀。①Ⅰ的目的是
②根据Ⅲ的现象,可判断
 的元素组成
的元素组成③Ⅱ中反应的化学方程式是
(4)综合以上实验,分析
 产生的可能原因:
产生的可能原因:①甲同学认为随着溶液酸性增强,
 中的
中的 氧化性增强。
氧化性增强。②乙同学认为
您最近半年使用:0次
2021-10-19更新
|
686次组卷
|
2卷引用:2020年北京高考化学真题变式题11-19
名校
解题方法
2 . 下列实验操作和现象、结论或目的均正确的是
| 选项 | 操作和现象 | 结论或目的 |
| A | 向某溶液中滴加盐酸,再加Ba(NO3)2溶液,有白色沉淀生成 | 原溶液中一定含有SO |
| B | CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液,溶液不显红色 | 黑色固体中可能含有Fe3O4 |
| C | 用托盘天平称取1.0g NaOH固体,在烧杯中加少量蒸馏水溶解,转移至250mL容量瓶中定容 | 配制250mL 0.1nol/L的NaOH溶液 |
| D | 用 pH 试纸分别测定等浓度的 NaClO 和NaHCO3溶液的 pH,pH:NaClO> NaHCO3 | 碱性:NaClO> NaHCO3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . CuCl是重要的化工原料,研究人员提出用有机硅生产中产生的废触煤(生产中未反应的硅粉和催化剂混合物,主要成分为粉末状的硅、铜、锌和碳)来生产CuCl,并设计出如下图所示流程图。
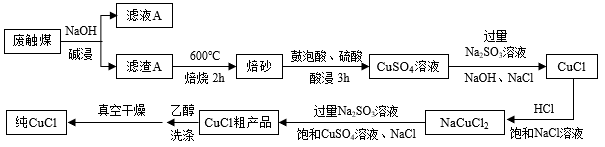
已知:氯化亚铜微溶于水,不溶于乙醇,溶于浓盐酸和氨水生成络合物。
(1)已知锌与铝性质相似,既能与强酸反应又能与强碱反应。写出碱浸时锌与NaOH反应的离子方程式___________ 。
(2)实验室模拟焙烧的过程,除三脚架外,还需要用到的实验仪器是___________ 。(从下列仪器中选出所需的仪器,填字母)
A.蒸发皿 B.坩埚 C.表面皿 D.泥三角 E酒精灯 F.干燥器 G.坩埚钳
(3)焙砂的主要成分是___________ ,写出提高焙砂浸取率和速率的两种方法___________ ,___________ 。
(4)写出由NaCuCl2生成CuCl的离子方程式___________ ,NaCl的作用是___________ ,用乙醇洗涤CuCl晶体的优点是___________ 。
(5)准确称取氯化亚铜产品10.00 g,将其置于过量的FeCl3溶液中,待样品完全溶解后加入适量稀硫酸和水配成1000 mL溶液,取50 mL用0.0500 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液16.67 mL,反应中 被还原为Cr3+,产品中CuCl的质量分数为
被还原为Cr3+,产品中CuCl的质量分数为___________ 。

已知:氯化亚铜微溶于水,不溶于乙醇,溶于浓盐酸和氨水生成络合物。
(1)已知锌与铝性质相似,既能与强酸反应又能与强碱反应。写出碱浸时锌与NaOH反应的离子方程式
(2)实验室模拟焙烧的过程,除三脚架外,还需要用到的实验仪器是
A.蒸发皿 B.坩埚 C.表面皿 D.泥三角 E酒精灯 F.干燥器 G.坩埚钳
(3)焙砂的主要成分是
(4)写出由NaCuCl2生成CuCl的离子方程式
(5)准确称取氯化亚铜产品10.00 g,将其置于过量的FeCl3溶液中,待样品完全溶解后加入适量稀硫酸和水配成1000 mL溶液,取50 mL用0.0500 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液16.67 mL,反应中
 被还原为Cr3+,产品中CuCl的质量分数为
被还原为Cr3+,产品中CuCl的质量分数为
您最近半年使用:0次
名校
解题方法
4 . 有一包白色固体(为一种二元酸的正盐),下表为进行相关实验的部分实验报告。
(1)请根据实验现象,将你作出的判断填在表格内的相应位置。
(2)若想确认此白色固体的成分,应在步骤________ (填步骤序号)中加入试剂A,试剂A为_________ 。
(3)若在步骤②的操作中,加入试剂A后仍有白色沉淀,写出据此确认的溶液X与氢氧化钡溶液加热反应的离子方程式___________________________
(1)请根据实验现象,将你作出的判断填在表格内的相应位置。
| 步骤序号 | 操作 | 实验现象 | 判断 |
| ① | 取固体溶于水,得溶液X | 得到无色溶液 | |
| ② | 取少量溶液X,加入氯化钡溶液 | 生成白色沉淀 | 可能含有 |
| ③ | 取少量溶液X,加入浓氢氧化钠溶液,加热,并在试管口用湿润的红色石蕊试纸检验 | 试纸变蓝 | 含有 |
| 结论:此白色固体可能是 | |||
(3)若在步骤②的操作中,加入试剂A后仍有白色沉淀,写出据此确认的溶液X与氢氧化钡溶液加热反应的离子方程式
您最近半年使用:0次
2020-10-28更新
|
80次组卷
|
2卷引用:安徽省六安市城南中学2021届高三上学期第一次月考化学试题
名校
解题方法
5 . 焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5,装置Ⅲ中有Na2S2O5黄色晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5。

(1)装置Ⅰ中盛放浓硫酸的仪器名称为_____ ;装置Ⅰ中产生气体的化学方程式为______ 。
(2)装置Ⅱ的作用之一是观察SO2的生成速率,盛装的试剂为_____ 。
(3)要从装置Ⅲ中获得已析出的晶体,可采取的分离方法是_____ 。
实验二 焦亚硫酸钠的性质:Na2S2O5溶于水即生成NaHSO3
(4)证明NaHSO3溶液中 的电离程度大于水解程度,可采用的实验方法是
的电离程度大于水解程度,可采用的实验方法是_____ (填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸 d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是_______ 。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时化学方程式为:SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为_______ g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果______ (填“偏高”“偏低”或“不变”)。
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5,装置Ⅲ中有Na2S2O5黄色晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5。

(1)装置Ⅰ中盛放浓硫酸的仪器名称为
(2)装置Ⅱ的作用之一是观察SO2的生成速率,盛装的试剂为
(3)要从装置Ⅲ中获得已析出的晶体,可采取的分离方法是
实验二 焦亚硫酸钠的性质:Na2S2O5溶于水即生成NaHSO3
(4)证明NaHSO3溶液中
 的电离程度大于水解程度,可采用的实验方法是
的电离程度大于水解程度,可采用的实验方法是a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸 d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时化学方程式为:SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为
②在上述实验过程中,若有部分HI被空气氧化,则测得结果
您最近半年使用:0次
2020-09-21更新
|
457次组卷
|
2卷引用:广东省广州大学附属中学等三校2021届高三上学期返校联考化学试题
6 . 铜及其化合物在生产生活中有广泛应用
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是________________ ,验证SO2的方法是________________ 。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②___________ 。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加热,可生成CuC1沉淀,写出生成CuCl的离子方程式______________ 。
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:
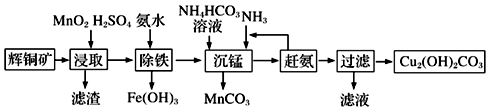
①辉铜矿在浸取前要富集与粉碎,粉碎的好处是___________ 。
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式___________ 。
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过_________ mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
(1)工业上以黄铜矿(CuFeS2) 为原料,采用火法熔炼工艺生产铜的中间过程会发生反应:2Cu2O+Cu2S
 6Cu+SO2↑ 该反应的氧化剂是
6Cu+SO2↑ 该反应的氧化剂是(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入H2O2,反应一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜。温度控制在50℃~60℃的原因有:①加快反应速率;②
(3)碱式碳酸铜在有机催化剂、烟火制造和颜料、农药生产中有广泛的应用。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备碱式碳酸铜的流程如下:

①辉铜矿在浸取前要富集与粉碎,粉碎的好处是
②浸取过程中可得到一种黄色单质,写出浸取时主要反应的化学方程式
③“除铁”这一步反应在25℃进行,加入氨水调节溶液pH为4后,溶液中铜离子最大浓度不超过
您最近半年使用:0次
2018-08-30更新
|
297次组卷
|
2卷引用:【全国省级联考】广东省2017-2018学年高二第二学期期末检测理科综合化学试题



