1 . 下列说法不正确的是
| A.冠醚与碱金属离子之间的配位键属于共价键,冠醚与碱金属离子形成配合物得到的晶体里还有阴离子,这类晶体是离子晶体 |
| B.制备晶体的三种途径都可以制得有重要价值的大晶体。例如芯片的基质是二氧化硅,它是由熔融态水晶制备的,俗称“拉单晶”。 |
| C.超分子实际应用的实例较多,第一个例子杯酚分离C60和C70,第二个例子是冠醚识别碱金属离子。 |
| D.低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链而没有封闭的环状结构,这一结构决定了它具有手性(左、右型) |
您最近一年使用:0次
2 . 半导体材料砷化硼(BAs)的晶胞结构如下图所示,可看作是金刚石晶胞内部的C原子被As原子代替、顶点和面心的C原子被B原子代替。下列说法正确的是
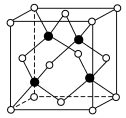

| A.基态As原子的核外电子排布式为[Ar]4s24p3 |
| B.砷化硼(BAs)晶体属于分子晶体 |
| C.1molBAs晶体中含有4molB-As键 |
| D.与同一个B原子相连的As原子构成的立体构型为正四面体形 |
您最近一年使用:0次
3 . (1)冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石的化学方程式为:
2 Al(OH)3 + 12 HF + 3 Na2CO3 = 2 Na3AlF6 + 3CO2 + 9 H2O。上述反应中有两种元素在元素周期表中的位置相邻,二者的电负性较小的是_______ ,上述反应的生成物中极性分子的空间构型呈__________
(2)已知NF3与NH3的组成结构相似,但NF3的沸点比NH3的沸点(-33℃)低得多,其主要原因是____________ 。
(3)一种有机EL材料结构如图,该分子内存在作用力有_________ 
A.σ键 B.π键 C.配位键
D.氢键 E.金属键 F.离子键

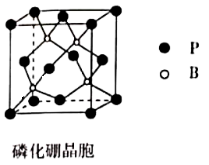
(4)2019年电子科技大学孙旭平教授团队报道了一种磷化硼纳米颗粒作为高选择性 CO2电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于 极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示,立方氮化硼是一种新型无机非金属材料,熔点很高.硬度很大,立方氮化硼晶体属于_______________ (填晶体类型),氮化硼与磷化硼具有相似的结构,比较 BN 和 BP 的熔点大小并说明原因:_____________ ;
2 Al(OH)3 + 12 HF + 3 Na2CO3 = 2 Na3AlF6 + 3CO2 + 9 H2O。上述反应中有两种元素在元素周期表中的位置相邻,二者的电负性较小的是
(2)已知NF3与NH3的组成结构相似,但NF3的沸点比NH3的沸点(-33℃)低得多,其主要原因是
(3)一种有机EL材料结构如图,该分子内存在作用力有

A.σ键 B.π键 C.配位键
D.氢键 E.金属键 F.离子键

(4)2019年电子科技大学孙旭平教授团队报道了一种磷化硼纳米颗粒作为高选择性 CO2电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于 极高温的空气环境时也具有抗氧化作用。其晶胞结构如图所示,立方氮化硼是一种新型无机非金属材料,熔点很高.硬度很大,立方氮化硼晶体属于

您最近一年使用:0次
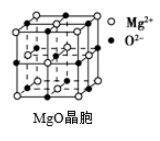
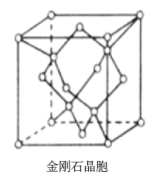
4 . 晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着它们具有不同的性质和用途。几种晶胞的结构示意图如下:

回答下列问题:
(1)这些晶体中粒子之间以共价键结合形成的是___________ 。
(2)每个Cu晶胞中包含的铜原子个数是___________ ,铜原子在晶胞中的空间占有率为___________ 。
(3)NaCl晶胞与MgO晶胞结构相同,NaCl晶体的熔点___________ (填“大于”或“小于”)MgO晶体的熔点,原因是___________ 。
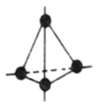
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元(如图)取代形成的一种新型三维立方晶体结构。已知T-碳晶胞参数为a nm,阿伏加德罗常数为NA,则T-碳的密度为___________ g/cm3(列出计算式)。



回答下列问题:
(1)这些晶体中粒子之间以共价键结合形成的是
(2)每个Cu晶胞中包含的铜原子个数是
(3)NaCl晶胞与MgO晶胞结构相同,NaCl晶体的熔点
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元(如图)取代形成的一种新型三维立方晶体结构。已知T-碳晶胞参数为a nm,阿伏加德罗常数为NA,则T-碳的密度为

您最近一年使用:0次
2021-05-15更新
|
469次组卷
|
3卷引用:山东省潍坊市2020-2021学年高二下学期期中考试化学试题
5 . 下列叙述正确的是
A.镁晶体中1个 只与2个价电子存在强烈的相互作用 只与2个价电子存在强烈的相互作用 |
| B.在二氧化硅晶体中,原子未排列成紧密堆积结构的原因是共价键具有方向性和饱和性 |
| C.熔点为2700℃,导电性好、延展性强的晶体一定是共价晶体 |
| D.离子晶体中晶格能的大小仅与阴、阳离子之间的距离有关 |
您最近一年使用:0次
6 . 方英石(SiO2)结构和金刚石相似,其结构单元如图,下列有关说法正确的是


| A.图示结构单元中实际占有18个硅原子 |
| B.1 mol Si形成2 mol Si—O键 |
| C.方英石晶体中的Si采用的是sp3杂化 |
| D.方英石晶体中,Si-O键之间的夹角为90° |
您最近一年使用:0次
2021-05-11更新
|
371次组卷
|
3卷引用:四川省成都市郫都区2020-2021学年高二下学期期中考试化学试题
四川省成都市郫都区2020-2021学年高二下学期期中考试化学试题 (已下线)第3.2.2讲 共价晶体-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)吉林省洮南市第一中学2022-2023学年高二下学期学习质量检测化学试卷
7 . 现有短周期主族元素X、Y、Q、R、T。其中基态R原子核外电子占据3个能级,每个能级上电子数相等;常温常压下,X、Y能组成2种液态化合物,且一种液态化合物可以转化成另一种液态化合物;短周期元素中,Q的第一电离能最小,Q2T能促进水的电离。五种元素的原子半径与原子序数关系如图所示。下列推断正确的是


| A.上述五种元素只能组成3种类型的晶体 |
| B.1个R的单质晶胞中可能含有8个R原子 |
| C.由Y和Q组成的晶体只可能含一种类型的化学键 |
| D.Q2T的晶格能大于Q2Y的晶格能 |
您最近一年使用:0次
2021-05-08更新
|
139次组卷
|
2卷引用:河南省开封市五县联考2020-2021学年高二下学期期中考试化学试题
8 . (1)写出 的电子式:
的电子式:___________ 。
(2)二氧化硅熔化需1723℃,而干冰升华在常温下就可以进行,解释前者比后者所需温度高很多的原因:___________ 。
(3)已知: 比
比 易电离出
易电离出 。请用一个离子方程式证明:
。请用一个离子方程式证明:___________ 。
 的电子式:
的电子式:(2)二氧化硅熔化需1723℃,而干冰升华在常温下就可以进行,解释前者比后者所需温度高很多的原因:
(3)已知:
 比
比 易电离出
易电离出 。请用一个离子方程式证明:
。请用一个离子方程式证明:
您最近一年使用:0次
9 . 完成下列晶体知识。

I.硼酸(H3BO3)为片层状白色晶体,层内H3BO3分子间通过氢键相连,如图1。H3BO3水溶液中存在 的平衡。
的平衡。
(1)1mol硼酸晶体中有_______ mol氢键。
(2)下列关于硼酸的说法正确的是_______ (填序号)。
a.H3BO3是一元酸
b.其水溶液中,水的电离平衡受到抑制
c.晶体中有氢键,因此硼酸分子较稳定
II.某离子晶体晶胞结构如上图2所示。X、Y分别位于立方体的顶角和中心。
(1)该晶体的化学式_______ 。
(2)晶体中距离最近的2个X与1个Y形成的夹角的度数_______ 。
III.金刚砂(SiC),其晶胞结构,如图3。
(1)金刚砂晶体中每个C原子周围最近的C原子数目为_______ 。
(2)金刚砂(SiC)为三维骨架结构,由共价键形成的碳、硅原子环中,最小的环上共有_______ 个原子。
IV.冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如图4。
(1)每个冰晶胞平均占有_______ 个水分子。
(2)冰晶胞与金刚石晶胞微粒排列方式相同的原因是_______ (填序号)。
a.水中的O和金刚石中的C都是sp3杂化
b.水分子间的氢键具有方向性,且每个水分子可与相邻的4个水分子形成4个氢键
c.冰和金刚石都属于共价晶体

I.硼酸(H3BO3)为片层状白色晶体,层内H3BO3分子间通过氢键相连,如图1。H3BO3水溶液中存在
 的平衡。
的平衡。(1)1mol硼酸晶体中有
(2)下列关于硼酸的说法正确的是
a.H3BO3是一元酸
b.其水溶液中,水的电离平衡受到抑制
c.晶体中有氢键,因此硼酸分子较稳定
II.某离子晶体晶胞结构如上图2所示。X、Y分别位于立方体的顶角和中心。
(1)该晶体的化学式
(2)晶体中距离最近的2个X与1个Y形成的夹角的度数
III.金刚砂(SiC),其晶胞结构,如图3。
(1)金刚砂晶体中每个C原子周围最近的C原子数目为
(2)金刚砂(SiC)为三维骨架结构,由共价键形成的碳、硅原子环中,最小的环上共有
IV.冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如图4。
(1)每个冰晶胞平均占有
(2)冰晶胞与金刚石晶胞微粒排列方式相同的原因是
a.水中的O和金刚石中的C都是sp3杂化
b.水分子间的氢键具有方向性,且每个水分子可与相邻的4个水分子形成4个氢键
c.冰和金刚石都属于共价晶体
您最近一年使用:0次
10 . 石墨晶体是层状结构如图。以下有关石墨晶体的说法正确的是


| A.石墨的熔点、沸点都比金刚石的低 |
B.石墨中的C原子均为 杂化 杂化 |
| C.每个六元环完全占有的碳原子数是2 |
| D.石墨晶体中存在的化学键有共价键、金属键和范德华力 |
您最近一年使用:0次
2021-05-06更新
|
646次组卷
|
3卷引用:山西省运城市2020-2021学年高二下学期期中考试化学(A)试题



