1 . 化学反应都会伴随能量变化,化学能可以与热能、电能、光能等各种形式的能量之间相互转化,回答下列问题:
(1)下列反应中,生成物总能量高于反应物总能量的是___________(填字母)。
(2)利用如图所示装置测定中和反应反应热的实验步骤如下: 盐酸倒入内筒中,测出盐酸温度;
盐酸倒入内筒中,测出盐酸温度;
Ⅱ.用另一量筒量取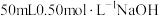 溶液,并用同一温度计测出其温度;
溶液,并用同一温度计测出其温度;
Ⅲ.将 溶液倒入内筒中,使之与盐酸混合均匀,测得混合液最高温度。
溶液倒入内筒中,使之与盐酸混合均匀,测得混合液最高温度。
① 溶液稍过量的原因是
溶液稍过量的原因是___________ 。
②倒入 溶液的正确操作是
溶液的正确操作是___________ (填字母)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
③假设盐酸和 溶液的密度都是
溶液的密度都是 ,中和反应后生成溶液的比热容
,中和反应后生成溶液的比热容 。为了计算中和反应的反应热,某学生实验记录如表数据。则生成
。为了计算中和反应的反应热,某学生实验记录如表数据。则生成 水的反应热
水的反应热
___________  (保留三位有效数字)。
(保留三位有效数字)。
(3)以 为原料合成
为原料合成 依然是“碳达峰”环境下的科研热点,相关反应如下:
依然是“碳达峰”环境下的科研热点,相关反应如下:
i.

ii.
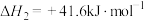
iii.
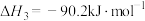
①
___________  。
。
②部分键能的数据如下表所示,则
___________ 。
(4) 和
和 是两种比较稳定的温室气体,科学家利用原电池装置,实现了两种分子的耦合转化,装置如图所示。
是两种比较稳定的温室气体,科学家利用原电池装置,实现了两种分子的耦合转化,装置如图所示。___________ (填“正”或“负”)极。
②催化电极1的电极反应式为___________ 。
(1)下列反应中,生成物总能量高于反应物总能量的是___________(填字母)。
| A.锌与稀硫酸 | B.食物的腐烂 |
| C.碳酸钙分解 | D.红热的木炭与水蒸气 |
(2)利用如图所示装置测定中和反应反应热的实验步骤如下:
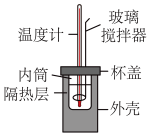
 盐酸倒入内筒中,测出盐酸温度;
盐酸倒入内筒中,测出盐酸温度;Ⅱ.用另一量筒量取
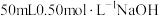 溶液,并用同一温度计测出其温度;
溶液,并用同一温度计测出其温度;Ⅲ.将
 溶液倒入内筒中,使之与盐酸混合均匀,测得混合液最高温度。
溶液倒入内筒中,使之与盐酸混合均匀,测得混合液最高温度。①
 溶液稍过量的原因是
溶液稍过量的原因是②倒入
 溶液的正确操作是
溶液的正确操作是A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
③假设盐酸和
 溶液的密度都是
溶液的密度都是 ,中和反应后生成溶液的比热容
,中和反应后生成溶液的比热容 。为了计算中和反应的反应热,某学生实验记录如表数据。则生成
。为了计算中和反应的反应热,某学生实验记录如表数据。则生成 水的反应热
水的反应热
 (保留三位有效数字)。
(保留三位有效数字)。| 实验序号 | 起始温度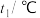 | 终止温度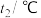 | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(3)以
 为原料合成
为原料合成 依然是“碳达峰”环境下的科研热点,相关反应如下:
依然是“碳达峰”环境下的科研热点,相关反应如下:i.


ii.

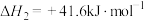
iii.

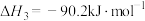
①

 。
。②部分键能的数据如下表所示,则

| 共价键 |  |  |  | 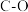 |  |
键能/( ) ) | 436 | 803 | 414 |  | 464 |
(4)
 和
和 是两种比较稳定的温室气体,科学家利用原电池装置,实现了两种分子的耦合转化,装置如图所示。
是两种比较稳定的温室气体,科学家利用原电池装置,实现了两种分子的耦合转化,装置如图所示。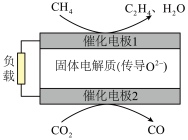
②催化电极1的电极反应式为
您最近一年使用:0次
2 . 请回答下列有关问题。
(1)Fe元素按周期表分区属于_______ 区元素,基态Fe原子的价电子排布式为_______ 。
(2)钠在火焰上灼烧产生的黄光是一种_______ 。 (填字母)
A.吸收光谱 B.发射光谱
(3)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是_______ 。
(4)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为_______ 。
(5)分析Cu、Zn的核外电子排布,推测Cu的第二电离能I2_______ Zn的第二电离能I2(填写“大于”、“小于”或“等于”)。
(6)资料显示:N元素电负性略大于Cl;NCl3可溶于水发生水解反应。试判断NCl3可能的水解方程式为_______ 。
(1)Fe元素按周期表分区属于
(2)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(3)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(4)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(5)分析Cu、Zn的核外电子排布,推测Cu的第二电离能I2
(6)资料显示:N元素电负性略大于Cl;NCl3可溶于水发生水解反应。试判断NCl3可能的水解方程式为
您最近一年使用:0次
3 . 一定压强下,向10L密闭容器中充入1molS2Cl2(g)和1molCl2,发生反应: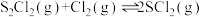 。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中正确的是
。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中正确的是
 。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中正确的是
。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中正确的是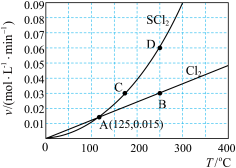
| A.A、B、C、D四点对应状态下,达到平衡状态的是A |
| B. 正反应的活化能大于逆反应的活化能 |
| C. 达到平衡后再加热,平衡向逆反应方向移动 |
| D.在300℃下,达平衡后缩小容器容积,重新达平衡后,Cl2的转化率增大 |
您最近一年使用:0次
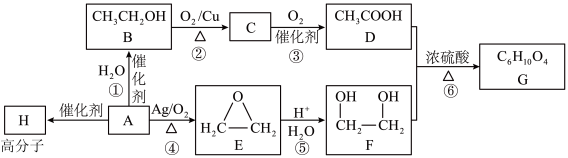
4 . 有机物A为煤的干馏产物之一,其产量可以用来衡量一个国家石油化工的发展水平,以A为原料合成香料G的流程如下:
(1)C的官能团名称为_______ ,常用于检验该官能团的一种试剂名称为_______ 。
(2)写出反应①的化学反应方程式_______ 。
(3)写出反应⑤的化学反应方程式_______ ,此反应的原子利用率为_______ 。
(4)1molF与足量的金属钠反应可产生_______ L气体(标准状况)。相对分子质量比A多14的物质的高聚物的结构简式_______ 。
(5)F经酸性 溶液氧化可转化为J
溶液氧化可转化为J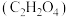 ,J与F可反应生成一种六元环状化合物,写出J与F反应的化学方程式
,J与F可反应生成一种六元环状化合物,写出J与F反应的化学方程式_______ 。
(1)C的官能团名称为
(2)写出反应①的化学反应方程式
(3)写出反应⑤的化学反应方程式
(4)1molF与足量的金属钠反应可产生
(5)F经酸性
 溶液氧化可转化为J
溶液氧化可转化为J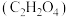 ,J与F可反应生成一种六元环状化合物,写出J与F反应的化学方程式
,J与F可反应生成一种六元环状化合物,写出J与F反应的化学方程式
您最近一年使用:0次
解题方法
5 . 实验室为探究铜与浓硫酸的反应,并验证 的性质,设计如图所示装置进行实验。
的性质,设计如图所示装置进行实验。
(1)装置A中的反应,浓硫酸体现了_______ 性和_______ 性。
(2)装置B中酸性 溶液逐渐褪色,证明
溶液逐渐褪色,证明 具有
具有_______ 性;装置C中发生反应的化学方程式_______ 。
(3)装置D的作用是_______ ;实验结束时需从导管a通入大量空气,其目的是_______ 。
(4)装置E中NaOH溶液足量,写出E中反应的离子方程式_______ 。
(5) 溶于水生成
溶于水生成 ,已知酸性
,已知酸性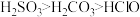 ,为了证明酸性
,为了证明酸性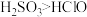 ,将
,将 通入到下列试剂,下列试剂排序正确的是_______(填选项)。
通入到下列试剂,下列试剂排序正确的是_______(填选项)。
①小苏打溶液;②品红溶液;③酸性 溶液;④漂白粉溶液
溶液;④漂白粉溶液
(6)实验室制取的乙烯中常混有少量 ,用下面装置证明混合气体中含有乙烯。其中Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液。
,用下面装置证明混合气体中含有乙烯。其中Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液。_______ (填字母)。
a.酸性 溶液 b.NaOH溶液 c.
溶液 b.NaOH溶液 c. 溶液
溶液
②证明含有乙烯的现象是_______ 。
 的性质,设计如图所示装置进行实验。
的性质,设计如图所示装置进行实验。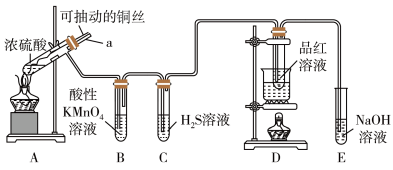
(1)装置A中的反应,浓硫酸体现了
(2)装置B中酸性
 溶液逐渐褪色,证明
溶液逐渐褪色,证明 具有
具有(3)装置D的作用是
(4)装置E中NaOH溶液足量,写出E中反应的离子方程式
(5)
 溶于水生成
溶于水生成 ,已知酸性
,已知酸性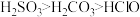 ,为了证明酸性
,为了证明酸性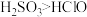 ,将
,将 通入到下列试剂,下列试剂排序正确的是_______(填选项)。
通入到下列试剂,下列试剂排序正确的是_______(填选项)。①小苏打溶液;②品红溶液;③酸性
 溶液;④漂白粉溶液
溶液;④漂白粉溶液| A.②①③④ | B.③②①④ | C.①③②④ | D.④③②① |
(6)实验室制取的乙烯中常混有少量
 ,用下面装置证明混合气体中含有乙烯。其中Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液。
,用下面装置证明混合气体中含有乙烯。其中Ⅱ中为品红溶液,Ⅲ中为溴的四氯化碳溶液。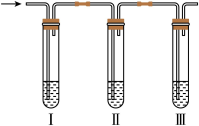
a.酸性
 溶液 b.NaOH溶液 c.
溶液 b.NaOH溶液 c. 溶液
溶液②证明含有乙烯的现象是
您最近一年使用:0次
解题方法
6 . 在一定温度下,将1molA和2molB放入容积为2L的某密闭容器中发生反应: 2min后达到平衡,测得容器内C的浓度为
2min后达到平衡,测得容器内C的浓度为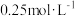 ,则下列叙述不正确的是
,则下列叙述不正确的是
 2min后达到平衡,测得容器内C的浓度为
2min后达到平衡,测得容器内C的浓度为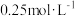 ,则下列叙述不正确的是
,则下列叙述不正确的是| A.在2min内该反应用D表示的反应速率为0.0625mol·L-1·min-1 |
| B.平衡时A的转化率为25% |
| C.平衡时B的体积分数约为50% |
D.初始时的压强与平衡时的压强之比为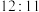 |
您最近一年使用:0次
7 . 下列说法正确的是
| A.硅的化学性质稳定,在自然界中主要以单质形式存在 |
| B.油脂属于有机高分子,可以为人体提供能量 |
| C.糖类、油脂、蛋白质均可水解 |
| D.葡萄糖溶液与新制的氢氧化铜混合加热,产生砖红色沉淀 |
您最近一年使用:0次
解题方法
8 . 为提纯下列物质(括号内为杂质),所用除杂试剂和分离方法都正确的是
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A |  | 酸性 溶液 溶液 | 洗气 |
| B |  (乙酸) (乙酸) |  溶液 溶液 | 分液 |
| C |  | 饱和 溶液 溶液 | 洗气 |
| D |  溶液 溶液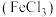 | NaOH溶液 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 设 为阿伏加德罗常数的值。下列说法中正确的是
为阿伏加德罗常数的值。下列说法中正确的是
 为阿伏加德罗常数的值。下列说法中正确的是
为阿伏加德罗常数的值。下列说法中正确的是A.0.4mol铁与足量的S反应,转移的电子数为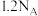 |
B.11.2L乙烷和丙烯的混合气体中含碳氢键数为 |
C.10g46%的乙醇溶液与足量的钠反应生成 数为 数为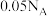 |
D.38g正丁烷和20g异丁烷的混合物中共价键数目为 |
您最近一年使用:0次
10 . 按要求回答下列问题
(1)已知: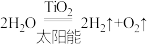 ,根据下表数据回答:
,根据下表数据回答:
①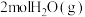 完全分解需
完全分解需_______ (填“放出”或“吸收”)能量_______ kJ。
②能正确表示该过程能量变化的示意图是_______ 。 和
和 发生反应,生成
发生反应,生成 和
和 ,
, 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。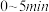 内,
内,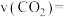
_______  。
。
②下列说明该反应一定达到化学平衡状态的是_______ 。
a.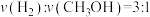
b.容器中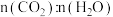 不再变化
不再变化
c.容器中气体压强不再变化
d.容器中气体密度不再变化
e.体系的温度保持不再变化
(3)氢氧燃料电池是短寿命载人航天器电源的一个合适的选择。下图是一种碱性氢氧燃料电池结构示意图。_______ (填“a”或“b”),该电极上发生的电极反应是_______ 。
②电池工作时产生的水会以水蒸气的形式被气体物质带出,在出口加装冷凝器可以将水回收,冷凝器应装在出口_______ (填“c”或“d”)处。
③电池工作时,电解质溶液会因稀释及吸收 而变质,此时电解质溶液的pH将
而变质,此时电解质溶液的pH将_______ (填“升高”或“降低”)。
(1)已知:
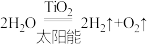 ,根据下表数据回答:
,根据下表数据回答:| 化学键 |  |  |  |
键能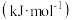 | 436 | 496 | 463 |
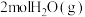 完全分解需
完全分解需②能正确表示该过程能量变化的示意图是
A.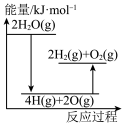 B.
B.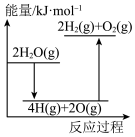
C.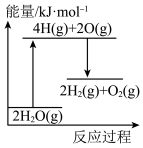 D.
D.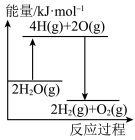
 和
和 发生反应,生成
发生反应,生成 和
和 ,
, 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。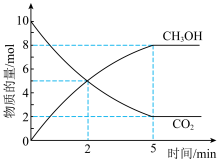
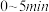 内,
内,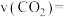
 。
。②下列说明该反应一定达到化学平衡状态的是
a.
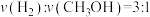
b.容器中
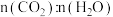 不再变化
不再变化c.容器中气体压强不再变化
d.容器中气体密度不再变化
e.体系的温度保持不再变化
(3)氢氧燃料电池是短寿命载人航天器电源的一个合适的选择。下图是一种碱性氢氧燃料电池结构示意图。
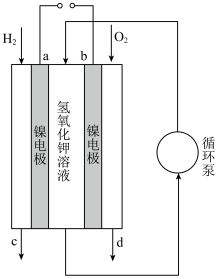
②电池工作时产生的水会以水蒸气的形式被气体物质带出,在出口加装冷凝器可以将水回收,冷凝器应装在出口
③电池工作时,电解质溶液会因稀释及吸收
 而变质,此时电解质溶液的pH将
而变质,此时电解质溶液的pH将
您最近一年使用:0次



