1 . 下列物质的用途利用了其还原性的是
| A.用金属铝进行铝热法炼铁 | B.用熟石灰中和土壤的酸性 |
| C.用NaHCO3治疗胃酸过多 | D.用水玻璃制备硅胶和木材防火剂 |
您最近一年使用:0次
2 . 下列关于乙烯用途、性质、结构叙述正确的是
①乙烯通入水中即可转化为乙醇
②乙烯可作香蕉等水果的催熟剂
③1mol乙烯与氯气完全加成,然后与氯气发生取代反应,一共需要氯气3mol
④乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤乙烯分子中所有原子在同一个平面
⑥乙烯容易与溴水发生反应,1mol乙烯加成消耗1mol溴单质,说明乙烯分子含有一个碳碳双键
①乙烯通入水中即可转化为乙醇
②乙烯可作香蕉等水果的催熟剂
③1mol乙烯与氯气完全加成,然后与氯气发生取代反应,一共需要氯气3mol
④乙烯能够被酸性KMnO4溶液所氧化,说明乙烯结构中含有一个碳碳双键
⑤乙烯分子中所有原子在同一个平面
⑥乙烯容易与溴水发生反应,1mol乙烯加成消耗1mol溴单质,说明乙烯分子含有一个碳碳双键
| A.①②④ | B.②⑤⑥ | C.②③⑤ | D.①④⑤ |
您最近一年使用:0次
2016-12-09更新
|
514次组卷
|
4卷引用:辽宁省锦州市黑山县第四高级中学2021-2022学年高二下学期3月月考化学试题
辽宁省锦州市黑山县第四高级中学2021-2022学年高二下学期3月月考化学试题辽宁省锦州市黑山县黑山中学2021-2022学年高二下学期4月月考化学试题2015-2016学年广西宾阳县宾阳中学高一5月月考化学试卷(已下线)第七章 有机化合物(培优提升卷)-2020-2021学年高一化学章末集训必刷卷(人教版2019必修第二册)
3 . 铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
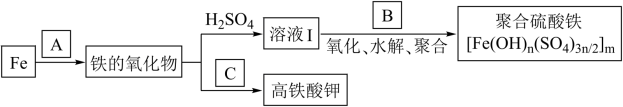
请回答下列问题:
(1)若A为H2O(g),写出反应方程式:_______________________________ ;
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+的离子方程式(还原产物为Cl-)___________________ ;
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾(K2FeO4)的化学方程式,并配平:
□Fe2O3+□KNO3+□KOH □
□_________ +□KNO2+□__________
(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1000mol・L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.
已知:
2Fe3++2I-═2Fe2++I2
I2+2S2O32-═2I-+S4O42-
①滴定选用的指示剂及滴定终点观察到的现象_______________________________ ;
②溶液Ⅰ中铁元素的总含量为____________ g・L-1.若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将_________ (填“偏高”“偏低”或“不变”)。

请回答下列问题:
(1)若A为H2O(g),写出反应方程式:
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+的离子方程式(还原产物为Cl-)
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾(K2FeO4)的化学方程式,并配平:
□Fe2O3+□KNO3+□KOH
 □
□(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1000mol・L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL.
已知:
2Fe3++2I-═2Fe2++I2
I2+2S2O32-═2I-+S4O42-
①滴定选用的指示剂及滴定终点观察到的现象
②溶液Ⅰ中铁元素的总含量为
您最近一年使用:0次
4 . 高铁酸钾(K2FeO4)是一种理想的绿色高效水处理剂。某学习小组用下图所示装置(夹持仪器已略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备K2FeO4。

查阅资料知K2FeO4的部分性质如下:①可溶于水、微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。
请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是_________________ 。
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是___________ 。
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式____________________________________________ ;该操作不能将KClO饱和溶液滴加到Fe(NO3)3饱和溶液中,其原因是________________________________________ 。
(4)制得的粗产品中含有Fe(OH)3、KCl等杂质。一种提纯方案为:将一定量的K2FeO4粗产品溶于冷的3 mol·L-1KOH溶液中,用砂芯漏斗过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥。
①第一次和第二次过滤得到的固体分别对应的是(填化学式)______________ 、___________ ,过滤时不用普通漏斗而采用砂芯漏斗的原因是_____________________ 。
②晶体用乙醇洗涤的原因是________________________ 。

查阅资料知K2FeO4的部分性质如下:①可溶于水、微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。
请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3。为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式
(4)制得的粗产品中含有Fe(OH)3、KCl等杂质。一种提纯方案为:将一定量的K2FeO4粗产品溶于冷的3 mol·L-1KOH溶液中,用砂芯漏斗过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥。
①第一次和第二次过滤得到的固体分别对应的是(填化学式)
②晶体用乙醇洗涤的原因是
您最近一年使用:0次
2016-12-09更新
|
349次组卷
|
4卷引用:辽宁省沈阳市城郊市重点联合体2020届高三上学期期中模拟考试(2)化学试题
名校
5 . 下列有关合金的说法错误的是
| A.青铜是我国使用最早的合金 | B.钢是用量最大、用途最广的合金 |
| C.合金的硬度一般高于各成分金属 | D.合金的熔点一般高于各成分金属 |
您最近一年使用:0次
2016-12-09更新
|
178次组卷
|
3卷引用:2016-2017学年辽宁省大连市高一上学期期末考试化学试卷
6 . 下列物质与其用途完全符合的有
①Na2CO3—制玻璃; ②SiO2—太阳能电池; ③Na2SiO3—木材防火剂; ④NH3—制冷剂;
⑤Al2O3—焊接钢轨; ⑥NaClO—消毒剂、漂白织物 ⑦Fe2O3—红色油漆或涂料
①Na2CO3—制玻璃; ②SiO2—太阳能电池; ③Na2SiO3—木材防火剂; ④NH3—制冷剂;
⑤Al2O3—焊接钢轨; ⑥NaClO—消毒剂、漂白织物 ⑦Fe2O3—红色油漆或涂料
| A.4个 | B.5个 | C.6个 | D.7个 |
您最近一年使用:0次
7 . Ⅰ甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:

①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图_____ 。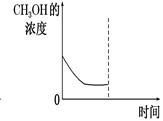
Ⅱ甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+ CO(g) CH3OH(g)
CH3OH(g)
(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)

①该反应的平衡常数表达式K=____ ,△H_____ 0(填“>”、“<”或“=”).
②按下列物质的量发生反应,CO的转化率由大到小的顺序是_____ (填甲乙丙).

(3)已知在常温常压下:化学反应①②③④的平衡常数分别为K1,K2,K3,K4
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) K1
②2CO(g)+O2(g)=2CO2(g)K2
③H2O(g)=H2O(l)K3
④CH3OH(l)+O2(g)=CO(g)+2H2O(l)K4
则K4=__________ (用含有K1,K2,K3的代数式表达)
(1)已知:2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
①平衡时,c(CH3OCH3)等于
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图

Ⅱ甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+ CO(g)
 CH3OH(g)
CH3OH(g)(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)

①该反应的平衡常数表达式K=
②按下列物质的量发生反应,CO的转化率由大到小的顺序是

(3)已知在常温常压下:化学反应①②③④的平衡常数分别为K1,K2,K3,K4
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) K1
②2CO(g)+O2(g)=2CO2(g)K2
③H2O(g)=H2O(l)K3
④CH3OH(l)+O2(g)=CO(g)+2H2O(l)K4
则K4=
您最近一年使用:0次
8 . 已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答下列问题:

(1)B、D、I的化学式是B______ D______ I______
(2)写出H的一种用途______
(3)写出A受热分解的化学方程式______
(4)若H与C反应固体增重4.2g,则参加反应的C气体在标准状况下的体积为______ L

(1)B、D、I的化学式是B
(2)写出H的一种用途
(3)写出A受热分解的化学方程式
(4)若H与C反应固体增重4.2g,则参加反应的C气体在标准状况下的体积为
您最近一年使用:0次
9 . 过氧化氢和臭氧都是常见的绿色氧化剂,工业生产中有着重要用途。
(1)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)===H2O(l)+ O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1
H2O(l)===H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式_________________________ 。
(2)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+O3(g) NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是
NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是________________ 。
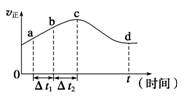
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.该反应为放热反应
d.Δt1=Δt2时,NO的转化量:a~b段小于b~c段
(1)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂。
已知:N2H4(l)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1
H2O2(l)===H2O(l)+
 O2(g),ΔH=-98 kJ·mol-1
O2(g),ΔH=-98 kJ·mol-1H2O(l)===H2O(g),ΔH=+44 kJ·mol-1
试写出N2H4和液态H2O2反应生成气态水的热化学方程式
(2)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+O3(g)
 NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是
NO2(g)+O2(g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图如图所示。由图可得出的正确说法是
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.该反应为放热反应
d.Δt1=Δt2时,NO的转化量:a~b段小于b~c段
您最近一年使用:0次
10 . 钠及其化合物是中学化学常见物质
(1)含氯化钠0.9%的水称为生理盐水,因为它与血浆有相同的渗透压,若将生理盐水的密度视为1g/cm3,则生理盐水的物质的量浓度为_______________ (保留两位有效数字)
缺钾患者补钾,可以在食用盐中加入一定比例的钾盐,怎样判断食用的食盐中是否添加了钾盐___________________________________
(2)工业纯碱常混有小苏打,现有二者的混合固体7.0g,加热至质量不变为止,固体变为6.38g,则该工业纯碱的纯度为____________ ,纯碱在工业上有重要的用途,如制玻璃,制玻璃的原料除纯碱外,还需_____________________
(3)在120℃时,将12.4 g CO2和H2O(g)的混合气体缓缓通入过量的过氧化钠固体中,充分反应后,固体的质量增加6g。
①产生氧气在标准状况下的体积是_________ ;
②原混合气体中CO2的质量是_________ ;
(1)含氯化钠0.9%的水称为生理盐水,因为它与血浆有相同的渗透压,若将生理盐水的密度视为1g/cm3,则生理盐水的物质的量浓度为
缺钾患者补钾,可以在食用盐中加入一定比例的钾盐,怎样判断食用的食盐中是否添加了钾盐
(2)工业纯碱常混有小苏打,现有二者的混合固体7.0g,加热至质量不变为止,固体变为6.38g,则该工业纯碱的纯度为
(3)在120℃时,将12.4 g CO2和H2O(g)的混合气体缓缓通入过量的过氧化钠固体中,充分反应后,固体的质量增加6g。
①产生氧气在标准状况下的体积是
②原混合气体中CO2的质量是
您最近一年使用:0次



