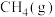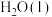名校
解题方法
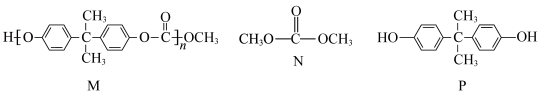
1 . 某高分子化合物M常用于制作眼镜镜片,可由N和P两种物质合成,M、N、P的结构如图所示,下列说法正确的是
| A.N与P合成M的反应为加聚反应 | B.M的链节中在同一平面的碳原子最多有14个 |
| C.P在空气中很稳定,可以保存在广口瓶中 | D.常温下,M、N、P均易溶于水 |
您最近一年使用:0次
今日更新
|
296次组卷
|
4卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
2 . 下列化学用语表示正确的是
|
|
| A.醛基的电子式为 | B.异戊烷的球棍模型 |
|
|
| C.苯的分子结构模型 | D.反-2-戊烯的结构式 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 对氨基苯甲酸可用甲苯为原料合成。已知①苯环上的硝基可被还原为氨基:
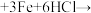

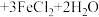 ,产物苯胺还原性强,易被氧化;②−CH3为邻、对位取代定位基,而−COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是
,产物苯胺还原性强,易被氧化;②−CH3为邻、对位取代定位基,而−COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是
A.甲苯 X X Y Y 对氨基苯甲酸 对氨基苯甲酸 |
B.甲苯 X X Y Y 对氨基苯甲酸 对氨基苯甲酸 |
C.甲苯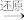 X X Y Y 对氨基苯甲酸 对氨基苯甲酸 |
D.甲苯 X X Y Y 对氨基苯甲酸 对氨基苯甲酸 |
您最近一年使用:0次
4 . 实验是高中化学的重要组成部分,下列说法正确的是

| A.用乙醇萃取碘水中的碘时需要使用a、f |
| B.重结晶法提纯苯甲酸时需要使用b、f |
| C.分离二氯甲烷、三氯甲烷和四氯化碳时需要使用c、d、e、f |
| D.分离乙酸乙酯和饱和食盐水时需要使用c、d、f |
您最近一年使用:0次
名校
5 . 化学与生活密切相关,下列说法错误的是
| A.可作为麻醉剂的新戊烷在常温下为气态 |
| B.汽油的主要成分之一辛烷与甲烷互为同系物 |
| C.用于制备导电高分子材料的聚乙炔能使溴水褪色 |
| D.常用于合成塑料和橡胶的苯乙烯中含有两种官能团 |
您最近一年使用:0次
名校
6 . 已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法错误 的是
 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法| A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器 |
B.乙组实验中 将 将 氧化为 氧化为 |
C.丙组实验发生反应的离子方程式: |
D.丁组实验说明还原性: |
您最近一年使用:0次
7日内更新
|
219次组卷
|
5卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
7 . 下列对物质性质的解释错误的是
选项 | 物质性质 | 解释 |
A | 吡咯( | 吡咯中,氮原子的孤对电子参与形成了离域键,使得氮原子上的电子云密度降低 |
B | HF气体的摩尔质量测定值大于实际值 | HF形成了分子间氢键 |
C | 乙酸的酸性大于丙酸 | 烃基越长,推电子效应越大 |
D | 18-冠-6识别钾离子,体现了超分子“分子识别”的特征 | 18-冠-6中,氧原子电负性大,带负电荷,通过离子键与钾离子作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
223次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
名校
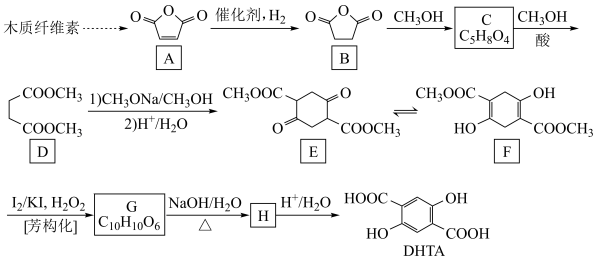
8 . 2,5—二羟基对苯二甲酸(DHTA)是一种重要的化工原料,广泛用于合成高性能有机颜料及光敏聚合物;作为钠离子电池的正、负电极材料也表现出优异的性能。利用生物质资源合成DHTA的路线如下:
(1)A→B的反应类型为___________ 。
(2)C的结构简式为___________ 。
(3)D的化学名称为___________ 。
(4)G→H的化学方程式为___________ 。
(5)写出一种能同时满足下列条件的G的同分异构体的结构简式___________ 。
(a)核磁共振氢谱有两组峰,且峰面积比为3:2;
(b)红外光谱中存在 吸收峰,但没有
吸收峰,但没有 吸收峰;
吸收峰;
(c)可与NaOH水溶液反应,反应液酸化后可与 溶液发生显色反应。
溶液发生显色反应。
(6)阿伏苯宗(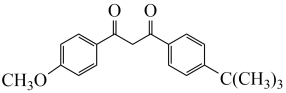 )是防晒霜的添加剂之一、以碘甲烷(
)是防晒霜的添加剂之一、以碘甲烷( )、对羟基苯乙酮(
)、对羟基苯乙酮(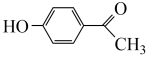 )和对叔丁基甲苯(
)和对叔丁基甲苯(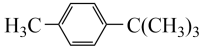 )为原料,合成阿伏苯宗的路线如下。
)为原料,合成阿伏苯宗的路线如下。___________ ;N___________ ;Q___________ 。
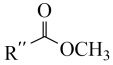
已知: +
+

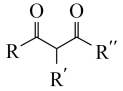
(1)A→B的反应类型为
(2)C的结构简式为
(3)D的化学名称为
(4)G→H的化学方程式为
(5)写出一种能同时满足下列条件的G的同分异构体的结构简式
(a)核磁共振氢谱有两组峰,且峰面积比为3:2;
(b)红外光谱中存在
 吸收峰,但没有
吸收峰,但没有 吸收峰;
吸收峰;(c)可与NaOH水溶液反应,反应液酸化后可与
 溶液发生显色反应。
溶液发生显色反应。(6)阿伏苯宗(
 )是防晒霜的添加剂之一、以碘甲烷(
)是防晒霜的添加剂之一、以碘甲烷( )、对羟基苯乙酮(
)、对羟基苯乙酮( )和对叔丁基甲苯(
)和对叔丁基甲苯( )为原料,合成阿伏苯宗的路线如下。
)为原料,合成阿伏苯宗的路线如下。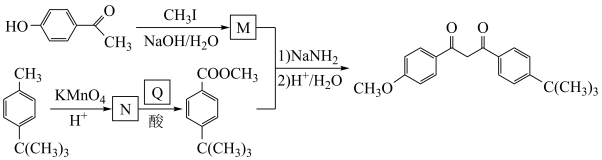
您最近一年使用:0次
2024-06-02更新
|
183次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
名校
9 .  还原CO2是实现“双碱”经济的有效途径之一,涉及反应如下:
还原CO2是实现“双碱”经济的有效途径之一,涉及反应如下:
Ⅰ:

Ⅱ:

回答下列问题:
(1)物质的标准生成焓是指在标态和某温度下,由元素最稳定的单质生成1mol纯净物时的焓变。一些物质298K时的标准生成焓(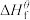 )
)


______ 
(2)有利于提高CO平衡产率的条件是______(填标号)。
(3)反应Ⅰ的正、逆反应速率方程为: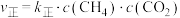 、
、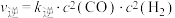 ,
, 、
、 符合阿伦尼乌斯公式
符合阿伦尼乌斯公式 (
( 为活化能:T为温度:R、c为常数),实验测得
为活化能:T为温度:R、c为常数),实验测得 的实验数据如图所示,则正反应的活化能
的实验数据如图所示,则正反应的活化能
______  ,升高温度
,升高温度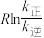 的值
的值______ (填“增大”“减小”或“不变”)。 而产生积碳,从而导致催化剂活性降低。若向容器中通入过量水蒸气可以清除积碳.反应的化学方程式为
而产生积碳,从而导致催化剂活性降低。若向容器中通入过量水蒸气可以清除积碳.反应的化学方程式为______ ,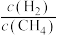 的值
的值______ (填“增大”“减小”或“不变”)。
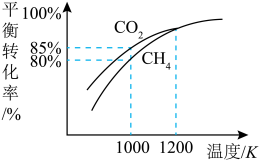
(5)在101kPa时,工业上按投料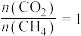 加入刚性密闭容器中,只发生Ⅰ、Ⅱ两个反应,
加入刚性密闭容器中,只发生Ⅰ、Ⅱ两个反应, 和
和 的平衡转化率与温度的关系如图所示.温度高于1200 K时,
的平衡转化率与温度的关系如图所示.温度高于1200 K时, 和
和 的平衡转化率趋于相等的原因可能是
的平衡转化率趋于相等的原因可能是______ ;计算1000 K时反应Ⅱ的压强平衡常数
______ (计算结果保留3位有效数字,用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
 还原CO2是实现“双碱”经济的有效途径之一,涉及反应如下:
还原CO2是实现“双碱”经济的有效途径之一,涉及反应如下:Ⅰ:


Ⅱ:


回答下列问题:
(1)物质的标准生成焓是指在标态和某温度下,由元素最稳定的单质生成1mol纯净物时的焓变。一些物质298K时的标准生成焓(
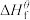 )
)


物质 |
|
|
|
|
|
| -74.8 | -110 | -393.5 | -286 | 0 |
(2)有利于提高CO平衡产率的条件是______(填标号)。
| A.低温低压 | B.低温高压 | C.高温低压 | D.高温高压 |
(3)反应Ⅰ的正、逆反应速率方程为:
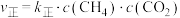 、
、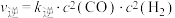 ,
, 、
、 符合阿伦尼乌斯公式
符合阿伦尼乌斯公式 (
( 为活化能:T为温度:R、c为常数),实验测得
为活化能:T为温度:R、c为常数),实验测得 的实验数据如图所示,则正反应的活化能
的实验数据如图所示,则正反应的活化能
 ,升高温度
,升高温度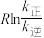 的值
的值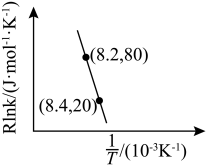
 而产生积碳,从而导致催化剂活性降低。若向容器中通入过量水蒸气可以清除积碳.反应的化学方程式为
而产生积碳,从而导致催化剂活性降低。若向容器中通入过量水蒸气可以清除积碳.反应的化学方程式为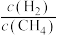 的值
的值(5)在101kPa时,工业上按投料
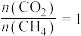 加入刚性密闭容器中,只发生Ⅰ、Ⅱ两个反应,
加入刚性密闭容器中,只发生Ⅰ、Ⅱ两个反应, 和
和 的平衡转化率与温度的关系如图所示.温度高于1200 K时,
的平衡转化率与温度的关系如图所示.温度高于1200 K时, 和
和 的平衡转化率趋于相等的原因可能是
的平衡转化率趋于相等的原因可能是
您最近一年使用:0次
2024-06-02更新
|
220次组卷
|
3卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题
名校
10 . 丙烯是重要的有机化工原料。一定条件下,丙烷直接脱氢制备丙烯过程中的转化率和丙烯的选择性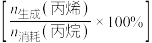 随时间变化的关系如图所示。下列说法错误的是
随时间变化的关系如图所示。下列说法错误的是
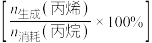 随时间变化的关系如图所示。下列说法错误的是
随时间变化的关系如图所示。下列说法错误的是
| A.该反应为氧化反应 |
| B.催化剂可以降低反应的活化能,不改变反应的焓变 |
| C.丙烯的产率小于10% |
| D.恒温恒容条件下,增大c(丙烷),平衡正向移动,丙烷的转化率增大 |
您最近一年使用:0次
2024-06-02更新
|
92次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题





 )和吡啶(
)和吡啶( )均为平面分子,吡啶碱性较强
)均为平面分子,吡啶碱性较强