解题方法
1 . 锶(Sr)和镁位于同主族,锶比镁更活泼,锶与氮气在加热条件下反应生成氮化锶(Sr3N2),已知氮化锶遇水剧烈反应。某同学设计如下装置制备氮化锶(Sr3N2相对分子质量:290.8)。
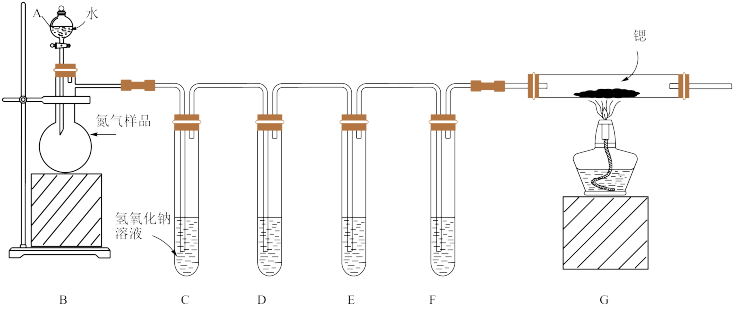
已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜(CH3COO[Cu(NH3)2])溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
试回答下列问题:
(1)仪器A的名称是___________
(2)打开分液漏斗的旋塞,装置B能持续提供N2,这是利用了N2___________ 的物理性质
(3)装置C中盛放NaOH溶液的作用为___________
(4)装置D、E、F中盛装的试剂分别是___________ (填代号)
①浓硫酸②连苯三酚碱性溶液③醋酸二氨合亚铜溶液
(5)为了制得纯净的氮气,实验室中可选用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:___________
(6)上述实验设计存在明显的缺陷,可能会导致产品变质,提出改进方案为:___________
(7)产品纯度的测定:称取0.8000g实验所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用20.00mL1.00mol/L的盐酸标准溶液完全吸收,再用1.00mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00mLNaOH溶液。则产品纯度为___________ %。

已知:①所使用的氮气样品可能含有少量CO、CO2、O2等气体杂质。
②醋酸二氨合亚铜(CH3COO[Cu(NH3)2])溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
试回答下列问题:
(1)仪器A的名称是
(2)打开分液漏斗的旋塞,装置B能持续提供N2,这是利用了N2
(3)装置C中盛放NaOH溶液的作用为
(4)装置D、E、F中盛装的试剂分别是
①浓硫酸②连苯三酚碱性溶液③醋酸二氨合亚铜溶液
(5)为了制得纯净的氮气,实验室中可选用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气,其化学方程式为:
(6)上述实验设计存在明显的缺陷,可能会导致产品变质,提出改进方案为:
(7)产品纯度的测定:称取0.8000g实验所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用20.00mL1.00mol/L的盐酸标准溶液完全吸收,再用1.00mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗16.00mLNaOH溶液。则产品纯度为
您最近一年使用:0次
2 . 某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧.他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
【提出假设】假设1:白色物质是Na2O
假设2:白色物质是Na2CO3.
假设3:白色物质是Na2O和Na2CO3。该小组对燃烧后的白色产物进行如下探究:
方案1:取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液溶液变成红色,则白色物质为Na2O
方案2:①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液出现白色沉淀②静置片刻,取上层清液于试管中,滴加无色酚酞试液无明显现象
(1)甲同学认为方案1得到的结论不正确,其理由是___________________________________ .
(2)乙同学认为方案2得到的结论正确,白色物质为__________________ .
(3)通过方案1和方案2的实验,你认为上述三个假设中,______ 成立.你的理由是_______________ .
(4)写出钠在二氧化碳中燃烧的化学方程式并用双线桥法表示电子转移为_________________________ .
(5)丙同学认为白色物质有可能是氢氧化钠.你是否同意丙同学的观点,并简述理由:______ .
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.
【提出假设】假设1:白色物质是Na2O
假设2:白色物质是Na2CO3.
假设3:白色物质是Na2O和Na2CO3。该小组对燃烧后的白色产物进行如下探究:
方案1:取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液溶液变成红色,则白色物质为Na2O
方案2:①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液出现白色沉淀②静置片刻,取上层清液于试管中,滴加无色酚酞试液无明显现象
(1)甲同学认为方案1得到的结论不正确,其理由是
(2)乙同学认为方案2得到的结论正确,白色物质为
(3)通过方案1和方案2的实验,你认为上述三个假设中,
(4)写出钠在二氧化碳中燃烧的化学方程式并用双线桥法表示电子转移为
(5)丙同学认为白色物质有可能是氢氧化钠.你是否同意丙同学的观点,并简述理由:
您最近一年使用:0次
2020-11-16更新
|
334次组卷
|
3卷引用:安徽省黄山市屯溪第一中学2020-2021学年高一上学期期中考试化学试题
安徽省黄山市屯溪第一中学2020-2021学年高一上学期期中考试化学试题江苏省天一中学2021-2022学年高一上学期期中考试化学(强化班)试题(已下线)2.1.1 活泼的金属单质——钠-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
3 . (1)分别取等质量的甲烷和A(饱和一元醇)、B(饱和一元醛)、C(稠环芳香烃含氧衍生物),若它们完全燃烧,生成等物质的量的CO2,则:
①A的分子式为_______________ ;B的分子式为_______________ ;C的分子式为_____________ (C写出分子量最小的一种)。
②写出符合上述要求时,CH4和A、B、C的分子组成必须满足的条件是_______________ (以n表示碳原子数,m表示氧原子数,只写通式)。
(2)已知:在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸,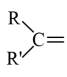 基被氧化成酮。回答下列问题:
基被氧化成酮。回答下列问题:
①1mol某烯与酸性高锰酸钾反应后生成2mol丁酮,则该烯的结构简式为是____ 。
②1mol某烯与酸性高锰酸钾反应后只生成1mol HOOC-CH(CH3)-CH2-CH2-CH(CH3)-COCH3,则该烯的结构简式为___ (键线式表示)。
(3)某有机化合物,经测定其蒸汽是相同条件下氢气密度的30倍。取该有机物样品0.90 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重0.54 g和1.32 g.则该有机物的分子式为______ 。
(4)写出一氯代物只有两种的苯的同系物的结构简式并用系统命名法命名(写出两种)。
①结构简式:__________ ,名称:___________ 。
②结构简式:____________ ,名称:___________ 。
①A的分子式为
②写出符合上述要求时,CH4和A、B、C的分子组成必须满足的条件是
(2)已知:在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸,
 基被氧化成酮。回答下列问题:
基被氧化成酮。回答下列问题:①1mol某烯与酸性高锰酸钾反应后生成2mol丁酮,则该烯的结构简式为是
②1mol某烯与酸性高锰酸钾反应后只生成1mol HOOC-CH(CH3)-CH2-CH2-CH(CH3)-COCH3,则该烯的结构简式为
(3)某有机化合物,经测定其蒸汽是相同条件下氢气密度的30倍。取该有机物样品0.90 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重0.54 g和1.32 g.则该有机物的分子式为
(4)写出一氯代物只有两种的苯的同系物的结构简式并用系统命名法命名(写出两种)。
①结构简式:
②结构简式:
您最近一年使用:0次
2019-04-29更新
|
105次组卷
|
2卷引用:【全国百强校】安徽省黄山市屯溪第一中学2018-2019学年高二(理)下学期期中考试化学试题
名校
4 . 某学习小组的同学对氯气与铁的反应及产物进行了如下探究:

(1)装置的连接顺序为a→___ →______→_____→_____→b→c→f。
(2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是________________ 。
(3)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
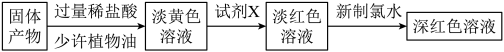
试剂X中溶质的化学式为____________ ;固体产物的成分可能为_____ (填字母)。
A.Fe和FeCl3 B.FeCl2和FeCl3 C.Fe、FeCl2和FeCl3 D.Fe和FeCl2
(4)加入少许植物油的作用是____________ ,加入新制氯水后溶液红色加深的原因:___________ (用离子方程式表示)。
(5)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为______ 。(计算结果保留两位有效数字)

(1)装置的连接顺序为a→
(2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是
(3)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

试剂X中溶质的化学式为
A.Fe和FeCl3 B.FeCl2和FeCl3 C.Fe、FeCl2和FeCl3 D.Fe和FeCl2
(4)加入少许植物油的作用是
(5)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为
您最近一年使用:0次
2019-02-02更新
|
778次组卷
|
10卷引用:【市级联考】安徽省黄山市2018-2019学年高一上学期期末考试化学试题
【市级联考】安徽省黄山市2018-2019学年高一上学期期末考试化学试题云南省盈江县第一高级中学2019-2020学年高一上学期期末考试化学试题云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高一上学期期末考试化学试题云南省昆明市寻甸县第五中学2019-2020学年高一上学期期末考试化学试题(已下线)河北省保定一中2018-2019学年高一上学期期末测试化学试题(已下线)第三章单元检测(测)--2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)安徽省滁州市定远县民族中学2020-2021学年高一11月月考化学试题(已下线)专题10 化学实验基础——备战2021年高考化学纠错笔记云南省瑞丽市第一民族中学2021-2022学年高一下学期3月份考试化学试题实验活动2 铁及其化合物的性质



