1 . 氮化锶(Sr3N2)是工业上生产荧光粉的原材料。已知:氮化锶遇水剧烈反应产生氨气。某同学设计如下装置制备氮化锶(Sr3N2相对分子质量:290.8)。
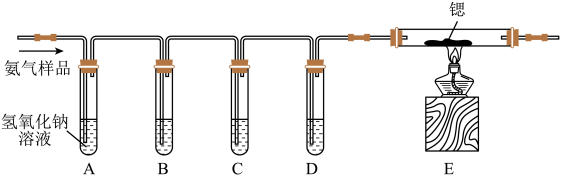
已知:①所使用的氮气样品可能含有少量 CO、CO2、O2等气体杂质;
②醋酸二氨合亚铜 CH3COO[Cu(NH3)2]溶液能定量吸收 CO,但易被O2化,失去吸收CO 能力,连苯三酚碱性溶液能定量吸收O2。
(1)装置 B盛装的试剂是___________ 。
(2)氮化锶遇水剧烈反应的化学方程式为___________ 。
(3)装置设计存在缺陷,可能会导致产品变质,提出改进措施为:___________ 。
(4)产品纯度的测定:称取 0.4000 g 所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用 50.00 mL 0.100 mol·L-1的盐酸标准溶液完全吸收,再用0.100 mol·L-1 NaOH 标准溶液滴定过剩的 HCl,到终点时消耗 30.00 mL NaOH 溶液。
①若用酚酞作指示剂,滴定终点的现象是___________ ;
②则产品纯度为___________ (计算结果保留 3 位有效数字);
③若氨没有完全蒸出,则会导致产品纯度___________ (填“偏大”“偏小”或“不影响”)

已知:①所使用的氮气样品可能含有少量 CO、CO2、O2等气体杂质;
②醋酸二氨合亚铜 CH3COO[Cu(NH3)2]溶液能定量吸收 CO,但易被O2化,失去吸收CO 能力,连苯三酚碱性溶液能定量吸收O2。
(1)装置 B盛装的试剂是
(2)氮化锶遇水剧烈反应的化学方程式为
(3)装置设计存在缺陷,可能会导致产品变质,提出改进措施为:
(4)产品纯度的测定:称取 0.4000 g 所得产品,加入干燥的三颈瓶中,加入蒸馏水,并通入足量水蒸气,将产生的氨全部蒸出,用 50.00 mL 0.100 mol·L-1的盐酸标准溶液完全吸收,再用0.100 mol·L-1 NaOH 标准溶液滴定过剩的 HCl,到终点时消耗 30.00 mL NaOH 溶液。
①若用酚酞作指示剂,滴定终点的现象是
②则产品纯度为
③若氨没有完全蒸出,则会导致产品纯度
您最近一年使用:0次
名校
解题方法
2 . 铁的化合物在生活、生产中用途十分广泛。回答下列问题:
(1)高铁酸钠( )是一种新型绿色消毒剂,能以
)是一种新型绿色消毒剂,能以 溶液为原料,经氧化制得,步骤如下:
溶液为原料,经氧化制得,步骤如下:
i.向 溶液中加入稀硫酸酸化;
溶液中加入稀硫酸酸化;
ii.在30℃左右加入H2O2溶液搅拌;
iii.再依次向其中加入NaOH溶液、NaClO溶液;
iv.经分离可得 。
。
已知:H2O2溶液可将 氧化为
氧化为 。
。
① 中铁元素的化合价为
中铁元素的化合价为___________ ,其在处理水时既能起到杀菌消毒作用,又能起到净水作用的原因是___________ 。
②加入H2O2溶液时发生反应的离子方程式为___________ ,该步反应不能在较高温度下进行的原因是___________ 。
③加入NaOH溶液后,再加入NaClO溶液时发生反应的化学方程式为___________ ,用单线桥标出电子转移的方向和数目:___________ 。
(2)无水 (易与H2O反应而变质、易升华)是常用的芳香烃取代反应催化剂。铁粉与氯气反应制备无水
(易与H2O反应而变质、易升华)是常用的芳香烃取代反应催化剂。铁粉与氯气反应制备无水 的实验装置如图所示(E用来收集产物):
的实验装置如图所示(E用来收集产物):

①在E处收集产物是利用了
___________ 的性质。
②实验过程中若D、E之间出现堵塞,可通过___________ (填简单操作),使实验能继续进行。
③某同学用5.60g干燥铁粉制得无水 13.00g,该次实验的产率(
13.00g,该次实验的产率( )是
)是___________ 。
④无水 的作用是
的作用是___________ 。
(1)高铁酸钠(
 )是一种新型绿色消毒剂,能以
)是一种新型绿色消毒剂,能以 溶液为原料,经氧化制得,步骤如下:
溶液为原料,经氧化制得,步骤如下:i.向
 溶液中加入稀硫酸酸化;
溶液中加入稀硫酸酸化;ii.在30℃左右加入H2O2溶液搅拌;
iii.再依次向其中加入NaOH溶液、NaClO溶液;
iv.经分离可得
 。
。已知:H2O2溶液可将
 氧化为
氧化为 。
。①
 中铁元素的化合价为
中铁元素的化合价为②加入H2O2溶液时发生反应的离子方程式为
③加入NaOH溶液后,再加入NaClO溶液时发生反应的化学方程式为
(2)无水
 (易与H2O反应而变质、易升华)是常用的芳香烃取代反应催化剂。铁粉与氯气反应制备无水
(易与H2O反应而变质、易升华)是常用的芳香烃取代反应催化剂。铁粉与氯气反应制备无水 的实验装置如图所示(E用来收集产物):
的实验装置如图所示(E用来收集产物):
①在E处收集产物是利用了

②实验过程中若D、E之间出现堵塞,可通过
③某同学用5.60g干燥铁粉制得无水
 13.00g,该次实验的产率(
13.00g,该次实验的产率( )是
)是④无水
 的作用是
的作用是
您最近一年使用:0次
名校
3 . (1)铁及其化合物在生活、生产中有广泛的应用。请回答下列问题:
①黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为_____ ,若有3mol FeS2参加反应,转移__________ mol电子。
②FeCl3与氢碘酸反应时可生成棕色物质I2,该反应的离子方程式为_________________ 。
(2)已知:S2O32-具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2,I2+2S2O32-→2I-+S4O62-则S2O82-、S4O62-、I2氧化性强弱顺序:_________ .
(3) 已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。

①写出a点处还原产物是_______________ ;b点到c点反应的离子方程式_________________________ 。
②当溶液中的I-为0.5 mol时,加入的KIO3为___________ mol。
①黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为
②FeCl3与氢碘酸反应时可生成棕色物质I2,该反应的离子方程式为
(2)已知:S2O32-具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2,I2+2S2O32-→2I-+S4O62-则S2O82-、S4O62-、I2氧化性强弱顺序:
(3) 已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。

①写出a点处还原产物是
②当溶液中的I-为0.5 mol时,加入的KIO3为
您最近一年使用:0次



