名校
1 .  是锂离子电池中广泛应用的电解质。某工厂用LiF、
是锂离子电池中广泛应用的电解质。某工厂用LiF、 为原料,低温反应制备
为原料,低温反应制备 ,其流程如下:
,其流程如下:
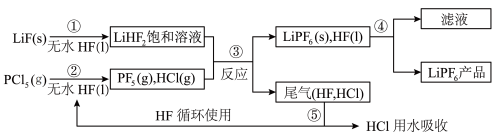
已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是做反应物和___________ 。反应设备不能用玻璃材质的原因是___________ (用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的___________ 溶液冲洗。
(2)该流程需在无水条件下进行,第②步反应中 极易水解,其产物为两种酸,写出
极易水解,其产物为两种酸,写出 水解的化学方程式:
水解的化学方程式:___________ 。
(3)第④步分离采用的方法是___________ ;第⑤步分离尾气中HF、HCl采用的方法是___________ 。
(4) 产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中
产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中 的物质的量为
的物质的量为___________ mol(用含有w、n的代数式表示)。
 是锂离子电池中广泛应用的电解质。某工厂用LiF、
是锂离子电池中广泛应用的电解质。某工厂用LiF、 为原料,低温反应制备
为原料,低温反应制备 ,其流程如下:
,其流程如下:
已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是做反应物和
(2)该流程需在无水条件下进行,第②步反应中
 极易水解,其产物为两种酸,写出
极易水解,其产物为两种酸,写出 水解的化学方程式:
水解的化学方程式:(3)第④步分离采用的方法是
(4)
 产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中
产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中 的物质的量为
的物质的量为
您最近一年使用:0次
2 . 锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231 ℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用:__________________ 及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、________________________ 。
③步骤Ⅲ生成SnO的离子方程式:__________________________ 。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是:______________________ ,证明已洗净。
⑤步骤Ⅴ操作依次为____________ 、____________ 、过滤、洗涤、低温干燥。
(2)某化学兴趣小组对用于微电子器件生产的锡粉进行了纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
①写出步骤②加入Fe2(SO4)3发生反应的离子方程式:____________________ ;
②此锡粉样品中锡的质量分数为:__________________ 。
(1)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用:
②步骤Ⅱ用到的玻璃仪器有烧杯、
③步骤Ⅲ生成SnO的离子方程式:
④步骤Ⅳ中检验SnO是否洗涤干净的操作是:
⑤步骤Ⅴ操作依次为
(2)某化学兴趣小组对用于微电子器件生产的锡粉进行了纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1 000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。
①写出步骤②加入Fe2(SO4)3发生反应的离子方程式:
②此锡粉样品中锡的质量分数为:
您最近一年使用:0次



