解题方法
1 . 下列实验操作、实验现象和实验结论均正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 常温下,向含溶解足量NH3的饱和食盐水中通入过量CO2 | 析出白色固体 | 溶解性:NaHCO3<NH4Cl |
B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液不变红 | Fe(NO3)2样品没有变质 |
C | 室温下,用pH试纸分别测定等物质的量浓度的 NaClO溶液和CH3COONa溶液的pH | NaClO溶液对应的pH试纸蓝色更深 | 酸性:HClO< CH3COOH |
D | 向2mL0.1mol·L–1AgNO3溶液中滴加1~2滴NaCl溶液,再滴加2滴Na2S溶液 | 开始有白色沉淀生成,后有黑色沉淀生成 | Ksp(Ag2S)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 某校实验室过氧化钠因保存不当变质,课外活动小组称取a g样品,设计用如图装置来测定过氧化钠质量分数。
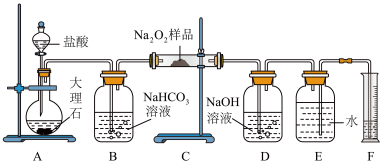
(1)将仪器连接好后,进行的第一步操作是_________ 。
(2)B装置出来的气体是否需要干燥_____________ (填“是”或“否”)。
(3)写出装置C中发生的主要反应化学方程式__________ 。
(4)D中NaOH溶液的作用________ 。
(5)实验结束时,读取实验中生成气体的体积时,不合理的是__________ 。
a.直接读取气体体积,不需冷却到室温。
b.上下移动量筒,使得E、F中液面高度相同。
c.视线与凹液面的最低点相平读取量筒中水的体积。
(6)读出量筒内水的体积后,折算成标准状况下氧气的体积为V L,则样品中过氧化钠的质量分数为_____________ 。(用含a和V的代数式表示)
(7)实验完成后E到F之间导管内残留水的体积会使测量结果________ (填“偏大”“偏小”“不影响”)。

(1)将仪器连接好后,进行的第一步操作是
(2)B装置出来的气体是否需要干燥
(3)写出装置C中发生的主要反应化学方程式
(4)D中NaOH溶液的作用
(5)实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温。
b.上下移动量筒,使得E、F中液面高度相同。
c.视线与凹液面的最低点相平读取量筒中水的体积。
(6)读出量筒内水的体积后,折算成标准状况下氧气的体积为V L,则样品中过氧化钠的质量分数为
(7)实验完成后E到F之间导管内残留水的体积会使测量结果
您最近一年使用:0次



