名校
解题方法
1 . 下列实验操作或实验方案,能达到目的的是
| 选项 | 实验操作或实验方案 | 目的 |
| A | 分别向相同体积的稀、浓硝酸插入大小一样的铜丝,比反应快慢 | 比较稀硝酸和浓硝酸的氧化性强弱 |
| B | 铜和浓硫酸反应的试管中溶液变黑,往该试管中加蒸馏水、震荡,溶液显蓝色 | 验证Cu被氧化为Cu2+ |
| C | 往粗盐溶液中依次加入过量的Na2CO3、BaCl2、NaOH,过滤后加适量盐酸,蒸发结晶 | 依次除去粗盐中的杂质:Ca2+、SO 和Mg2+,并得到较纯净的NaCl晶体 和Mg2+,并得到较纯净的NaCl晶体 |
| D | 把反应后的气体依次通入品红溶液和澄清石灰水,品红溶液褪色,澄清石灰水出现混浊 | 检验碳和浓硫酸反应产生的气体有SO2和CO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 如图为元素周期表的一部分,请参照a~h在表中的位置,回答下列问题:
(1)g在周期表中的位置是___________ 。
(2)元素d、g、h形成的简单离子中,离子半径最大的是___________ 。(填离子符号)
(3)元素c和元素f形成的化合物的化学式为___________ ,化学键为___________ 。
(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。已知Te与S元素同主族。
①碲及其化合物可能具有的性质为___________ (填标号)。
A.单质Te在常温下是固体
B.H2Te比H2O稳定
C.H2TeO4的酸性比H2SO4的弱
D.Cl2通入H2Te溶液中不发生反应
E.Te元素位于周期表中第六周期
②TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。写出TeO2与过量NaOH溶液反应的离子方程式___________ 。
③工业上,把SO2通入TeCl4溶液中,可得到Te,该反应的化学方程式是___________ 。
| a | |||||||||
| b | c | d | |||||||
| e | f | g | h |
(2)元素d、g、h形成的简单离子中,离子半径最大的是
(3)元素c和元素f形成的化合物的化学式为
(4)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号。已知Te与S元素同主族。
①碲及其化合物可能具有的性质为
A.单质Te在常温下是固体
B.H2Te比H2O稳定
C.H2TeO4的酸性比H2SO4的弱
D.Cl2通入H2Te溶液中不发生反应
E.Te元素位于周期表中第六周期
②TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。写出TeO2与过量NaOH溶液反应的离子方程式
③工业上,把SO2通入TeCl4溶液中,可得到Te,该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
3 . 陈述Ⅰ和Ⅱ均正确且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 用ClO2对自来水进行消毒 | ClO2具有还原性 |
| B | 用石灰乳出去烟气中的SO2 | SO2是酸性氧化物 |
| C | 蓝色的胆矾晶体加入浓硫酸后变白 | 浓硫酸有脱水性 |
| D | pH小于7的雨水是酸雨 | 硫和氮的氧化物容易容易引起酸雨 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 某油脂常温下呈液态,其中一种成分的结构简式为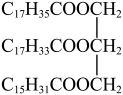 。
。
| A.加浓硫酸并加热 | B.加稀硫酸并加热 |
| C.加热 | D.加入NaOH溶液并加热 |
(2)1mol该油脂与
 加成最多消耗
加成最多消耗
(3)写出淀粉在催化剂作用下水解生成葡萄糖的反应方程式
(4)顺式聚异戊二烯的结构简式为
(5)新型合成材料的单体的结构简式如下:
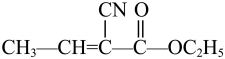
(6)外科缝合手术材料的结构片段
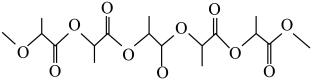 ,写出合成该聚合物所需的单体的结构简式
,写出合成该聚合物所需的单体的结构简式
您最近一年使用:0次
名校
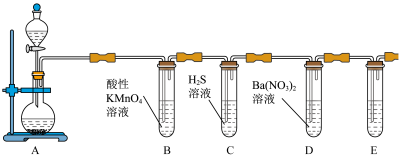
5 . 在装置A圆底烧瓶中加入Na2SO3固体,分液漏斗中滴加浓硫酸制备SO2气体,然后验证SO2的性质,根据题意回答下列问题。_______ 。
(2)B中溶液褪色,请用离子方程式解释_______ 。
(3)C中有黄色沉淀生成说明SO2具有_____ ,D中有白色沉淀生成说明SO2具有_____ 。(填“氧化性”、“还原性”或“酸性”)
(4)E装置中的试剂为_______ 。
(5)某兴趣小组欲证明还原性SO2>Fe2+,请设计试验方案_______ (请写明实验操作、现象和结论;限选试剂:SO2,硫酸铁,FeCl3,酸性高锰酸钾,盐酸,BaCl2溶液)
(2)B中溶液褪色,请用离子方程式解释
(3)C中有黄色沉淀生成说明SO2具有
(4)E装置中的试剂为
(5)某兴趣小组欲证明还原性SO2>Fe2+,请设计试验方案
您最近一年使用:0次
名校
6 . 下列生产或实验事实引出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 在容积可变的密闭容器中发生反应:2NH3(g) N2H4 (g)+H2 (g),把容器体积缩小一半 N2H4 (g)+H2 (g),把容器体积缩小一半 | 正反应速率加快,逆反应速率也加快 |
| B | 将少量Na2S2O3样品溶于水,滴入过量的稀硝酸后,再滴入BaCl2溶液,有白色沉淀产生 | 说明Na2S2O3已变质 |
| C | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 与氨溶液中无铵根离子 |
| D | 向鸡蛋清溶液中滴加饱和硫酸铵溶液,振荡,有固体析出 | 硫酸铵溶液能使蛋白质变性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 定量分析是研究物质常用的方法,下列有关说法正确的是
| A.已知1mol有机物A完全燃烧时生成xmol CO2和ymol H2O,可推知其分子式为CxH2y |
B.在标准状况下将充满NO2的试管倒扣在水中,假设溶质不扩散,则试管内溶液浓度为 |
| C.等质量的甲烷与乙烯气体分别完全燃烧时,乙烯消耗氧气量较多 |
| D.1mol乙烯与氯气完全发生加成反应,然后使加成产物与氯气在光照条件下充分反应,假定氢原子全部被取代,两个过程消耗Cl2共3mol |
您最近一年使用:0次
8 . N、S元素化合物知识在高中化学体系中占有重要地位,请根据题意回答下列问题。
(1)工业制硝酸中NH3的催化氧化化学方程式_______ 。
(2)检验溶液中含有NH4+的离子方程式_______ ,实验室一般使用_______ 检验该反应有氨气生成。
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有_______ 和_______ 。(填浓硫酸的性质)
(4)铜与浓硫酸的化学反应方程式为_______ 。
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因_______ 。
(1)工业制硝酸中NH3的催化氧化化学方程式
(2)检验溶液中含有NH4+的离子方程式
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有
(4)铜与浓硫酸的化学反应方程式为
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因
您最近一年使用:0次
名校
9 . Ⅰ.用如图所示的装置测定中和反应的反应热。____ ,其能否用铜质材料替代?____ (填“能”或“不能”)。
(2)将浓度为 的酸溶液和
的酸溶液和 的碱溶液各50mL混合(溶液密度均为1
的碱溶液各50mL混合(溶液密度均为1 ),生成溶液的比热容
),生成溶液的比热容 ,测得温度如表所示:
,测得温度如表所示:
 的
的
_______ (保留一位小数)。
Ⅱ.某学生用已知物质的量浓度的硫酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用硫酸溶液的体积为_______ mL。
根据表中数据计算可得该NaOH溶液的物质的量浓度为_______ (保留四位有效数字) 。
。
(5)下列操作可能使所测NaOH溶液的浓度数值偏小的是_______(填选项字母)。
Ⅲ.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的 溶液的浓度,现用0.1000
溶液的浓度,现用0.1000 的酸性
的酸性 溶液进行滴定。
溶液进行滴定。
(6)写出滴定的离子方程式:_______ 。
(7)用酸性 溶液进行滴定时,酸性
溶液进行滴定时,酸性 溶液应该装在
溶液应该装在_______ (填“酸式”或“碱式”)滴定管中,滴定终点的现象是_______ 。

(2)将浓度为
 的酸溶液和
的酸溶液和 的碱溶液各50mL混合(溶液密度均为1
的碱溶液各50mL混合(溶液密度均为1 ),生成溶液的比热容
),生成溶液的比热容 ,测得温度如表所示:
,测得温度如表所示:| 反应物 | 起始温度 /℃ /℃ | 最高温度 /℃ /℃ |
| 甲组(HCl+NaOH) | 15.0 | 18.3 |
乙组( ) ) | 15.0 | 18.1 |
 的
的
Ⅱ.某学生用已知物质的量浓度的硫酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用硫酸溶液的体积为

| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000 硫酸的体积/mL 硫酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
 。
。(5)下列操作可能使所测NaOH溶液的浓度数值偏小的是_______(填选项字母)。
| A.酸式滴定管未用标准硫酸润洗就直接注入标准硫酸 |
| B.读取硫酸体积时,开始时仰视读数,滴定结束时俯视读数 |
| C.酸式滴定管滴定前有气泡,滴定后气泡消失 |
| D.锥形瓶用水洗涤后,用待测液润洗 |
Ⅲ.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的
 溶液的浓度,现用0.1000
溶液的浓度,现用0.1000 的酸性
的酸性 溶液进行滴定。
溶液进行滴定。(6)写出滴定的离子方程式:
(7)用酸性
 溶液进行滴定时,酸性
溶液进行滴定时,酸性 溶液应该装在
溶液应该装在
您最近一年使用:0次
名校
解题方法
10 . 实验探究是化学发展的必要途径。下列实验过程可以达到相应实验目的的是
| 选项 | 实验过程 | 实验目的 |
| A | 在实验室,向刚制得的乙酸乙酯中加入饱和碳酸钠溶液,振荡,然后分液 | 除去乙酸乙酯中混有的乙酸、乙醇 |
| B | 在坩埚中, 受热分解为 受热分解为 | 用 制备 制备 固体 固体 |
| C | 向两支试管中加入少量同体积、同浓度的草酸溶液,再分别加入过量同体积、不同浓度的 溶液 溶液 | 根据褪色时间来探究浓度对反应速率的影响 |
| D | 用pH试纸测定相同浓度的NaSCN与NaClO溶液的pH,pH越大酸性越弱 | 比较HSCN与HClO的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



