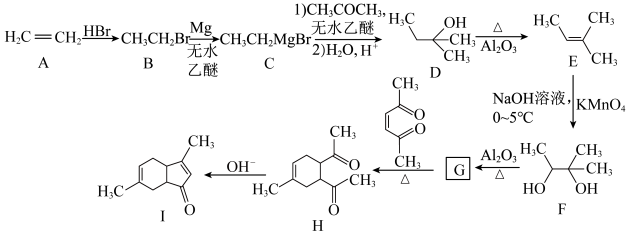
1 . 乙烯的用途广泛,被誉为有机合成之母。以下是以乙烯为原料制备某化工原料中间体I的合成路线。
(1) 的反应类型为
的反应类型为_______ 。
(2)在D的同分异构体中,同时满足下列条件的共有_______ 种;
①能与金属钠反应产生氢气;②在铜催化氧化的条件下,氧化产物能发生银镜反应。其中,核磁共振氢谱显示为3组峰,且峰面积比为 的同分异构体的结构简式为
的同分异构体的结构简式为_______ 。
(3)已知: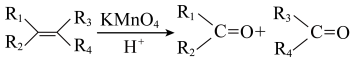 ,E与足量酸性
,E与足量酸性 溶液反应生成的有机物的结构简式为
溶液反应生成的有机物的结构简式为_______ 。
(4)G的结构简式为_______ ,用系统命名法命名为_______ 。
(5)在碱性条件下, 反应的化学方程式为
反应的化学方程式为_______ 。
(1)
 的反应类型为
的反应类型为(2)在D的同分异构体中,同时满足下列条件的共有
①能与金属钠反应产生氢气;②在铜催化氧化的条件下,氧化产物能发生银镜反应。其中,核磁共振氢谱显示为3组峰,且峰面积比为
 的同分异构体的结构简式为
的同分异构体的结构简式为(3)已知:
 ,E与足量酸性
,E与足量酸性 溶液反应生成的有机物的结构简式为
溶液反应生成的有机物的结构简式为(4)G的结构简式为
(5)在碱性条件下,
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解题方法
2 . 下列分子属于极性分子的是
A. | B. | C. | D. |
您最近一年使用:0次
3 . 环己酮是无色油状液体, 时在水中的溶解度为
时在水中的溶解度为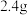 。实验室由环己醇制备环己酮。
。实验室由环己醇制备环己酮。
【实验原理】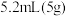 环已醇和
环已醇和 冰醋酸,开动磁力搅拌器。在冰水浴冷却下,逐滴加入次氯酸钠溶液至稍过量。
冰醋酸,开动磁力搅拌器。在冰水浴冷却下,逐滴加入次氯酸钠溶液至稍过量。
Ⅱ.在室温下继续搅拌 ,然后加入饱和亚硫酸氢钠溶液。
,然后加入饱和亚硫酸氢钠溶液。
Ⅲ.在反应混合物中加入 水、
水、 氯化铝,去掉仪器X,换成蒸馏装置,加热蒸馏,至馏出液无油珠滴出为止。
氯化铝,去掉仪器X,换成蒸馏装置,加热蒸馏,至馏出液无油珠滴出为止。
Ⅳ.在搅拌情况下向馏出液中加入无水碳酸钠至中性,然后再加入精制食盐使之饱和,将此液体倒入分液漏斗,分出有机层。
Ⅴ.向有机层中加入无水 ,静置,过滤,对滤液进行蒸馏,得到产品
,静置,过滤,对滤液进行蒸馏,得到产品 。
。
回答下列问题。
(1)仪器X的名称为_______ 。
(2)步骤Ⅰ中,加入冰醋酸除作为溶剂外,还有的作用是_______ 。用淀粉碘化钾试纸可检验反应后的液体,如果试纸变_______ 色,说明次氯酸钠过量。
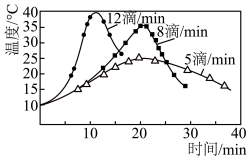
(3)步骤Ⅰ中,次氯酸钠溶液要在冰水浴冷却下逐滴加入,勿使氧化反应进行得过于猛烈而升温过高,否则产物环己酮将进一步被氧化而发生碳链断裂。在次氯酸钠的不同滴加速度下,在冰水浴存在的情况下,溶液温度随滴加时间变化曲线如图,为了控制好反应温度,应选择的滴速为_______ 滴/ 。
。_______ 。
(5)在步骤Ⅳ中,加入精制食盐的目的是_______ 。
(6)在步骤Ⅴ中,加入无水 的作用为
的作用为_______ 。
(7)产品的产率为_______ (精确至0.1%)。
 时在水中的溶解度为
时在水中的溶解度为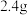 。实验室由环己醇制备环己酮。
。实验室由环己醇制备环己酮。【实验原理】
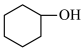 +NaClO
+NaClO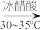
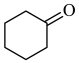 +NaCl+H2O
+NaCl+H2O 
【装置示意图】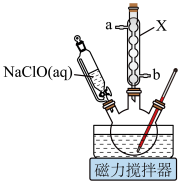
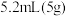 环已醇和
环已醇和 冰醋酸,开动磁力搅拌器。在冰水浴冷却下,逐滴加入次氯酸钠溶液至稍过量。
冰醋酸,开动磁力搅拌器。在冰水浴冷却下,逐滴加入次氯酸钠溶液至稍过量。Ⅱ.在室温下继续搅拌
 ,然后加入饱和亚硫酸氢钠溶液。
,然后加入饱和亚硫酸氢钠溶液。Ⅲ.在反应混合物中加入
 水、
水、 氯化铝,去掉仪器X,换成蒸馏装置,加热蒸馏,至馏出液无油珠滴出为止。
氯化铝,去掉仪器X,换成蒸馏装置,加热蒸馏,至馏出液无油珠滴出为止。Ⅳ.在搅拌情况下向馏出液中加入无水碳酸钠至中性,然后再加入精制食盐使之饱和,将此液体倒入分液漏斗,分出有机层。
Ⅴ.向有机层中加入无水
 ,静置,过滤,对滤液进行蒸馏,得到产品
,静置,过滤,对滤液进行蒸馏,得到产品 。
。回答下列问题。
(1)仪器X的名称为
(2)步骤Ⅰ中,加入冰醋酸除作为溶剂外,还有的作用是
(3)步骤Ⅰ中,次氯酸钠溶液要在冰水浴冷却下逐滴加入,勿使氧化反应进行得过于猛烈而升温过高,否则产物环己酮将进一步被氧化而发生碳链断裂。在次氯酸钠的不同滴加速度下,在冰水浴存在的情况下,溶液温度随滴加时间变化曲线如图,为了控制好反应温度,应选择的滴速为
 。
。
(5)在步骤Ⅳ中,加入精制食盐的目的是
(6)在步骤Ⅴ中,加入无水
 的作用为
的作用为(7)产品的产率为
您最近一年使用:0次
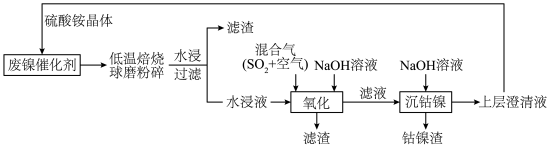
4 . 一种废镍催化剂回收镍、钴元素的工艺流程图如下,流程图中水浸液中含有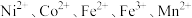 。
。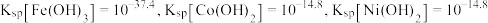 。
。
回答下列问题。
(1)球磨粉碎的作用是_______ 。
(2)“氧化”中,混合气在金属离子的催化作用下,生成具有强氧化性的过一硫酸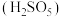 ,其反应的化学方程式为
,其反应的化学方程式为_______ 。
(3)“氧化”中, 被过一硫酸氧化为
被过一硫酸氧化为 沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:
沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:_______ (已知 的电离第一步完全,第二步微弱);用
的电离第一步完全,第二步微弱);用 溶液调节
溶液调节 ,还有
,还有_______ (写离子符号)也会形成沉淀而除去。
(4)“氧化”中保持空气通入速率不变, 的氧化率与
的氧化率与 的体积分数的关系如图所示。
的体积分数的关系如图所示。 的体积分数为9.0%时,
的体积分数为9.0%时, 的氧化率最大;当
的氧化率最大;当 的体积分数大于9.0%时,继续增大
的体积分数大于9.0%时,继续增大 的体积分数,
的体积分数, 的氧化率减小的原因可能是
的氧化率减小的原因可能是_______ 。 沉淀完全,需控制溶液的
沉淀完全,需控制溶液的 不低于
不低于_______ (说明:当溶液中的 浓度均小于
浓度均小于 时,认为已沉淀完全)。
时,认为已沉淀完全)。
(6)铬、钴、镍都属于副族金属元素,其中铬与氮气在一定条件下可以合成氨化铬,且氮化铬的晶体结构及类型与氯化钠的相似,其晶胞结构如图所示。A点的分数坐标为 ,则B点的分数坐标为
,则B点的分数坐标为_______ 。已知氮化铬的晶胞参数为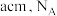 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为_______  。
。
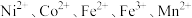 。
。
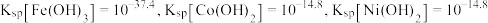 。
。回答下列问题。
(1)球磨粉碎的作用是
(2)“氧化”中,混合气在金属离子的催化作用下,生成具有强氧化性的过一硫酸
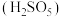 ,其反应的化学方程式为
,其反应的化学方程式为(3)“氧化”中,
 被过一硫酸氧化为
被过一硫酸氧化为 沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式:
沉淀,过一硫酸被还原为硫酸根离子,写出该反应的离子方程式: 的电离第一步完全,第二步微弱);用
的电离第一步完全,第二步微弱);用 溶液调节
溶液调节 ,还有
,还有(4)“氧化”中保持空气通入速率不变,
 的氧化率与
的氧化率与 的体积分数的关系如图所示。
的体积分数的关系如图所示。 的体积分数为9.0%时,
的体积分数为9.0%时, 的氧化率最大;当
的氧化率最大;当 的体积分数大于9.0%时,继续增大
的体积分数大于9.0%时,继续增大 的体积分数,
的体积分数, 的氧化率减小的原因可能是
的氧化率减小的原因可能是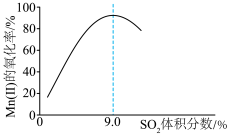
 沉淀完全,需控制溶液的
沉淀完全,需控制溶液的 不低于
不低于 浓度均小于
浓度均小于 时,认为已沉淀完全)。
时,认为已沉淀完全)。(6)铬、钴、镍都属于副族金属元素,其中铬与氮气在一定条件下可以合成氨化铬,且氮化铬的晶体结构及类型与氯化钠的相似,其晶胞结构如图所示。A点的分数坐标为
 ,则B点的分数坐标为
,则B点的分数坐标为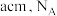 为阿伏加德罗常数,则该晶胞的密度为
为阿伏加德罗常数,则该晶胞的密度为 。
。
您最近一年使用:0次
5 . 一种新型溴流电池,可作储能设备(如图所示)。充电时,电极a的反应为: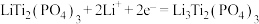 。下列说法正确的是
。下列说法正确的是
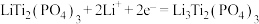 。下列说法正确的是
。下列说法正确的是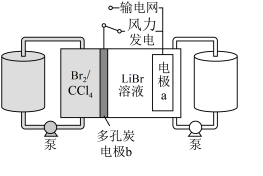
| A.充电时,锂元素被还原 |
B.放电时, 溶液的浓度不变 溶液的浓度不变 |
C.充电时,总反应式为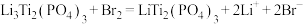 |
D.每生成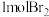 ,电极a的质量理论上增加 ,电极a的质量理论上增加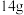 |
您最近一年使用:0次
6 . 室温下,某实验兴趣小组用 溶液标定某盐酸浓度,用甲基橙作指示剂,滴定曲线如图丁所示。下列说法正确的是
溶液标定某盐酸浓度,用甲基橙作指示剂,滴定曲线如图丁所示。下列说法正确的是
 溶液标定某盐酸浓度,用甲基橙作指示剂,滴定曲线如图丁所示。下列说法正确的是
溶液标定某盐酸浓度,用甲基橙作指示剂,滴定曲线如图丁所示。下列说法正确的是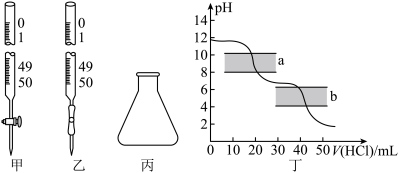
A.滴定中 溶液应该盛放在乙仪器中 溶液应该盛放在乙仪器中 |
| B.读数时,应双手一上一下持滴定管 |
C. 标准溶液吸收了空气中的 标准溶液吸收了空气中的 ,会使测得的盐酸浓度偏大 ,会使测得的盐酸浓度偏大 |
D.滴定终点 在b区域 在b区域 |
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.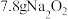 中含有的离子总数为 中含有的离子总数为 |
B.常温下, 的 的 溶液中含有的 溶液中含有的 总数约为 总数约为 |
C.含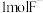 的 的 和 和 的混合物中所含质子数为 的混合物中所含质子数为 |
D.若反应中生成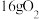 ,则转移电子数一定为 ,则转移电子数一定为 |
您最近一年使用:0次
8 . 下列事实能用平衡移动原理解释的是
| A.生铁比高纯度的铁在空气中更容易发生电化学腐蚀 |
B.用 分解制取氧气时加入少量 分解制取氧气时加入少量 固体可加速 固体可加速 的分解 的分解 |
C.密闭烧瓶内存在平衡体系: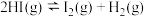 ,缩小容器的容积,混合气体颜色加深 ,缩小容器的容积,混合气体颜色加深 |
| D.漂白粉水溶液中滴入少量醋酸,漂白效果增强 |
您最近一年使用:0次
9 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是
A. 和 和 的空间结构相同 的空间结构相同 | B. 的键角小于 的键角小于 的键角 的键角 |
C. 和 和 均为非极性分子 均为非极性分子 | D. 与 与 的中心原子的杂化方式不同 的中心原子的杂化方式不同 |
您最近一年使用:0次
10 . 在催化下, 加氢合成甲酸发生反应Ⅰ,同时还伴有反应Ⅱ发生。
加氢合成甲酸发生反应Ⅰ,同时还伴有反应Ⅱ发生。
Ⅰ.
Ⅱ.
回答下列问题。
(1)已知: 时,部分物质的相对能量如表所示,则
时,部分物质的相对能量如表所示,则 的相对能量为
的相对能量为_______  。
。
(2)为了提高二氧化碳转化为甲酸的转化率,工业上常采用以下方法:
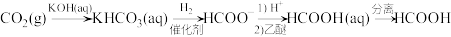
步骤1 步骤2 步骤3
①写出步骤1反应的离子方程式:_______ 。
②其他条件不变,步骤1中 转化为
转化为 的转化率与温度的关系如图所示。
的转化率与温度的关系如图所示。_______ ,后又下降的可能原因是_______ 。
③流程图步骤2中,加入乙醚的作用是_______ ,步骤3的分离方法是_______ 。
(3)保持 、恒压,
、恒压, 和
和 的投料物质的量之比为
的投料物质的量之比为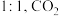 的初始分压为
的初始分压为 ,测得
,测得 的转化率
的转化率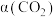 与时间t的关系如图所示。
与时间t的关系如图所示。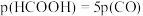 ,则反应Ⅰ的
,则反应Ⅰ的
_____ 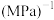 (用含
(用含 的式子表示)。
的式子表示)。
 加氢合成甲酸发生反应Ⅰ,同时还伴有反应Ⅱ发生。
加氢合成甲酸发生反应Ⅰ,同时还伴有反应Ⅱ发生。Ⅰ.

Ⅱ.

回答下列问题。
(1)已知:
 时,部分物质的相对能量如表所示,则
时,部分物质的相对能量如表所示,则 的相对能量为
的相对能量为 。
。| 物质 | 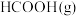 |  |
相对能量/ | 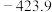 |  |
(2)为了提高二氧化碳转化为甲酸的转化率,工业上常采用以下方法:
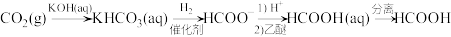
步骤1 步骤2 步骤3
①写出步骤1反应的离子方程式:
②其他条件不变,步骤1中
 转化为
转化为 的转化率与温度的关系如图所示。
的转化率与温度的关系如图所示。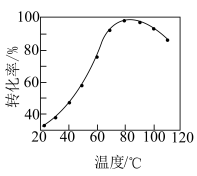
③流程图步骤2中,加入乙醚的作用是
(3)保持
 、恒压,
、恒压, 和
和 的投料物质的量之比为
的投料物质的量之比为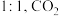 的初始分压为
的初始分压为 ,测得
,测得 的转化率
的转化率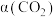 与时间t的关系如图所示。
与时间t的关系如图所示。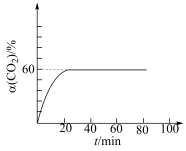
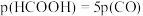 ,则反应Ⅰ的
,则反应Ⅰ的
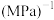 (用含
(用含 的式子表示)。
的式子表示)。
您最近一年使用:0次



